
来源:特诺科研
葡萄膜黑色素瘤(UVM)是成人最常见原发性眼内恶性肿瘤,80% 以上患者会发生肝脏转移,metastatic 患者中位生存期仅 6-12 个月,免疫治疗疗效有限,临床缺乏非侵入性预后工具和明确靶向靶点。近日,暨南大学附属广州红十字会医院、第一附属医院眼科联合团队在《International Journal of Surgery》(IF=10.3,外科领域顶刊,开源获取,0 版面费)发表重磅多组学研究:整合单细胞 RNA-seq、转录组、路径组学技术,结合体外功能实验,首次揭示 “癌症干细胞(HStem)- 癌相关成纤维细胞(CAFs)互作” 驱动 UVM 进展的核心机制,构建可直接落地的病理图像预后评分(IPS),筛选 4 种高风险患者敏感药物,锁定 IGFBP7 关键靶点,为罕见眼癌的精准预后与治疗提供完整解决方案!

文章信息速览
原标题:Multi-omics integrative analysis of stemness-associated pathological signatures to guide prognosis and therapeutic strategies in uveal melanoma
期刊:International Journal of Surgery(IF=10.3,外科领域顶刊,开源获取,0 版面费)
关键词:葡萄膜黑色素瘤(UVM)、癌症干细胞(CSCs)、多组学、单细胞 RNA-seq、路径组学、预后评分(IPS)、IGFBP7、免疫冷肿瘤、靶向治疗、癌相关成纤维细胞(CAFs)
研究背景与临床痛点
疾病困境:UVM 罕见但恶性度高,转移后无有效治疗,患者生存期极短,临床需求迫切,易获顶刊关注;
预后空白:传统病理评估依赖主观判读,缺乏量化、非侵入性预后工具,无法精准分层患者风险;
治疗瓶颈:免疫检查点抑制剂对 UVM 响应率低,“免疫冷肿瘤” 占比高,缺乏针对性靶向策略;
机制盲区:癌症干细胞是 UVM 转移和耐药的关键,但 “干细胞特性 - 肿瘤微环境 - 临床预后” 的关联机制未被解析,缺乏可视化评估手段和可靶向靶点。
多组学顶刊发文逻辑拆解
这篇 0 版面费开源顶刊的成功,核心在于 “临床问题→多组学整合→机制解析→临床转化” 的完整闭环,5 大关键步骤完美契合顶刊 “创新性 + 实用性 + 可重复性” 要求,每个环节都有明确图表支撑,值得医生借鉴:
1. 第一步:临床问题切入,单细胞测序锁定核心致病亚群(图 1、2)
发文关键:从“干细胞驱动恶性进展” 这一核心临床问题出发,用单细胞技术打开机制黑箱,为后续多组学整合奠定基础;
研究细节:
样本选择:11 例 UVM 样本(8 原发 + 3 转移),覆盖疾病不同阶段,提升研究代表性(图 1A);
细胞分群:质控后 46502 个细胞,鉴定 16 类细胞群,通过 inferCNV 筛选 30604 个恶性细胞(图 1B-C、2A);
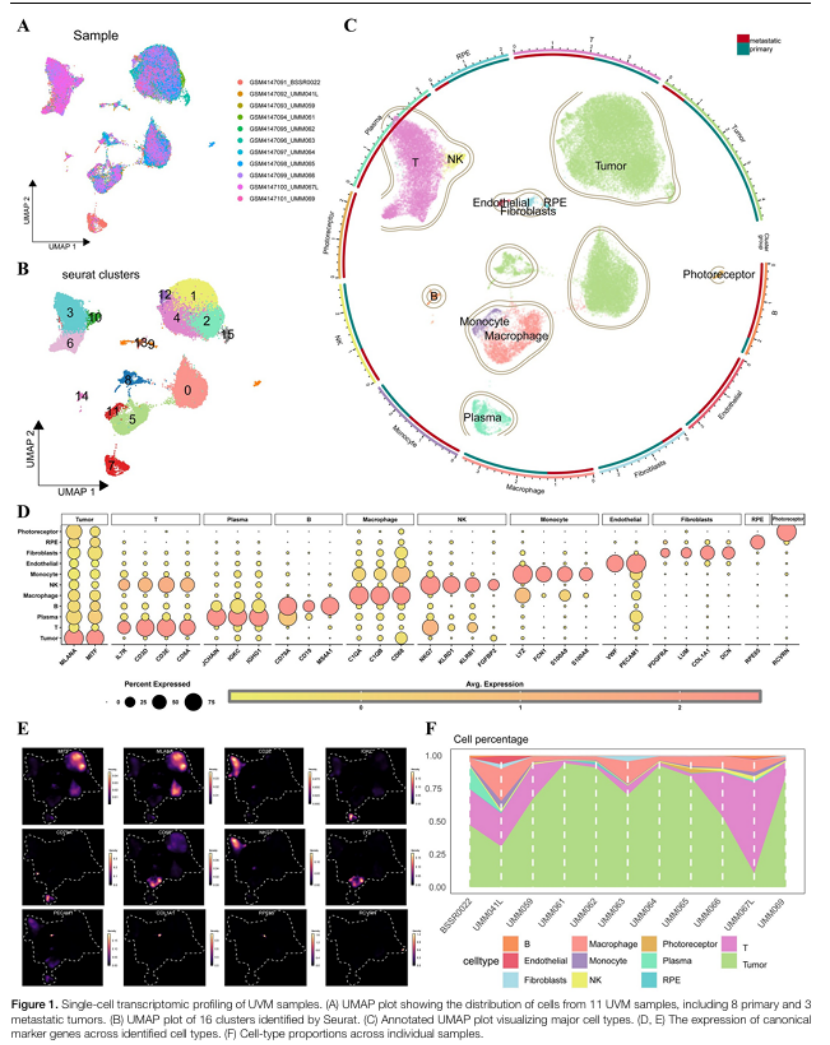
图1
核心发现:用 CytoTRACE 算法锁定高干细胞样(HStem)亚群,这类细胞位于伪时间轨迹早期(图 2F),富集于原发肿瘤(图 2G),与 CAFs 存在密集配体 - 受体相互作用(图 3A-B),是驱动转移的 “种子细胞”;
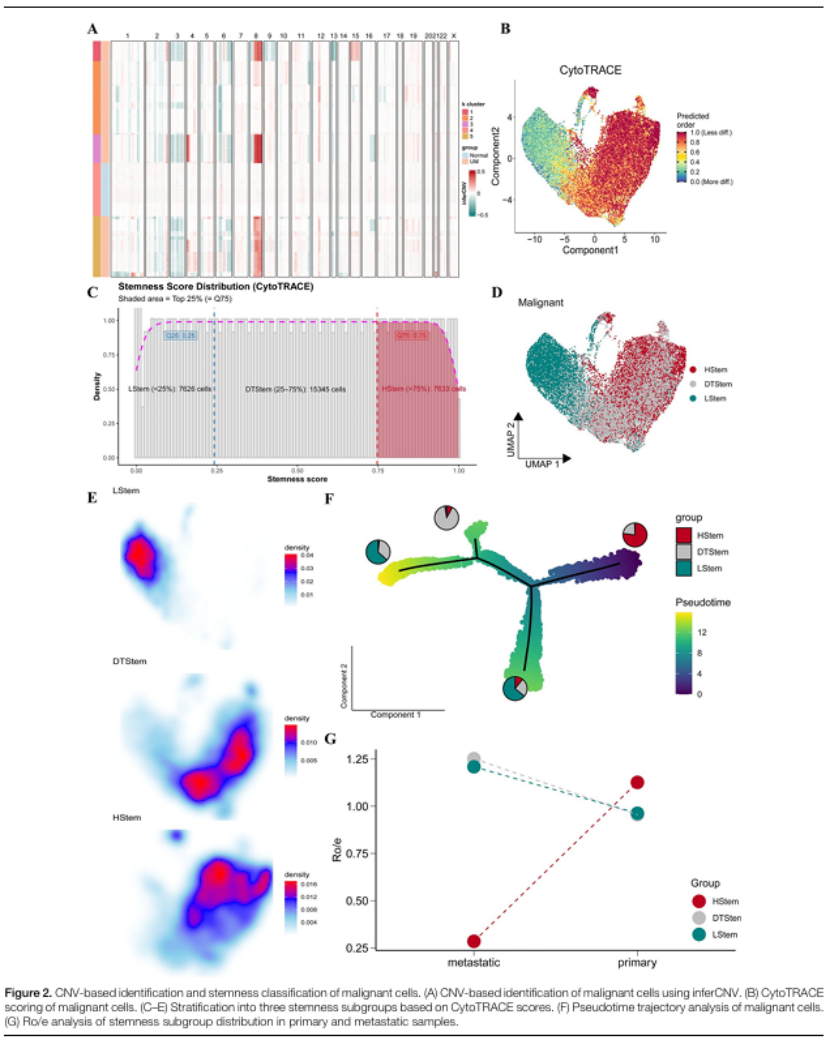
图2
顶刊加分点:将单细胞数据与肿瘤进展阶段关联,明确 HStem 细胞的临床意义,避免单纯 “细胞分群” 无临床价值的误区。
2. 第二步:多组学整合,hdWGCNA 挖掘特征基因(图 3)
发文关键:单细胞找到核心亚群后,通过加权基因共表达网络(hdWGCNA)关联转录组数据,筛选可用于临床转化的特征基因,搭建 “细胞亚群 - 分子特征 - 临床预后” 的桥梁;
研究细节:
模块分析:对恶性细胞进行 hdWGCNA,鉴定 7 个基因模块,其中棕色、黄色模块与 HStem 表型强相关(图 3D);
特征基因筛选:交集模块核心基因与 HStem/LStem 差异基因,得到 93 个 HStem 特征基因,富集于蛋白质折叠、N - 糖基化生物合成等关键通路(图 3F-H);
临床验证:基于特征基因计算 HStem 评分,高评分患者总生存期显著缩短(P<0.0001,图 4I),证实分子特征的预后价值;
顶刊加分点:不只是罗列差异基因,而是通过模块分析和生存验证,筛选出有临床意义的核心基因集,为后续路径组学建模提供靶点。
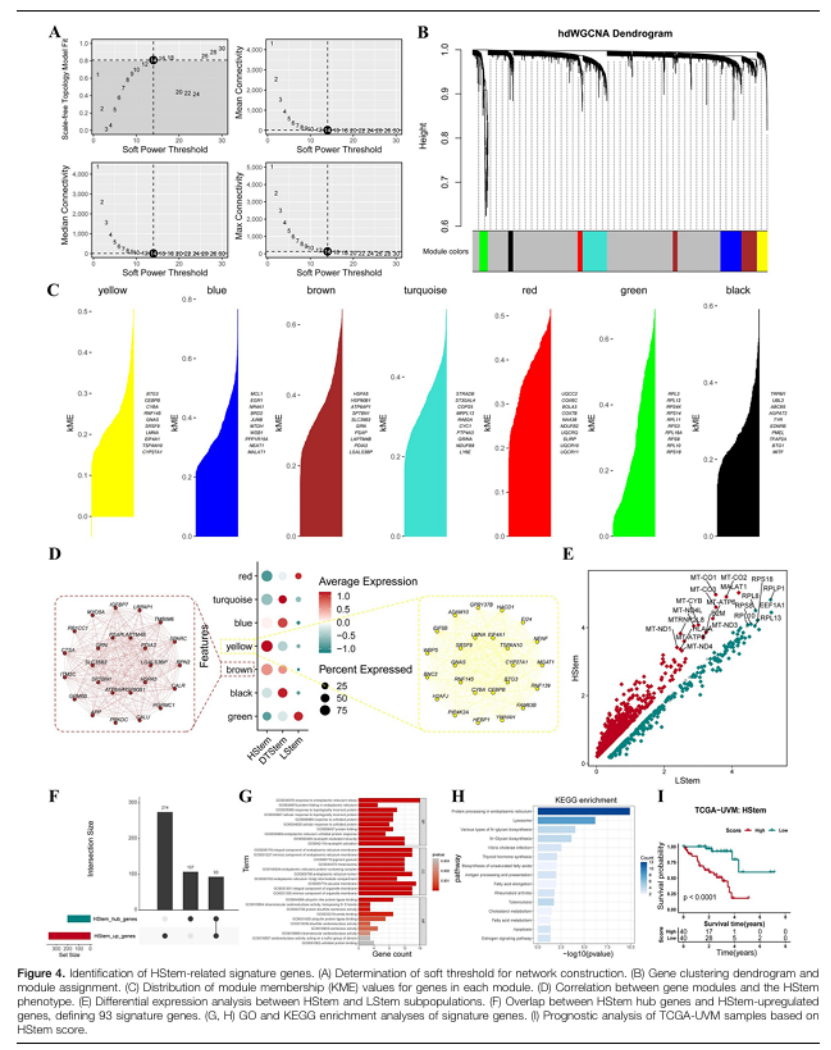
图3
3. 第三步:临床转化落地,路径组学构建可复用预后模型(图 4)
发文关键:将分子特征转化为临床可操作工具,路径组学是连接基础研究与临床应用的核心,也是顶刊青睐的“转化型” 研究方向;
研究细节:
特征提取:80 例 TCGA-UVM 病理切片,整合 ResNet50 深度特征(2048 个)和 CellProfiler 形态学特征(682 个),共 2730 个路径组学特征(图 4A);
模型构建:通过“相关性分析→单变量 Cox→Boruta 算法” 层层筛选,最终锁定 9 个核心特征,7 种机器学习模型 benchmark 后,Ridge 回归表现最优(C-index=0.81,图 4E),构建 IPS 预后评分;
临床效能:
训练集 1/2/3 年 OS 预测 AUC 达 0.84/0.85/0.87(图 5G),高 / 低 IPS 组生存差异显著(P=0.00011,图 4F);
验证集 3 年 OS 预测 AUC 高达 0.93(图 5I),仅需常规 H&E 切片即可检测,非侵入性易推广;
顶刊加分点:模型构建过程透明,有特征筛选流程和模型对比,结果可重复,且工具具有直接临床应用价值,解决“预后评估难” 的临床痛点。
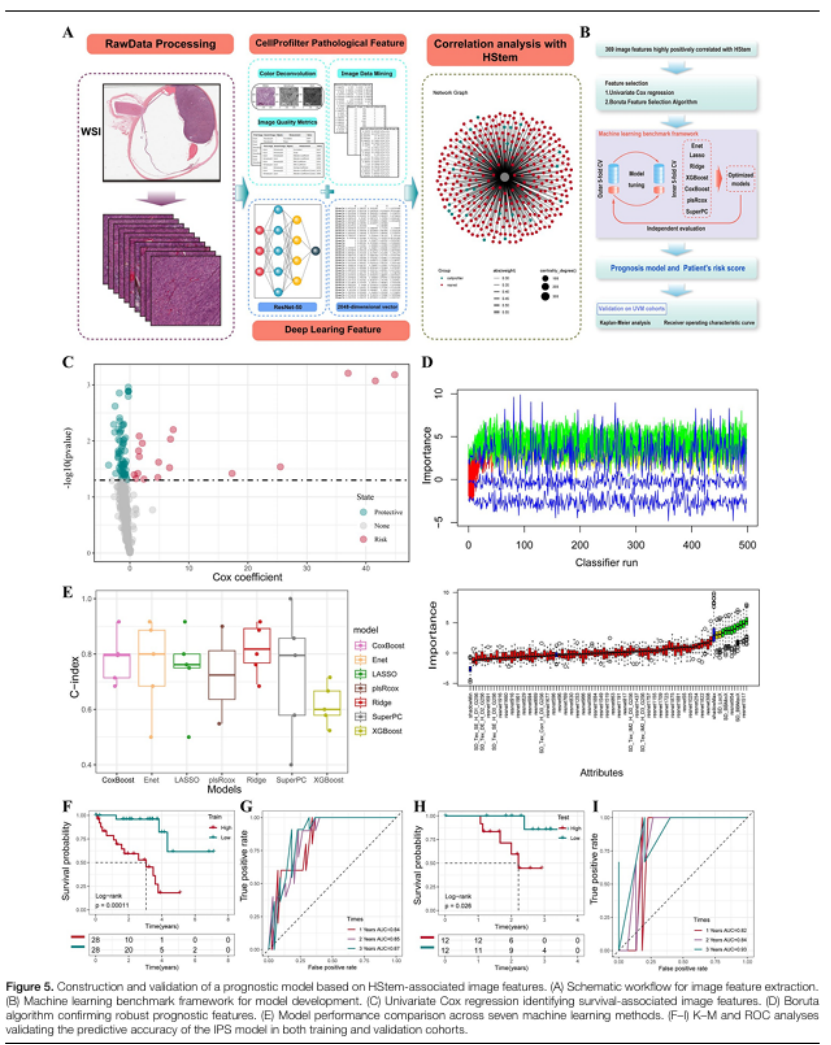
图4
4. 第四步:治疗分层,多数据库联合筛选精准药物(图 5)
发文关键:顶刊不仅关注预后,更关注治疗转化,通过药物筛选为高风险患者提供解决方案,提升研究临床价值;
研究细节:
免疫分层:先明确 IPS 分组的免疫表型 —— 高 IPS 肿瘤为 “免疫冷表型”,免疫细胞浸润少,PD-1 治疗响应率低(图 5A-B);
药物筛选:整合 CMap、CTRP/PRISM、GDSC 三大数据库,预测高 IPS 患者对 4 种药物敏感(IC50 更低):
ABT-888(PARP 抑制剂)、ATRA(维 A 酸)、AZ628(RAF 激酶抑制剂)、替西罗莫司(mTOR 抑制剂)(图 5F);
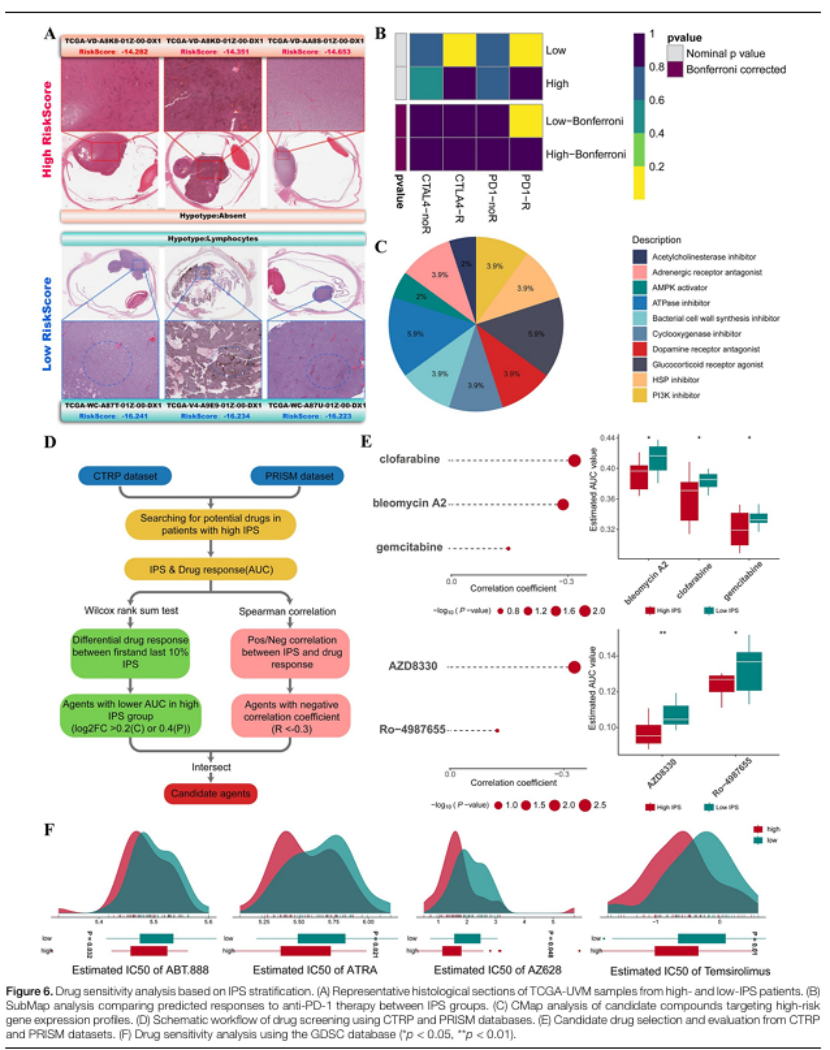
图5
机制契合:药物靶点与 HStem 细胞富集的干细胞特性、MAPK/mTOR 通路高度匹配,确保筛选结果的合理性;
顶刊加分点:药物筛选基于前期机制发现,不是盲目筛选,且药物多为已进入临床的品种,为后续临床试验提供明确方向。
5. 第五步:实验验证,锁定关键靶点闭环机制(图 6)
发文关键:多组学分析后,必须通过体外实验验证核心靶点,增强研究可信度,这是顶刊接收的“硬标准”;
研究细节:
靶点选择:从 46 个 IPS 相关 HStem 特征基因中,锁定 IGFBP7 为关键驱动基因(图 7C);
功能验证:
球形成实验:敲低 IGFBP7 后,MuM-2B、OCM-1 两种 UVM 细胞系的干细胞特性显著降低(图 6A-B);
Transwell 实验:细胞迁移和侵袭能力显著减弱(P<0.05,图 6C-E);
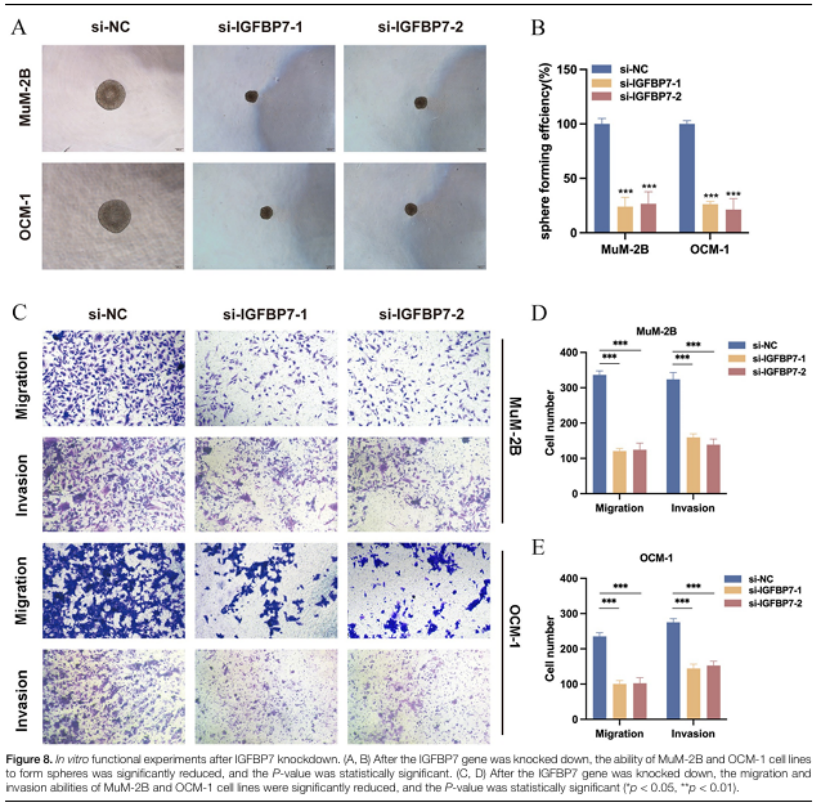
图6
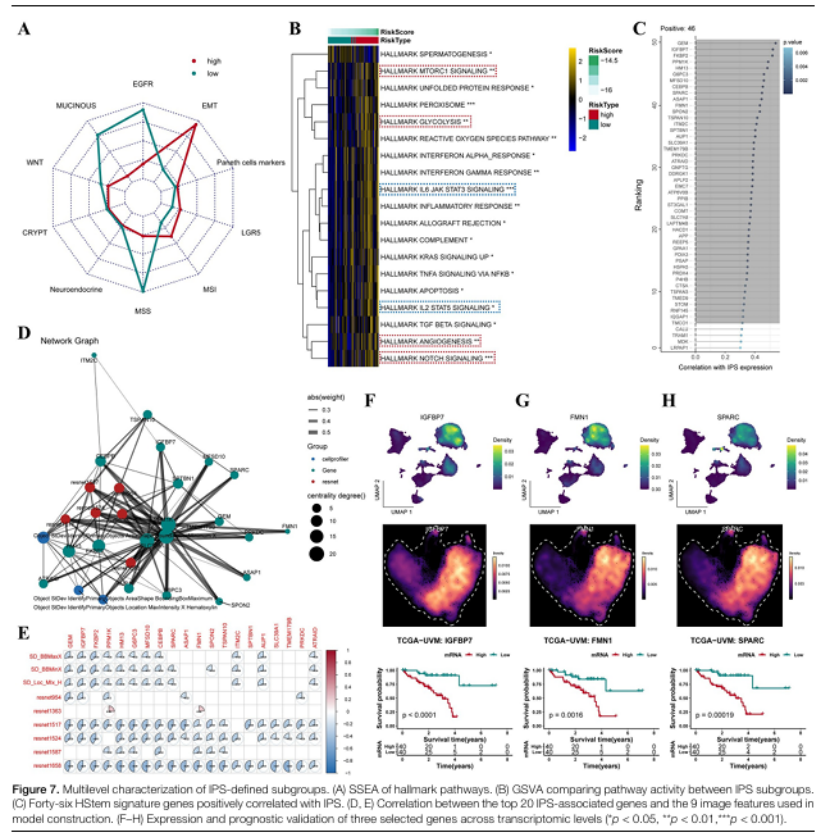
图7
机制意义:IGFBP7 是连接 HStem 细胞、CAF 互作、肿瘤侵袭的核心分子,为靶向治疗提供直接靶点;
顶刊加分点:选择两种细胞系验证,实验设计严谨,明确靶点的功能价值,形成“多组学发现→实验验证” 的闭环。
总结:多组学顶刊发文“黄金法则”
临床导向:从“预后评估、治疗响应、靶点缺乏” 等临床痛点切入,避免纯基础研究;
技术整合:单细胞测序(找核心亚群)+ 转录组(挖分子特征)+ 路径组学(临床转化),多技术交叉验证,提升说服力;
临床转化:不仅要发现机制,还要构建可落地的工具(如 IPS 模型)、筛选可复用的药物、验证可靶向的靶点;
开源优势:选择 0 版面费开源顶刊(如本文《International Journal of Surgery》),降低发表成本,扩大研究影响力;
图表支撑:每个核心结论都有明确图表对应(如 HStem 细胞→图 2,IPS 模型→图 5,IGFBP7 验证→图 8),确保结果可重复。
这篇研究通过“临床问题 - 多组学整合 - 机制验证 - 临床转化” 的完整链条,仅用 11 例单细胞样本 + 80 例临床样本,就实现了 IF=10.3 顶刊开源发表,充分证明 “小样本 + 强逻辑 + 高转化” 是罕见病多组学研究的高效发文路径。
原文DOI: 10.1097/JS9.0000000000004914
专注期刊投稿、发表十年,任何投稿、写作难题欢迎咨询!

PAPER INFORMATION

快速预审、投刊前指导、专业学术评审,对文章进行评价

校对编辑、深度润色,让稿 件符合学术规范,格式体例等标准
.png)
适用于语句和结构尚需完善和调整的中文文章,确保稿件达到要求
.png)
数据库包括: 期刊、文书籍、会议、预印章、书、百科全书和摘要等

让作者在期刊选择时避免走弯路,缩短稿件被接收的周期

根据目标期刊格式要求对作者文章进行全面的格式修改和调整
.png)
帮助作者将稿件提交至目标期刊投稿系统,降低退稿或拒稿率
.png)
按照您提供的稿件内容,指导完成投稿附信(cover letter)

北京总部:北京市海淀区碧桐园 3 号楼 2 层 211 广州办事处:广州市黄埔区科学城国际企业孵化器 E栋306 联系人:客服 / 18163670350
Copyright © 2022-2024 北京特诺科技有限公司 版权所有 备案/许可证编号为: 京 ICP 备 2023007944 号