
来源:特诺科研
COVID-19、流感、呼吸道合胞病毒(RSV)作为高发呼吸道病毒感染,临床症状相似但病理机制、治疗响应差异显著,传统诊断难以及时区分,重症救治缺乏针对性靶点。近日,广州国家实验室、广东省人民医院等团队在《npj Digital Medicine》(IF=15.1,Nature 子刊顶刊)发表里程碑式研究:通过可解释 AI 整合多组学数据(GWAS + 转录组 + 蛋白质组) ,系统解析三种病毒的宿主反应差异与共性,首次绘制 “共同抗病毒通路 + 病毒专属致病机制” 全景图,锁定6 大因果蛋白,为精准鉴别诊断、靶向治疗及广谱抗病毒策略提供核心依据!

文章信息速览
原标题:Explainable AI multiomics analysis reveals shared and divergent host responses in COVID-19 and influenza
期刊:npj Digital Medicine(IF=15.1,开源获取)
关键词:可解释 AI、多组学、COVID-19、流感、RSV、宿主反应、孟德尔随机化(MR)、因果蛋白、精准治疗
核心亮点
这篇顶刊的核a心突破在于“多组学数据整合 + 可解释 AI 解码 + 因果机制验证 + 临床转化落地” 的闭环,5 大核心发现直击诊疗痛点,完美契合顶刊对 “创新性 + 可靠性 + 转化价值” 的三重要求:
1. 第一步:多组学 + 可解释 AI,构建病毒宿主反应 “全景分析框架”
数据整合:整合 3 类核心数据 ——① COVID-19 HGI GWAS(Release 7,>100 万人);② 流感 / RSV 人体挑战试验转录组(GEO GSE73072);③ COMBAT 多组学血液图谱(COVID-19 vs 流感,含转录组、蛋白质组、免疫表型);
可解释 AI 模型:采用梯度提升决策树(XGBoost)+ SHAP 分析,既保证分类准确性,又量化每个特征的生物学贡献,避免 “黑箱模型”;
模型效能:区分 COVID-19 与流感 AUROC 达 0.93(混合严重度队列)、重症亚组 AUROC 0.88,即使轻度病例也达 0.75,远超传统检测手段。
2. 第二步:三大病毒的 “免疫指纹”:共同防御 + 专属致病机制(图 1、2)
共同抗病毒核心:三种病毒均激活Ⅰ 型干扰素(IFN)信号通路(IFN-α/β、ISG 基因),是宿主的 “基础防御系统”,但激活动力学差异显著:
流感:早期快速爆发(IFI27 24h 达峰),随后迅速回落;
RSV:延迟激活但持续时间长(72h 达峰,恢复期仍高表达);
COVID-19:早期迟钝、后期过度激活,与重症密切相关;
病毒专属机制(最核心发现):
COVID-19:独有的 “凝血 - 内皮损伤 + AP-1/MAPK 持续激活”—— 高 IL-6/CRP、凝血通路(ABO、VWF)、肾素 - 血管紧张素系统(RAAS)紊乱,T 细胞耗竭 / 淋巴细胞减少;
流感:更强的适应性免疫激活——CD4+/CD8+ T 细胞增殖、抗原呈递通路(MHCⅠ/Ⅱ)富集,IFN 信号与 T 细胞激活同步协调;
RSV:中性粒细胞主导的先天炎症 —— 中性粒细胞脱颗粒、NETosis 通路过度激活,T/B 细胞反应薄弱(尤其婴幼儿重症)。
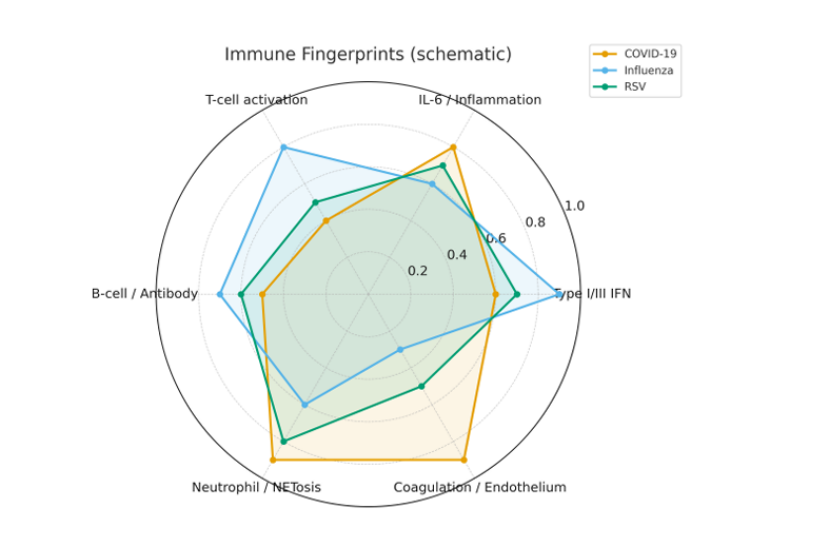
图1
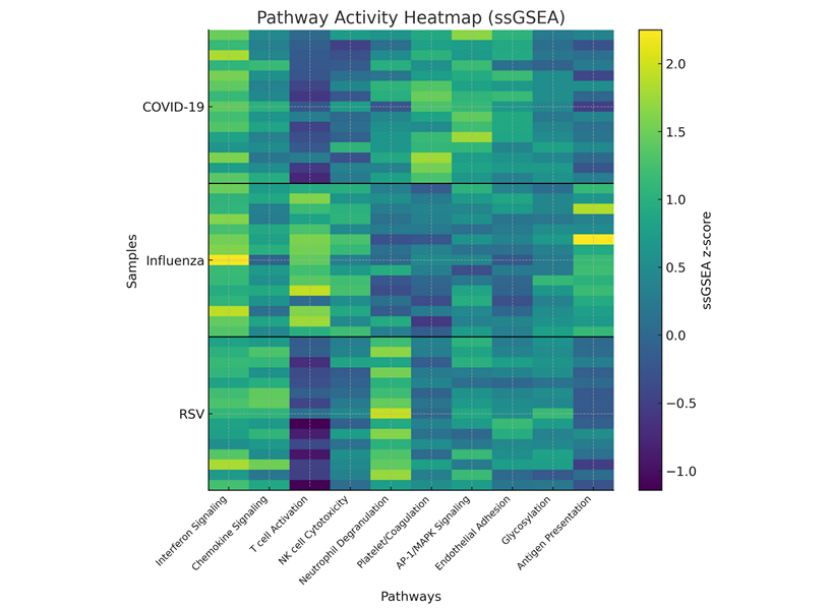
图2
3. 第三步:GWAS 遗传解码:三种病毒的 “易感基因差异”(表 1)
COVID-19 遗传风险:富集 Ⅰ 型干扰素信号(OAS1/2/3、IFNAR2)、IL-6/IL-10 细胞因子通路、凝血 / 内皮功能(ABO);
流感遗传风险:聚焦唾液酸生物合成(ST6GAL1、B3GALT5)—— 编码流感病毒入侵受体(α-2,6 唾液酸),与 COVID-19 遗传重叠极少;
关键差异:仅 ABO 基因在两种病毒中均有涉及,但风险等位基因方向相反(ABO 非 O 型增加 COVID-19 重症风险,却降低流感风险),提示遗传易感性完全不同。
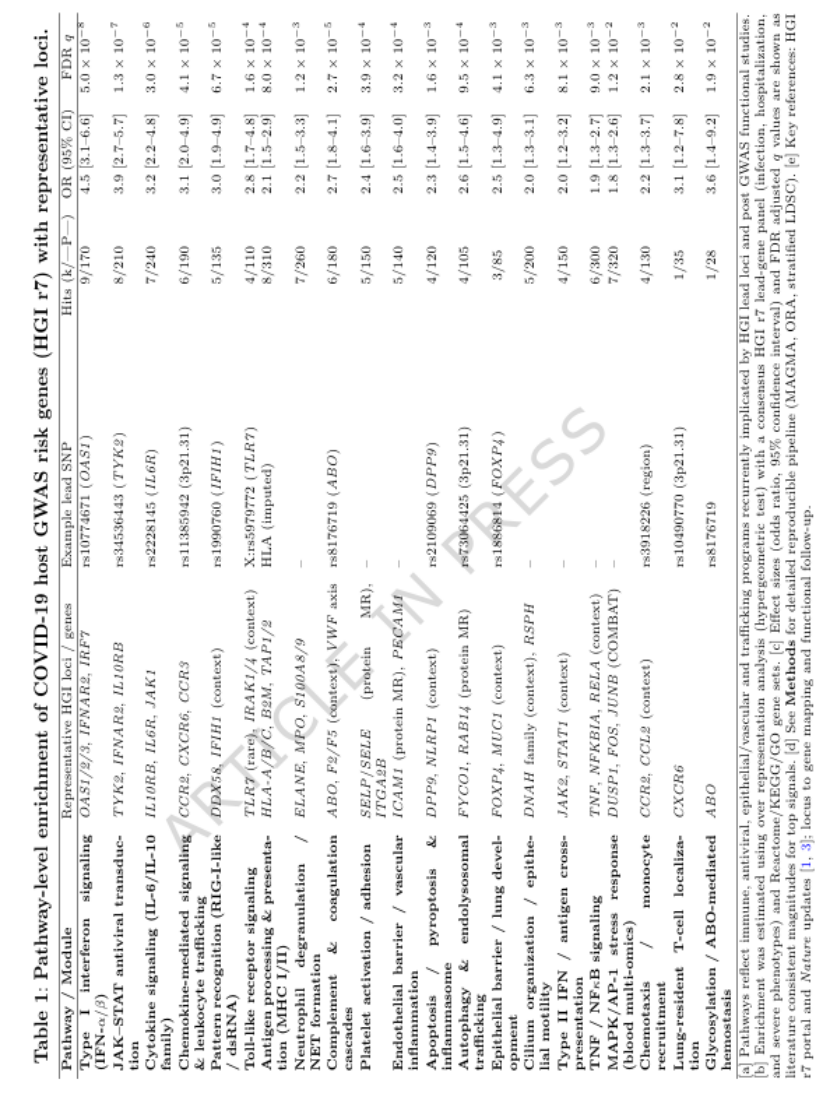
表1
4. 第四步:孟德尔随机化(MR)锁定 6 大因果蛋白(表 2、图 3)
通过蛋白组水平 MR 分析,首次明确驱动 COVID-19 重症的因果蛋白(非相关性):
风险蛋白(OR>1):ABO 血型糖基转移酶(OR=1.15)、RAB14(内体转运,OR=1.20)、CD207(树突状细胞凝集素,OR=1.15)—— 靶向这些蛋白可降低重症风险;
保护蛋白(OR<1):ICAM1(内皮黏附分子,OR=0.85)、SELE(E - 选择素,OR=0.88)、PECAM1(CD31,OR=0.73)—— 增强这些蛋白功能可改善预后;
核心机制:宿主糖基化(ABO、CD207)、内皮功能(ICAM1、SELE)、免疫细胞转运是 COVID-19 重症的关键因果通路。
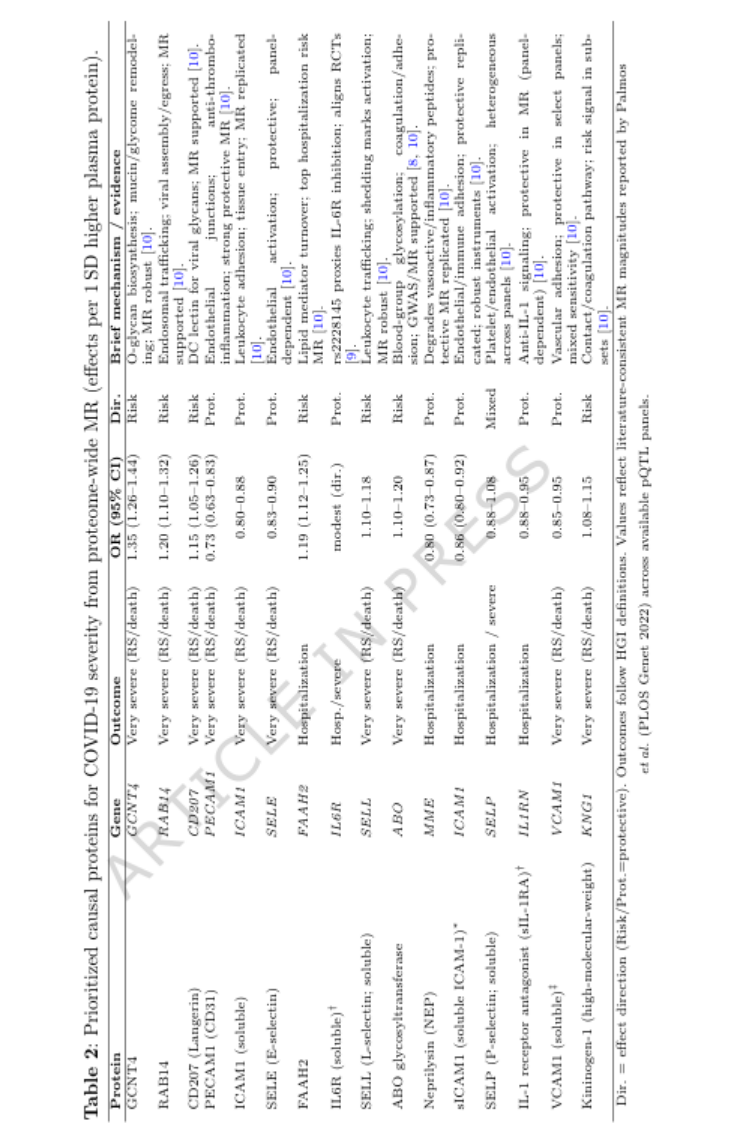
表2
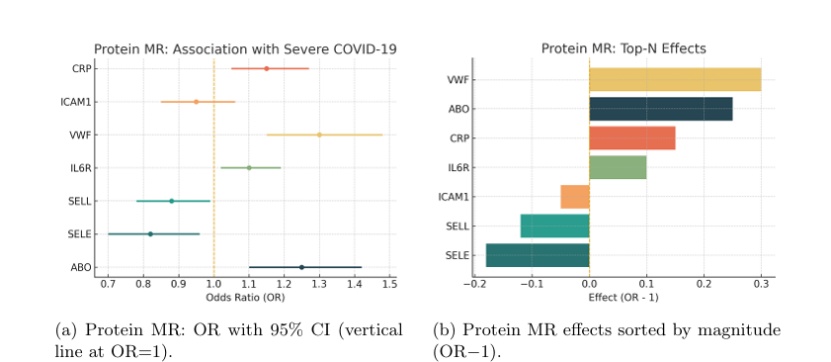
图3
5. 第五步:可解释 AI 揭秘模型决策逻辑(图 4、5)
SHAP 分析量化特征贡献,验证生物学合理性:
指向 COVID-19 的核心特征:IL-6/CRP、AP-1/MAPK 通路、TNF/NF-κB、凝血 / 内皮功能、中性粒细胞比例;
指向流感的核心特征:Ⅰ 型 IFN 反应强度、CD8+ T 细胞计数、淋巴细胞比例;
意义:模型决策完全契合已知免疫机制,证明发现的可靠性,而非数据过拟合。
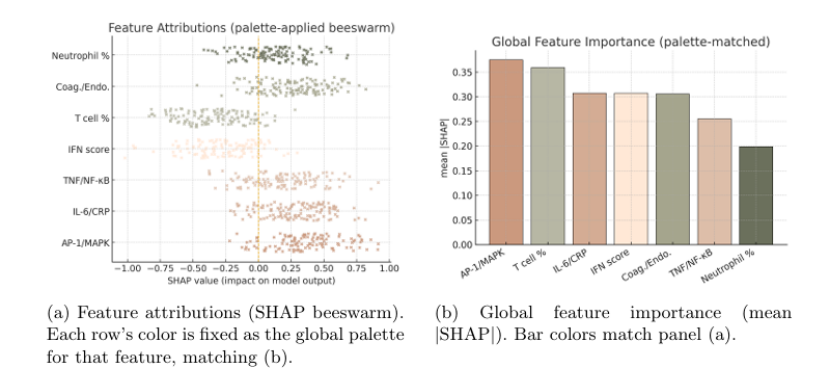
图4
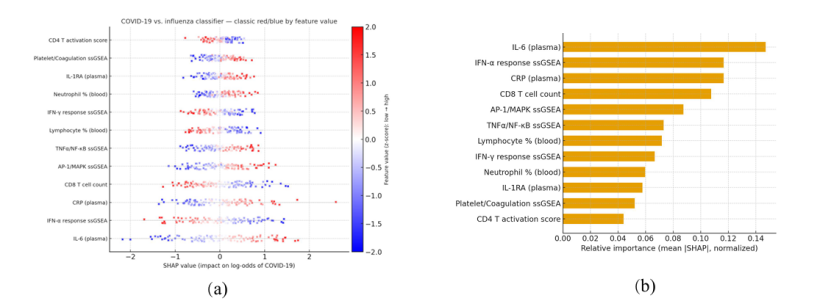
图5
关键结果解读
1. 三种病毒的 “共同防御” 与 “专属攻击套路”
通俗说:面对三种病毒,人体都会启动“干扰素防御系统”,但应对策略不同 —— 流感 “速战速决”(早期强 IFN+T 细胞清毒),RSV “拖延战”(持续中性粒细胞炎症),COVID-19 “乱战”(后期强炎症 + 血栓 + T 细胞失灵);
学术价值:首次在多组学层面证实“IFN 通路为共同核心,下游炎症 / 免疫 / 凝血分化为病毒专属特征”,为广谱抗病毒与靶向治疗提供双重依据。
2. 因果蛋白:COVID-19 重症的 “可靶向靶点”
通俗说:ABO 血型(非 O 型)、RAB14 等是 “坏蛋白”,越高越易重症;ICAM1、E - 选择素是 “好蛋白”,越高越安全,针对性调节这些蛋白可精准降低重症风险;
临床价值:这些蛋白均为可成药靶点(如 IL-6 受体抑制剂已用于临床,ICAM1 激动剂正在研发),直接加速转化研究。
3. AI 模型:快速区分三种病毒的 “临床工具”
通俗说:基于血液多组学特征,AI 能快速判断患者是 COVID-19、流感还是 RSV 感染,尤其重症患者准确率达 88%,解决临床鉴别难题;
落地前景:可整合到临床检验流程,结合常规检测实现快速精准分诊。
研究局限性
RSV 多组学数据相对有限,尤其是成人重症样本,需扩大队列验证;
缺乏疫苗接种后患者的多组学数据,无法评估疫苗对宿主反应的影响;
AI 模型尚未在临床真实世界部署,需进一步优化为快速检测试剂盒;
未探索三种病毒共感染的宿主反应,临床中需关注共感染场景。
总结
这篇 IF=15.1 顶刊研究,通过可解释 AI 整合多组学与遗传数据,首次完整绘制 COVID-19、流感、RSV 的宿主反应全景图,既揭示了 “Ⅰ 型干扰素” 这一共同抗病毒核心,又明确了每种病毒的专属致病机制(COVID-19 的凝血 / AP-1、流感的 T 细胞、RSV 的中性粒细胞),并锁定 6 大因果蛋白靶点。
对临床而言,研究提供了“鉴别诊断标志物 + 精准治疗靶点 + 预后评估工具” 的三重解决方案;对科研而言,“可解释 AI + 多组学 + MR” 的研究范式为复杂疾病机制解析提供了典范。未来,基于这些发现,有望开发出针对单一病毒的靶向药物与覆盖三种病毒的广谱抗病毒策略,彻底改变呼吸道病毒感染的诊疗格局!
原文DOI: 10.1038/s41746-025-02291-w
专注期刊投稿、发表十年,任何投稿、写作难题欢迎咨询!

PAPER INFORMATION

快速预审、投刊前指导、专业学术评审,对文章进行评价

校对编辑、深度润色,让稿 件符合学术规范,格式体例等标准
.png)
适用于语句和结构尚需完善和调整的中文文章,确保稿件达到要求
.png)
数据库包括: 期刊、文书籍、会议、预印章、书、百科全书和摘要等

让作者在期刊选择时避免走弯路,缩短稿件被接收的周期

根据目标期刊格式要求对作者文章进行全面的格式修改和调整
.png)
帮助作者将稿件提交至目标期刊投稿系统,降低退稿或拒稿率
.png)
按照您提供的稿件内容,指导完成投稿附信(cover letter)

北京总部:北京市海淀区碧桐园 3 号楼 2 层 211 广州办事处:广州市黄埔区科学城国际企业孵化器 E栋306 联系人:客服 / 18163670350
Copyright © 2022-2024 北京特诺科技有限公司 版权所有 备案/许可证编号为: 京 ICP 备 2023007944 号