
来源:特诺科研
近日,四川南充川北医学院团队在《International Journal of Surgery》(外科顶刊,IF=10.3,开源零版面费)发表重磅研究,通过孟德尔随机化、单细胞测序、机器学习、多组学验证等多维度技术,证实EB 病毒(EBV)感染与透明细胞肾细胞癌(ccRCC)的因果关联,锁定GBP1 为核心驱动靶点,并发现老药非那雄胺可靶向抑制 GBP1,为ccRCC 精准防治提供新方向。

文章信息速览
原标题:GBP1 as a Machine Learning-Prioritized Biomarker and Therapeutic Target for Epstein-Barr virus-Induced Clear Cell Renal Cell Carcinoma: Multi-Omics Causal Validation(GBP1 作为机器学习优先选择的 EB 病毒诱导透明细胞肾细胞癌生物标志物及治疗靶点:多组学因果验证)
期刊:International Journal of Surgery(IF=10.3,外科顶刊,开源获取)
关键词:EB 病毒、透明细胞肾细胞癌(ccRCC)、多组学分析、孟德尔随机化、机器学习、GBP1、非那雄胺、免疫介导
研究背景与核心痛点
作为肾癌最主要亚型(占70-80%),ccRCC 发病机制复杂,与遗传、环境、病毒感染等多因素相关,但缺乏精准诊断标志物和靶向治疗策略;
EBV 全球感染率超 90%,已证实与淋巴瘤、鼻咽癌等多种癌症相关,但与 ccRCC 的关系一直不明确 —— 是致癌诱因还是肿瘤发生后的伴随感染?传统研究难以区分因果;
单一组学研究说服力不足,缺乏因果推断和临床转化价值,难以满足顶刊发表要求,亟需 "多技术交叉验证+ 临床落地导向" 的研究范式。
研究核心亮点
这篇研究的成功关键的在于 "多技术闭环验证",从因果推断到药物筛选形成完整链条,8 大核心步骤可直接作为多组学论文模板:
1. 第一步:孟德尔随机化 "破局",实锤 EBV 与 ccRCC 因果关系(图 1、2)
技术核心:双向孟德尔随机化(MR)+ 广义汇总数据 MR(GSMR)+ 两步 MR 中介分析
关键结果:
EBV 抗体(EBNA-1/VCA p18)水平升高显著增加 ccRCC 遗传风险(OR=1.23/1.22,P=0.013/0.029),反向 MR 证实无反向因果(图 1A);
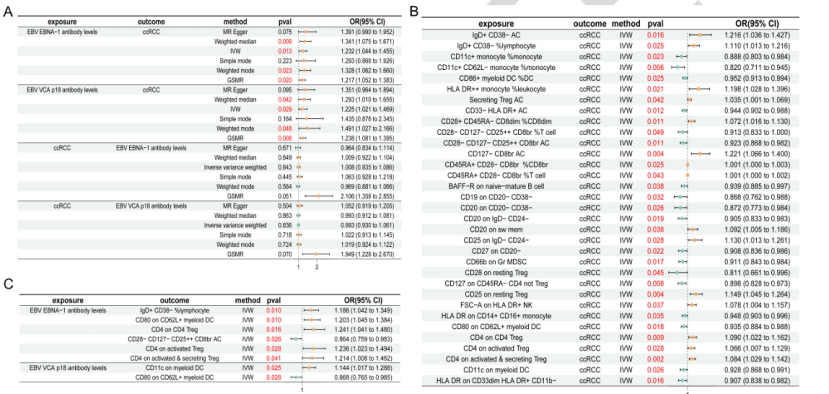
图1
调节性 T 细胞(Treg)和 B 细胞是核心中介因子,其中 CD4+ Treg、IgD+CD38- B 细胞等直接介导 EBV 的促癌效应(图 2A-F);
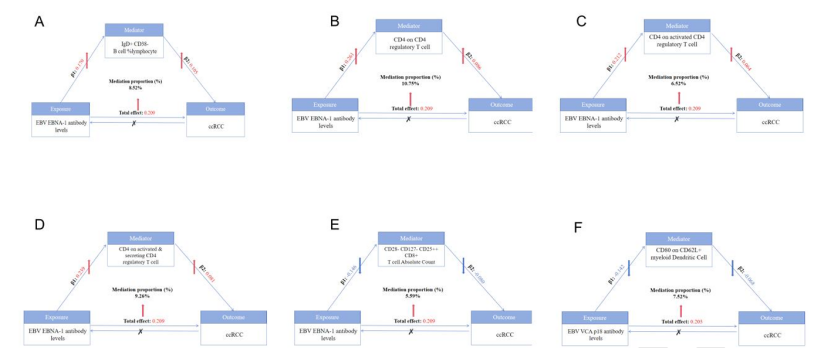
图2
敏感性分析(异质性检验、水平多效性检验、留一法分析)均验证结果可靠,无单 SNP 干扰。
顶刊价值:用遗传证据解决 "谁因谁果" 的经典争议,为后续机制研究奠定 "因果基础",是顶刊青睐的核心设计。
2. 第二步:单细胞测序解析 "免疫互作网络",锁定核心细胞亚群(图 3)
技术核心:scRNA-seq(GSE222703)+ CellChat 细胞通讯分析 + 差异表达分析
关键结果:
肿瘤微环境中,Treg、B 细胞与增殖 T 细胞的通讯强度显著高于正常组织,通讯通路从正常组织的 FN1/ICAM1 等免疫调节通路,变为肿瘤组织的 VEGFA(血管生成)、CDH1(细胞黏附)等促癌通路(图 3G-H);
肿瘤组织中 Treg 上调 959 个基因,B 细胞上调 61 个基因,共筛选出 1013 个肿瘤特异性差异基因(图 3I);
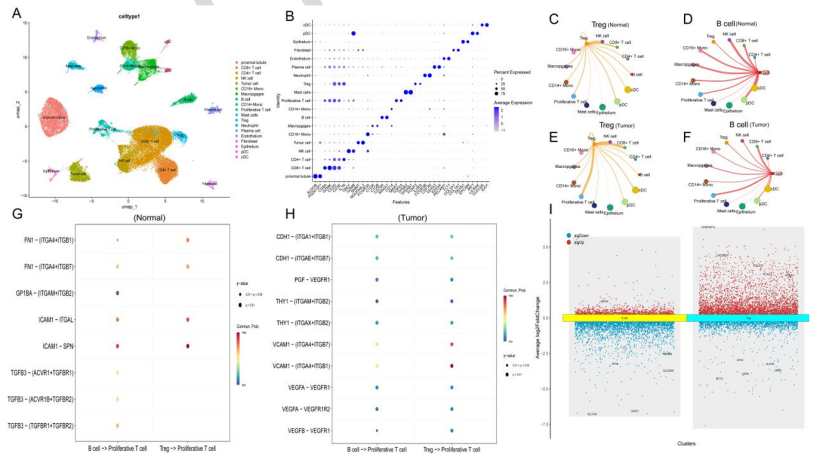
图3
顶刊价值:从 "细胞层面" 拆解 EBV 促癌的具体 "执行者",为后续基因筛选缩小范围。
3. 第三步:WGCNA + 差异分析,筛选 EBV 核心基因(图 4)
技术核心:EBV 感染数据集(GSE45918)差异表达分析 + 加权基因共表达网络分析(WGCNA)
关键结果:
鉴定出 891 个 EBV 感染相关差异基因(471 个上调、420 个下调)(图 4A-B);
WGCNA 筛选出与 EBV 感染最相关的 turquoise 模块(含 8892 个基因),该模块与感染状态高度相关(图 4G);

图4
交集 GeneCard 数据库 EBV 相关基因,得到高置信度 EBV 核心基因集。
顶刊价值:用 "共表达网络" 挖掘 EBV 感染的核心分子集群,避免单一差异基因的偶然性。
4. 第四步:交集分析,建立 "EBV-ccRCC" 分子连接(图 5)
技术核心:EBV 核心基因与 ccRCC 单细胞差异基因交集 + PPI 网络 + 功能富集分析
关键结果:
得到 24 个 Treg/B 细胞共表达基因(6 个上调、18 个下调)(图 5A-B);
这些基因富集于 EBV 感染通路、免疫调节、细胞因子产生等核心生物学过程(图 5D-E),形成紧密的蛋白质相互作用网络(图 5C);
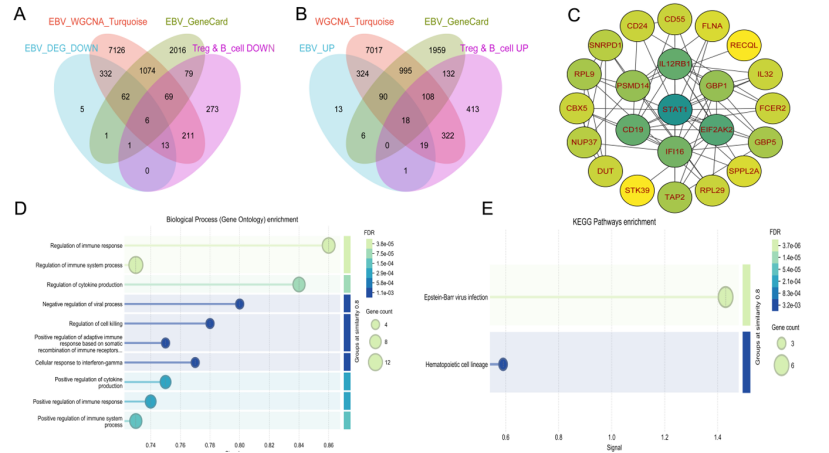
图5
顶刊价值:精准锁定 "EBV 感染→免疫细胞异常→ccRCC 发生" 的关键分子桥梁。
5. 第五步:机器学习 + SHAP,解锁核心靶点 GBP1(图 6)
技术核心:11 种机器学习算法(RF、Ridge、XGBoost 等)+ 堆叠集成学习 + SHAP 可解释性分析
关键结果:
构建 107 个预测模型,RF+Ridge 集成模型表现最优(AUC=0.973),筛选出 7 个关键诊断基因(GBP1、IFI16、RECQL 等)(图 6A-B);
SHAP 分析显示 GBP1 的贡献值最高(SHAP=0.191),是促进 ccRCC 发生的主要正向调控因子(图 6C-F);
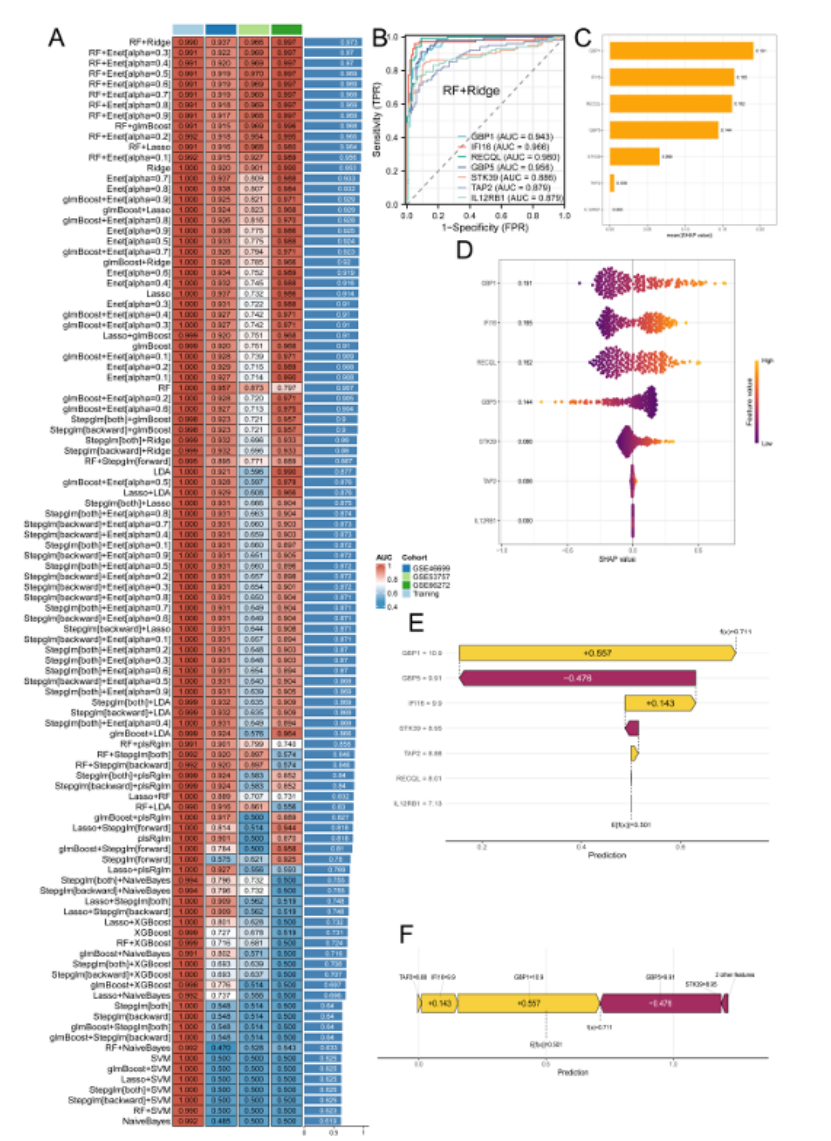
图6
顶刊价值:用 "多算法验证 + 可解释性分析" 解决机器学习 "黑箱" 问题,让核心靶点的筛选更具说服力。
6. 第六步:多组学因果验证,夯实 GBP1 驱动地位(图7)
技术核心:mQTL/eQTL/pQTL 多组学 MR + 汇总数据 MR(SMR)+ 贝叶斯共定位
关键结果:
GBP1 在甲基化(mQTL)、转录(eQTL)、蛋白质(pQTL)层面均与 ccRCC 存在显著因果关联(OR=0.4187-4.8557,P<0.001)(图 7A);
共定位分析显示 PP.H4>0.80,证实 GBP1 与 ccRCC 共享同一因果遗传变异,排除多效性干扰(图 7B-J);
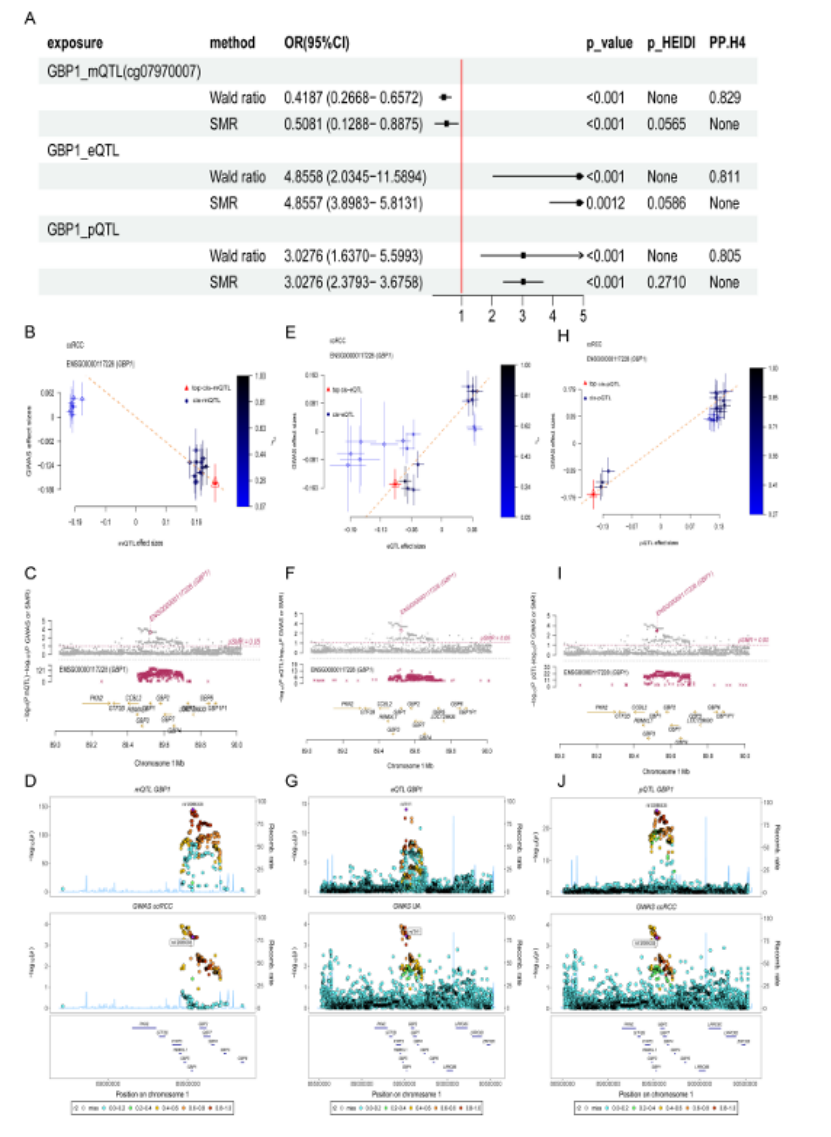
图7
顶刊价值:从 "基因组→转录组→蛋白质组" 多层面验证因果关系,满足顶刊 "多维度交叉验证" 的要求。
7. 第七步:多数据集验证,GBP1 成可靠诊断标志物(图 8、9)
技术核心:scRNA-seq、bulk RNA-seq(4 个队列)、CPTAC 蛋白质组、HPA 免疫组化(IHC)
关键结果:
GBP1 在 ccRCC 肿瘤组织(尤其 Treg 细胞)中显著高表达,4 个 RNA-seq 队列的诊断 AUC 均 > 0.85(图 8B-F);
蛋白质组数据证实 GBP1 在肿瘤组织中蛋白水平显著升高(图 8G-H);
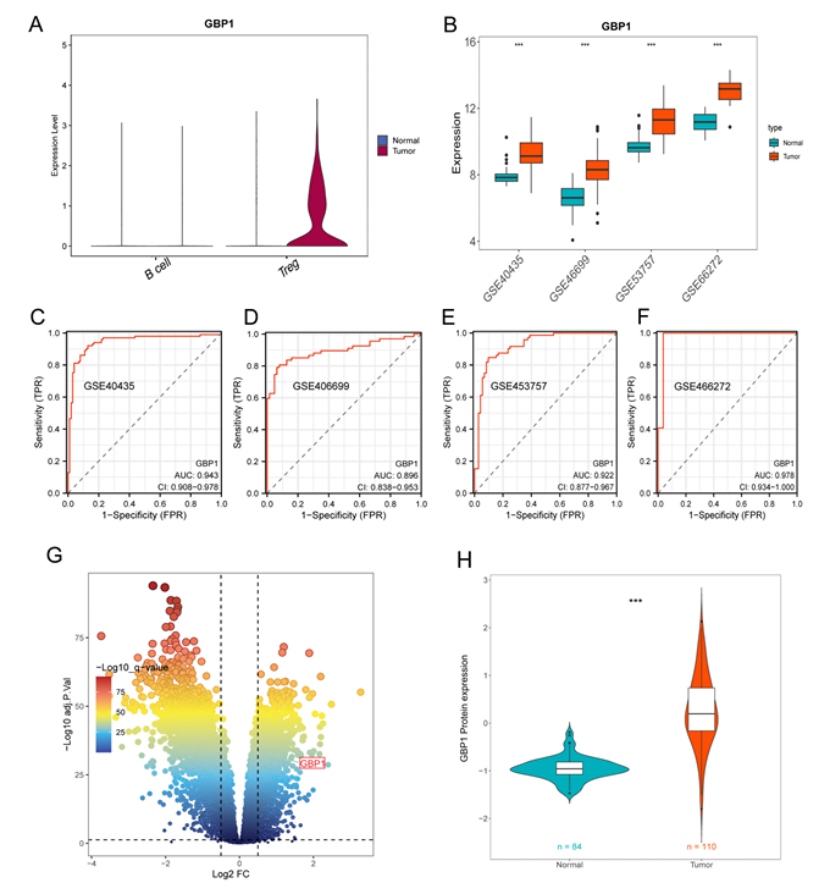
图8
IHC 显示正常肾组织几乎无 GBP1 表达,而肿瘤组织呈中高强度染色(图 9);
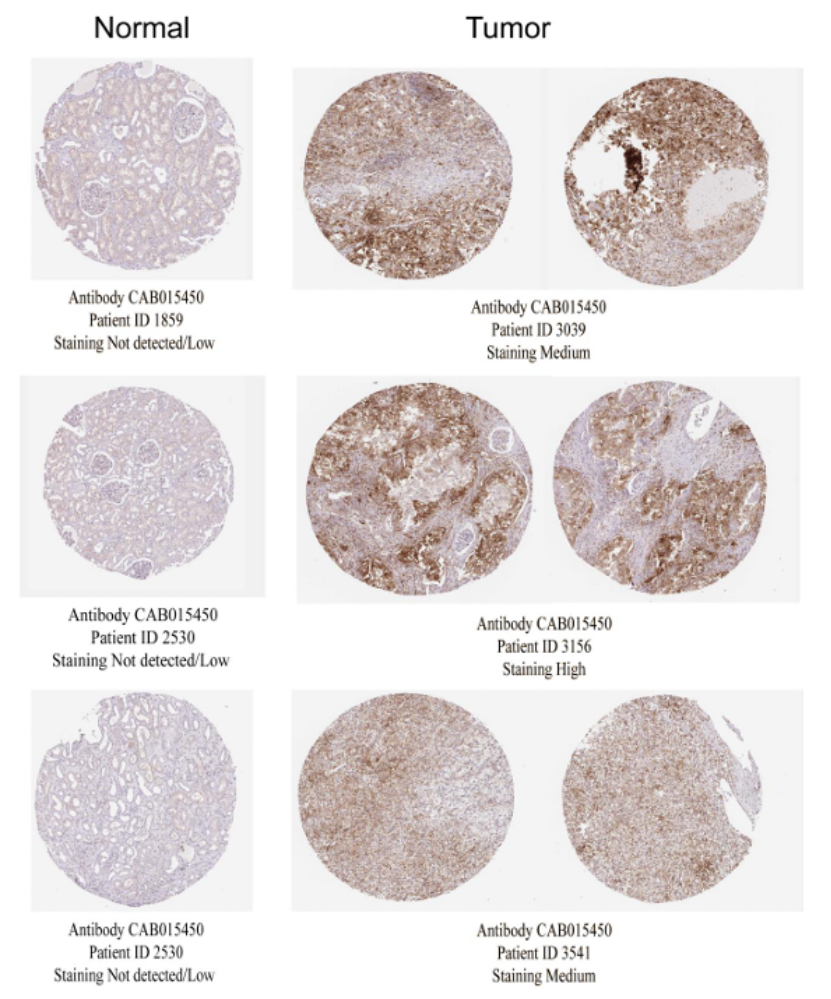
图9
顶刊价值:从 "转录→蛋白→组织形态" 全维度验证,让核心靶点的临床应用价值更扎实。
8.第八步:药物预测 + 分子对接,实现临床转化(图 10)
技术核心:DGIdb 药物 - 基因相互作用数据库 + AutoDock Vina 分子对接
关键结果:
筛选出唯一临床获批的 GBP1 抑制剂 —— 非那雄胺(原用于前列腺增生治疗);
分子对接显示非那雄胺与 GBP1 结合能达 - 7.6 kcal/mol,结合构象稳定,具备良好抑制潜力(图 10);
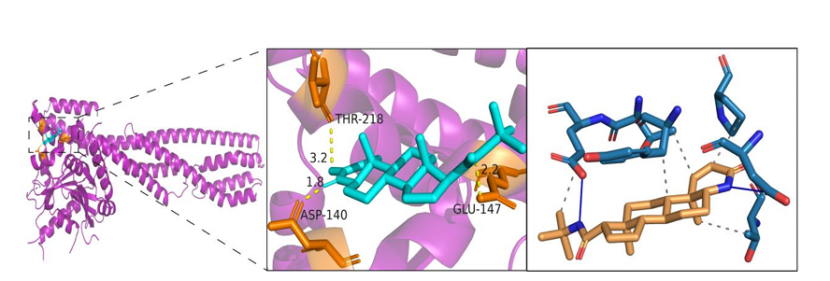
图10
将基础研究与临床药物直接关联,降低转化门槛,显著提升论文的临床意义和顶刊竞争力。
医生发文角度:
因果推断先行:用孟德尔随机化解决传统多组学研究 "混杂偏倚" 的痛点,先明确 "谁因谁果",再深入机制,让结论更具说服力;
多技术深度整合:不是简单堆砌技术,而是形成 "MR 因果验证→单细胞找细胞亚群→WGCNA 筛基因→机器学习锁靶点→多组学验证→药物筛选" 的完整闭环,每个步骤都为下一步服务;
临床转化导向:研究终点不只是找到靶点,而是关联已获批药物,给出明确的临床应用方向(诊断标志物 + 靶向药物),满足顶刊对 "临床价值" 的核心要求;
可视化赋能:每个关键结果都搭配高质量图表(UMAP 图、ROC 曲线、分子对接图、IHC 染色图),让复杂数据更易理解,提升论文可读性。
临床与科研价值
诊断层面:GBP1 可作为 EBV 相关ccRCC 的早期诊断标志物(AUC>0.85),为肾癌早筛提供新工具;
治疗层面:非那雄胺可作为潜在靶向治疗药物,为 ccRCC 提供 "老药新用" 的治疗方案,尤其适用于 EBV 抗体水平升高的高危人群;
预防层面:EBV 抗体(EBNA-1/VCA p18)可作为 ccRCC 风险筛查指标,高危人群可早期干预;
科研层面:提供 "病毒 - 免疫 - 肿瘤" 的多组学研究范式,为其他病毒相关癌症(如 EBV 相关胃癌、淋巴瘤)的研究提供参考。
四川南充川北医学院团队的这篇研究,完美诠释了顶刊多组学论文的核心设计逻辑:以临床疑问(EBV 与 ccRCC 的关系)为起点,用因果推断建立核心关联,用多技术整合精准定位靶点,最终落地到临床可用的诊断工具和治疗药物。对于医生和科研人员来说,这套 "从临床中来,到临床中去" 的研究思路,不仅能大幅提高顶刊命中率,还能让研究真正服务于临床实践。
原文DOI: 10.1097/JS9.0000000000004393
专注期刊投稿、发表十年,任何投稿、写作难题欢迎咨询!

PAPER INFORMATION

快速预审、投刊前指导、专业学术评审,对文章进行评价

校对编辑、深度润色,让稿 件符合学术规范,格式体例等标准
.png)
适用于语句和结构尚需完善和调整的中文文章,确保稿件达到要求
.png)
数据库包括: 期刊、文书籍、会议、预印章、书、百科全书和摘要等

让作者在期刊选择时避免走弯路,缩短稿件被接收的周期

根据目标期刊格式要求对作者文章进行全面的格式修改和调整
.png)
帮助作者将稿件提交至目标期刊投稿系统,降低退稿或拒稿率
.png)
按照您提供的稿件内容,指导完成投稿附信(cover letter)

北京总部:北京市海淀区碧桐园 3 号楼 2 层 211 广州办事处:广州市黄埔区科学城国际企业孵化器 E栋306 联系人:客服 / 18163670350
Copyright © 2022-2024 北京特诺科技有限公司 版权所有 备案/许可证编号为: 京 ICP 备 2023007944 号