
来源:特诺科研
前列腺癌(PCa)是全球男性第二高发恶性肿瘤,转移是导致患者死亡的首要原因,临床缺乏可靠的无创转移预警标志物,且表观遗传与代谢重编程在转移中的交叉调控机制尚未明确。近日,南京大学医学院附属鼓楼医院团队在《Cellular & Molecular Biology Letters》(IF=10.2,肿瘤领域优质期刊,开源获取)发表重磅研究,整合单细胞测序、bulk转录组、甲基化组多组学技术,结合体内外实验、临床样本验证,首次完整揭示“AZGP1启动子甲基化→基因沉默→糖酵解激活→前列腺癌转移”的调控链条,关键结果均有明确图表支撑,为前列腺癌转移的动态监测、预后评估及靶向治疗提供可直接转化的方案。

文章信息速览
原标题:Methylation-induced silencing of AZGP1 enhances prostate cancer metastasis by stimulating tumoral glycolysis
期刊:Cellular & Molecular Biology Letters(IF=10.2,肿瘤领域优质期刊,开源获取,Brief Report类型)
关键词:前列腺癌、AZGP1、DNA甲基化、糖酵解、肿瘤转移、分子标志物、表观遗传、代谢重编程
研究核心亮点
这篇IF=10.2顶刊论文的成功,核心在于“多组学整合+多维度验证”的经典发文范式,从“筛选→验证→机制→转化”形成完整闭环,完全可作为医生发多组学论文的参考模板,5大核心步骤+原文图表,清晰易懂、可复刻:
第一步:单细胞+bulk多组学联合,锁定转移相关核心基因AZGP1(图1) 研究团队先对GSE141445单细胞数据集(36424个细胞)进行预处理、细胞注释,通过Scissor工具结合bulk转录组数据(TCGA-PRAD),精准鉴定出具有转移优势的肿瘤细胞亚群(Met亚群)(图1A); 通过差异表达分析,筛选出9个转移相关候选基因,经TCGA-PRAD队列验证,最终锁定6个核心转移相关基因(MRGs),其中AZGP1与肿瘤转移呈显著负相关(图1B、C); 进一步通过单变量、多变量逻辑回归分析,建立前列腺癌转移预测模型,AUC值超70%,证实AZGP1是前列腺癌转移的独立保护因子(图1E、F); 另一个独立单细胞数据集(Tuong et al.)验证显示,Met亚群中AZGP1表达显著低于非Met亚群(P=2.289×10⁻⁷),进一步确认AZGP1的核心作用。
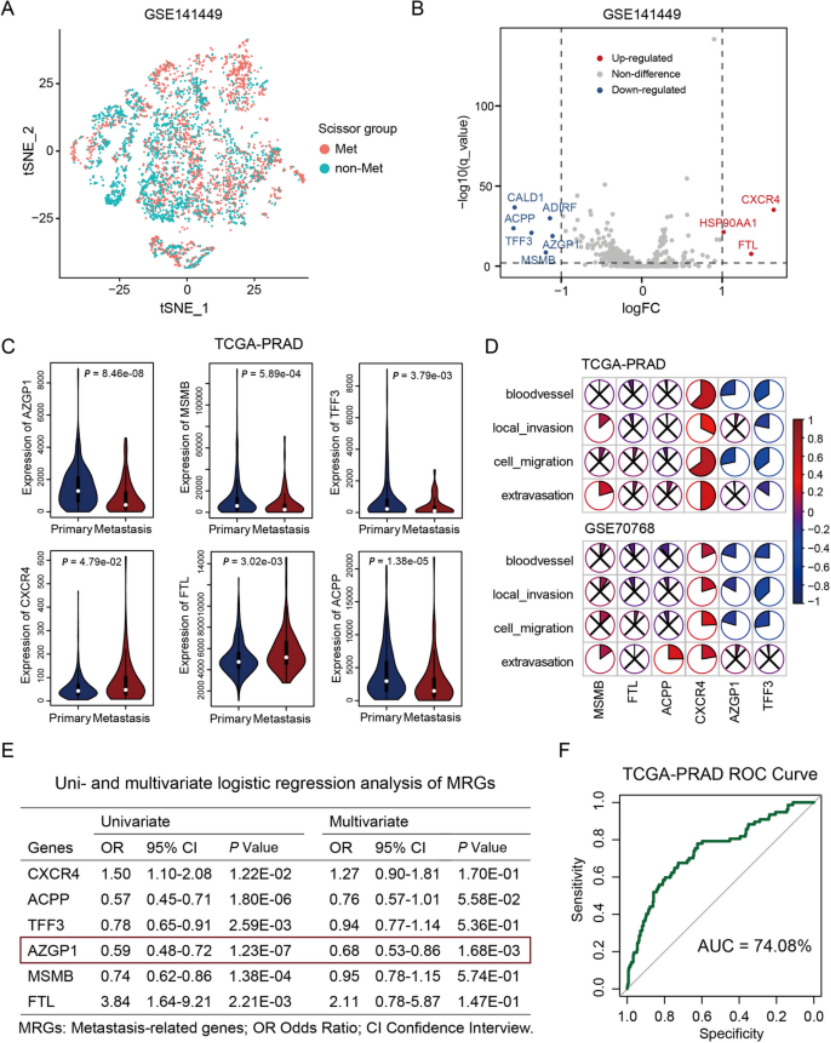
图1 转移亚群鉴定及转移预测模型建立(A:TSNE图展示Met/非Met细胞亚群;B:差异表达分析火山图;C:6个核心MRGs在转移与非转移样本中的表达小提琴图;D:MRGs与转移相关通路的相关性饼图;E:单/多变量逻辑回归分析图;F:转移预测模型AUC图)
第二步:多队列+临床样本验证,AZGP1低表达与前列腺癌进展、不良预后密切相关(图2) 多中心队列(TCGA-PRAD、GSE21034、DKFZ2018)验证显示,AZGP1低表达与前列腺癌高T分期、N1淋巴结转移、高Gleason评分显著相关(P均<0.05)(图2A、B、C); 生存分析显示,AZGP1低表达患者无进展生存期(PFS)显著缩短,9个bulk数据集的meta分析进一步证实AZGP1与患者预后的关联(图2D); 体内实验(裸鼠尾静脉注射、胫骨注射模型)显示,过表达AZGP1可显著降低肺转移、骨转移的荧光强度(P=0.0017、P=0.0217)(图2E); 40例临床FFPE样本免疫组化证实,转移组AZGP1的H-score显著低于非转移组(P=0.0002),明确AZGP1的临床应用价值(图2F、G)。
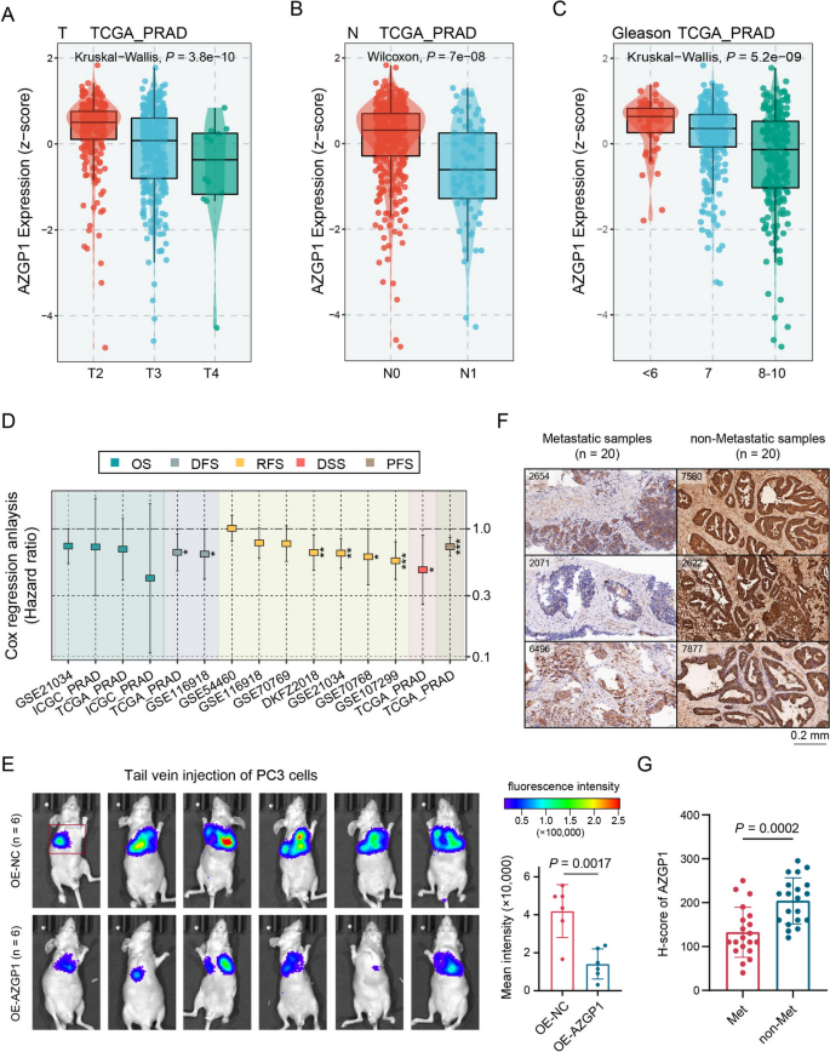
图2 AZGP1表达与前列腺癌进展及预后的关联(A:不同T分期AZGP1表达箱线图;B:N0/N1期AZGP1表达箱线图;C:不同Gleason评分AZGP1表达箱线图;D:AZGP1与患者预后的meta分析森林图;E:体内转移模型荧光成像及定量分析;F:转移与非转移样本AZGP1免疫组化染色图;G:两组样本H-score散点图)
第三步:体内外功能实验,直接验证AZGP1沉默促进前列腺癌转移(图3) 细胞系验证:CCLE数据库及RT-qPCR检测显示,转移性去势抵抗性前列腺癌细胞(PC3、DU145)中AZGP1表达最低,原发性细胞(22RV1、LNCaP)中表达最高(图3A、B); 功能验证:构建AZGP1敲低(22RV1细胞)和过表达(PC3细胞)模型,Transwell实验显示,AZGP1敲低显著增强细胞迁移、侵袭能力,过表达则显著抑制(图3D、E); 伤口愈合实验进一步证实,AZGP1表达与细胞迁移能力呈负相关(P均<0.05)(图3F、G); 蛋白水平验证:Western blot显示,AZGP1敲低可上调N-钙粘蛋白、VEGFA、MMP7等转移相关蛋白表达,下调E-钙粘蛋白表达,过表达则呈相反趋势(图3H)。
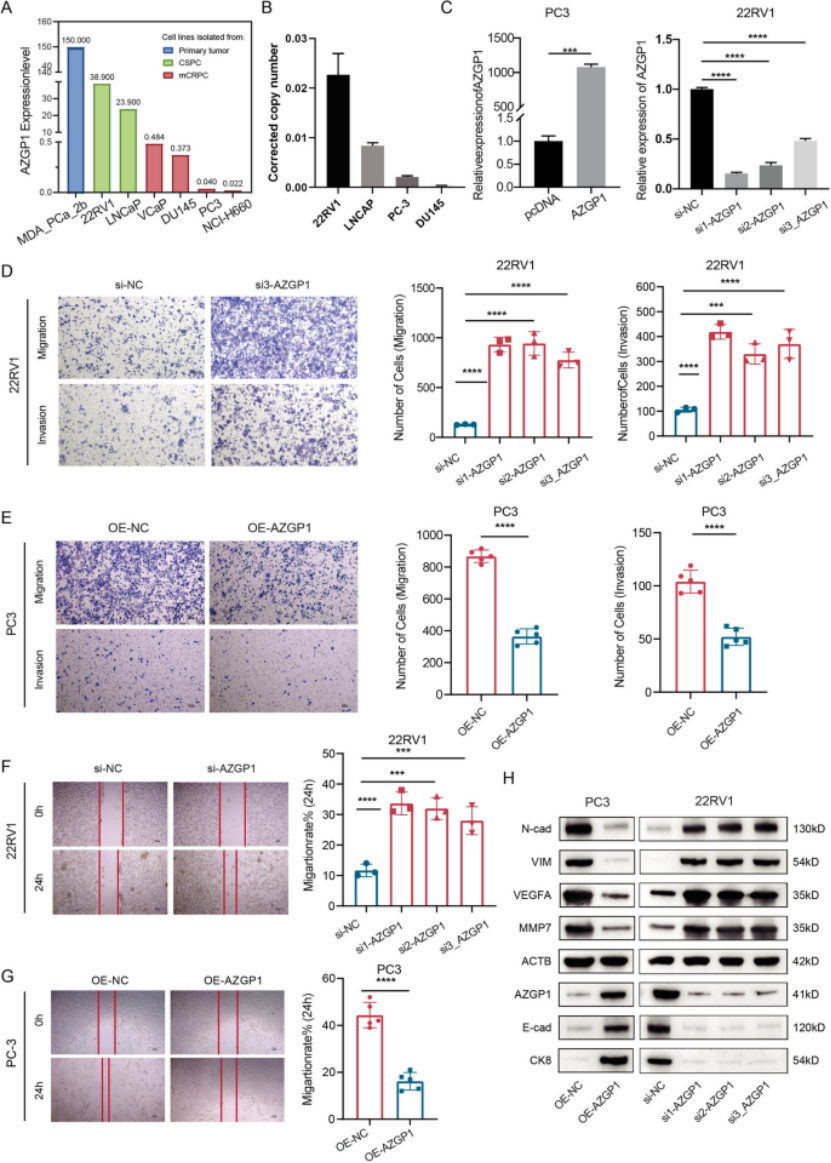
图3 AZGP1对前列腺癌细胞转移表型的调控(A:CCLE数据库中不同前列腺癌细胞系AZGP1表达;B:4种细胞系AZGP1表达RT-qPCR验证;C:AZGP1过表达/敲低效率验证;D:22RV1细胞敲低AZGP1后的Transwell实验;E:PC3细胞过表达AZGP1后的Transwell实验;F、G:伤口愈合实验及定量分析;H:转移相关蛋白Western blot结果)
第四步:代谢机制深挖,AZGP1沉默通过激活糖酵解驱动转移(图4) 单细胞代谢分析显示,AZGP1阴性腔面肿瘤细胞的糖酵解通路显著活化(图4A); TCGA-PRAD队列分析表明,AZGP1表达与糖酵解通路ssGSEA评分呈显著负相关(R=-0.1,P=0.03),与LDHA、PFKFB3、SLC2A1等关键糖酵解酶也呈显著负相关(R=-0.09~-0.23,P均<0.05)(图4B、C、D); 功能检测:PC3细胞过表达AZGP1后,乳酸生成量、ECAR(糖酵解速率)显著降低,OCR(线粒体呼吸速率)升高;22RV1细胞敲低AZGP1后则呈相反趋势,明确AZGP1通过抑制糖酵解阻断转移(图4E-J)。
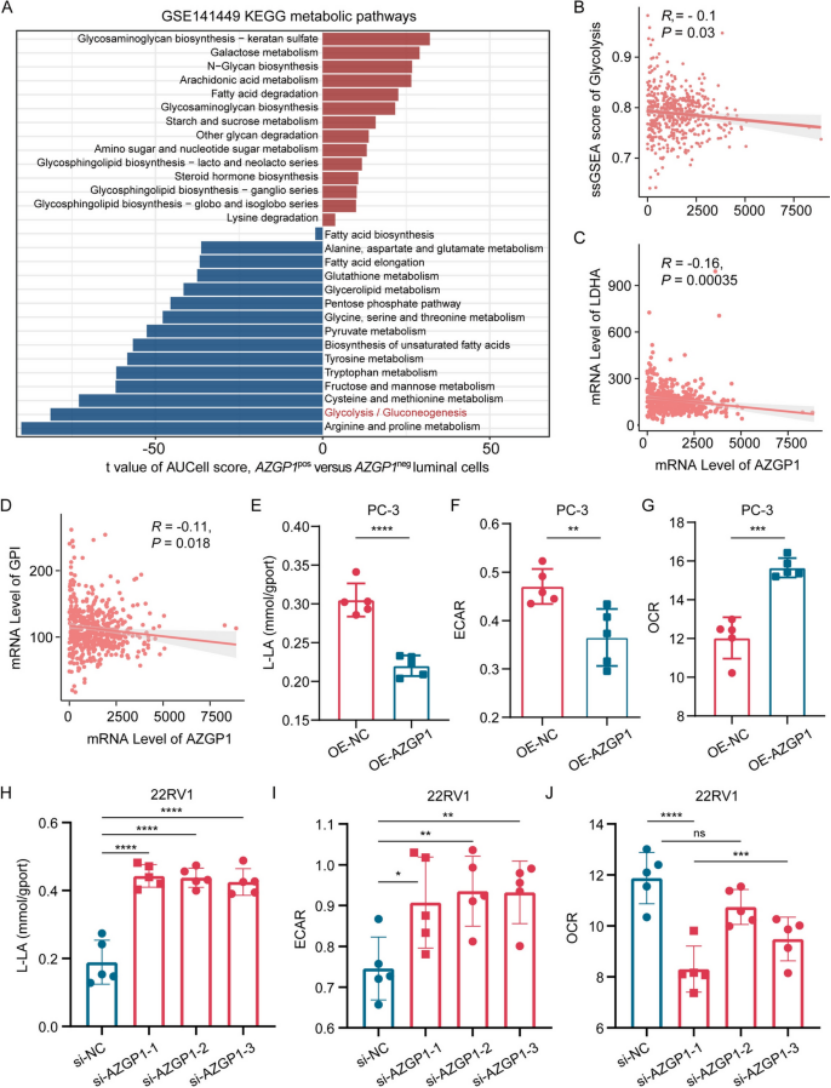
图4 AZGP1对前列腺癌细胞糖酵解的调控(A:AZGP1阳性/阴性细胞代谢通路富集差异;B:AZGP1表达与糖酵解通路ssGSEA评分相关性;C、D:AZGP1与LDHA、GP1的表达相关性;E-G:PC3细胞过表达AZGP1后乳酸、ECAR、OCR检测结果;H-J:22RV1细胞敲低AZGP1后乳酸、ECAR、OCR检测结果)
第五步:多组学揭秘调控源头,AZGP1启动子甲基化是其沉默的核心诱因(图5) 甲基化分析:TCGA甲基化与mRNA数据显示,AZGP1启动子cg26429636位点甲基化与基因表达呈强负相关,且淋巴结转移(N1)患者该位点甲基化水平显著高于非转移(N0)患者(P=0.049)(图5A、B); 甲基转移酶关联:AZGP1表达与DNMT1、DNMT3A、DNMT3B三种甲基转移酶表达呈显著负相关(R=-0.3~-0.44,P均<0.001),且cg26429636位点甲基化水平与这三种甲基转移酶表达呈正相关(图5D-L); MSP验证:甲基化特异性PCR显示,AZGP1高表达的22RV1、LNCaP细胞(原发性)中,cg26429636位点呈未甲基化状态;AZGP1低表达的PC3、DU145细胞(转移性)中呈高甲基化状态,证实甲基化是AZGP1沉默的关键原因(图5M)。
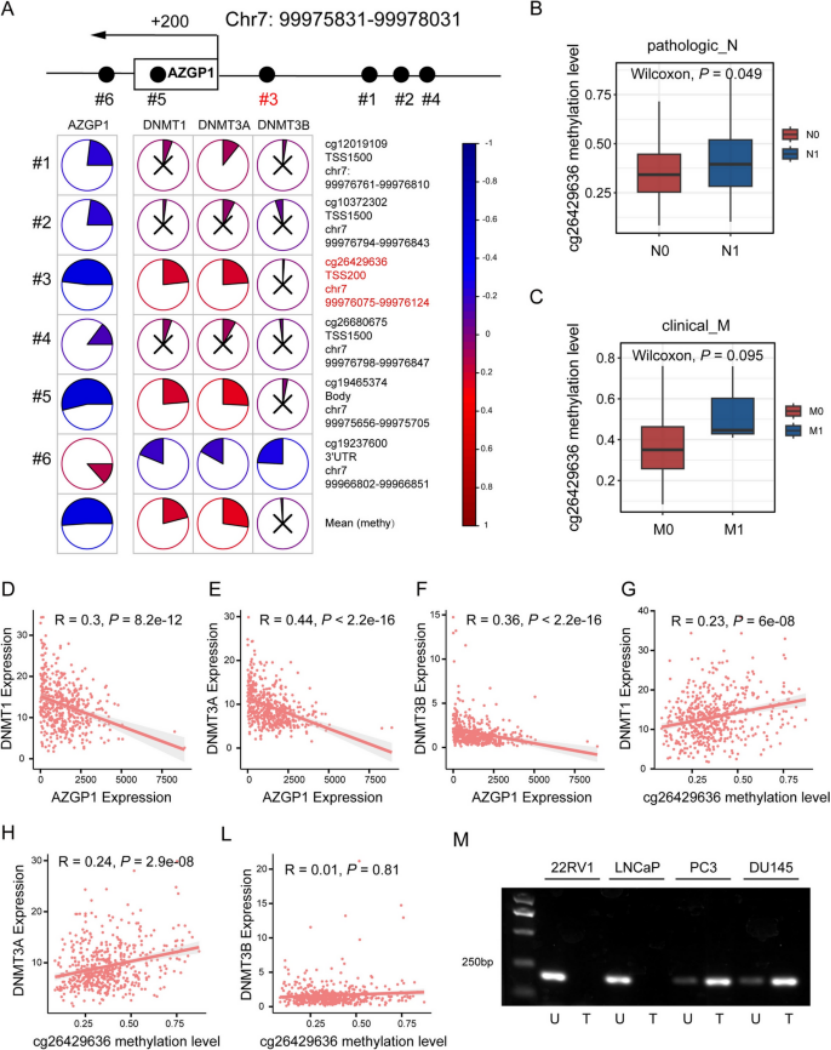
图5 AZGP1启动子甲基化的调控作用(A:AZGP1甲基化-表达调控模型及相关性;B:N0/N1期cg26429636位点甲基化水平箱线图;C:M0/M1期cg26429636位点甲基化水平箱线图;D-F:AZGP1与DNMT1、DNMT3A、DNMT3B的表达相关性;G-L:cg26429636甲基化水平与三种甲基转移酶的表达相关性;M:4种细胞系AZGP1启动子MSP检测结果)
总结:多组学发文模板级研究,为前列腺癌转移诊疗+医生发文双重赋能
南京大学医学院附属鼓楼医院团队的这项研究,完美契合中高分期刊“临床痛点→多组学筛选→机制解析→多维度验证→临床转化”的发文逻辑,仅用“单细胞+bulk转录组+甲基化组”三种多组学技术,结合常规体内外实验、临床样本,就成功拿下IF=10.2的顶刊,且开源0版面费,极大降低了医生发文成本。
研究不仅阐明了AZGP1甲基化通过激活糖酵解驱动前列腺癌转移的核心机制,提供了可临床转化的新型分子标志物(cg26429636位点甲基化)与干预靶点,更给想发多组学论文的医生提供了可直接复刻的范式:无需复杂的多组学组合,聚焦一个核心靶点,用“多组学筛选+多队列验证+体内外功能+机制深挖”的思路,即可高效产出中高分成果。
原文DOI:10.1186/s11658-025-00818-3
专注期刊投稿、发表十年,任何投稿、写作难题欢迎咨询!

PAPER INFORMATION

快速预审、投刊前指导、专业学术评审,对文章进行评价

校对编辑、深度润色,让稿 件符合学术规范,格式体例等标准
.png)
适用于语句和结构尚需完善和调整的中文文章,确保稿件达到要求
.png)
数据库包括: 期刊、文书籍、会议、预印章、书、百科全书和摘要等

让作者在期刊选择时避免走弯路,缩短稿件被接收的周期

根据目标期刊格式要求对作者文章进行全面的格式修改和调整
.png)
帮助作者将稿件提交至目标期刊投稿系统,降低退稿或拒稿率
.png)
按照您提供的稿件内容,指导完成投稿附信(cover letter)

北京总部:北京市海淀区碧桐园 3 号楼 2 层 211 广州办事处:广州市黄埔区科学城国际企业孵化器 E栋306 联系人:客服 / 18163670350
Copyright © 2022-2024 北京特诺科技有限公司 版权所有 备案/许可证编号为: 京 ICP 备 2023007944 号