
来源:特诺科研
骨生物材料植入后的先天免疫应答是调控成骨的核心,而金属植入体的骨整合效果直接决定骨科、牙科植入手术的成败,临床中亟需明确免疫细胞互作调控骨整合的分子机制,为优化植入材料、提升成骨效果提供新靶点。
近日,浙江大学团队在《Materials Today Bio》(IF=10.2,材料领域)发表重磅研究:通过转录组、蛋白质组多组学分析 + 单细胞 RNA 测序,结合体内外实验验证、条件性敲除小鼠模型及药理学干预,首次揭示 E3 泛素连接酶 TRIM30a 通过抑制 NF-κB/NLRP3 通路调控中性粒细胞 NETosis,同时校准巨噬细胞 cGAS-STING 信号的双重机制,证实 DNase I 靶向降解 dsDNA 可挽救 TRIM30a 缺陷小鼠的成骨能力,为植入体骨整合的免疫调控提供全新靶点和治疗策略!

文章信息速览
原标题:TRIM30a coordinates neutrophil-macrophage crosstalk to resolve inflammation and drive osseointegration via suppressing NETosis/cGAS-STING axis
期刊:Materials Today Bio(IF=10.2)
关键词:植入体、骨整合、中性粒细胞胞外陷阱、TRIM30a、NF-κB/NLRP3 通路、cGAS-STING 信号、中性粒细胞、巨噬细胞、DNase I、金属生物材料
研究背景与临床痛点
临床困境:骨科、牙科金属植入体的临床效果由宿主免疫应答决定,非成骨型植入体易引发过度异物反应,导致骨整合失败,目前缺乏调控植入体周围免疫微环境的有效靶点;
机制盲区:中性粒细胞和巨噬细胞是植入体免疫应答的核心细胞,但其互作调控骨整合的分子机制尚未明确,NETosis 及下游 cGAS-STING 信号在骨整合中的作用亟待解析;
技术缺口:单一组学技术难以全面解析植入体 - 免疫 - 成骨的调控网络,亟需多组学联合单细胞测序技术,挖掘骨整合的关键调控因子;
治疗短板:临床中仅通过优化植入材料理化性质提升成骨效果,未从免疫调控角度开发靶向干预手段,缺乏精准提升骨整合的药理学方案。
研究核心亮点
这篇顶刊研究的成功关键在于“多组学筛分子 + 单细胞定细胞 + 体内外验机制 + 药理学证临床” 的经典研究逻辑,完美契合材料与骨科学领域顶刊发文体例,关键图表层层递进支撑核心结论,为临床医生发多组学顶刊论文提供了可复刻的范本:
第一步:多组学联合筛选,锁定 TRIM30a 为骨整合关键调控因子(图 1)
成骨表型验证:构建 4 种成骨能力梯度的金属植入体(SR>SLA>PT>SS),Masson 染色证实 SR 成骨能力最强,SS 最弱(图 1A-B);
多组学分析:对植入体周围骨组织进行转录组(bulk RNA-seq)+ 蛋白质组(TMT) 多组学检测,发现 TRIM30a 是差异表达核心蛋白,其表达量与植入体成骨能力呈正相关(图 1D-E);
体内验证:免疫组化证实植入体周围 TRIM30a 阳性细胞数随成骨能力增强而升高(图 1F-G),相关性分析显示 TRIM30a 表达与新骨形成面积显著正相关(图 1H);
基因敲除验证:TRIM30a 全身敲除(KO)小鼠植入体周围骨体积、骨小梁厚度等成骨指标显著低于野生型(WT)小鼠(图 1I-L),Masson 染色证实 KO 小鼠新骨形成显著减少(图 1M-N),明确 TRIM30a 是骨整合的正调控因子。
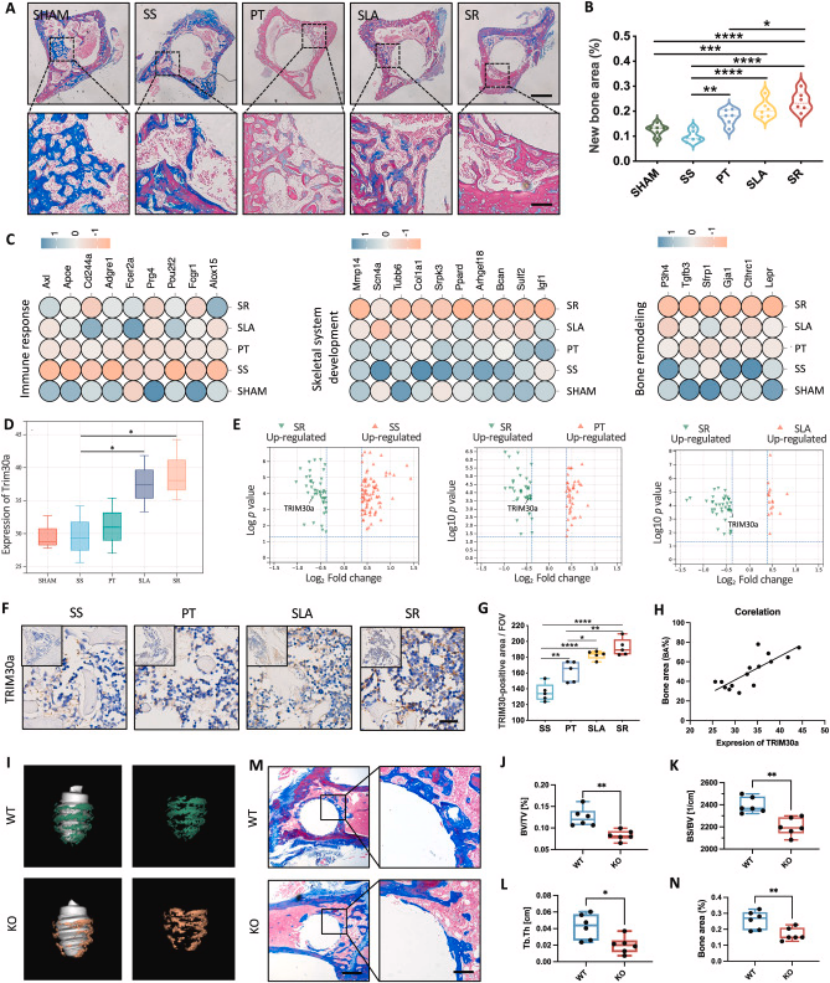
图1
第二步:单细胞测序定位,确定 TRIM30a 的功能细胞为中性粒细胞和巨噬细胞(图 2)
单细胞图谱构建:对植入体周围组织进行单细胞 RNA-seq,获得 35704 个细胞并分群为 10 类,发现 TRIM30a 表达几乎仅限于中性粒细胞和巨噬细胞,在成骨细胞、造血干祖细胞中无显著表达(图 2A-B);
条件性敲除验证:构建中性粒细胞特异性 TRIM30a 敲除小鼠(N-CKO)和巨噬细胞特异性敲除小鼠(M-CKO),微 - CT 证实两种条件性敲除小鼠植入体周围成骨指标均显著降低(图 2C-F、I-L),组织染色证实新骨形成减少(图 2G-H、M-N),明确中性粒细胞和巨噬细胞是 TRIM30a 调控骨整合的功能细胞;
材料调控验证:单细胞测序及体外蛋白实验证实,成骨型植入体(SR/SLA)可显著上调中性粒细胞和巨噬细胞中 TRIM30a 的表达,非成骨型植入体(SS)则显著抑制其表达(图 2O-X),明确植入材料通过调控免疫细胞中 TRIM30a 表达影响成骨。
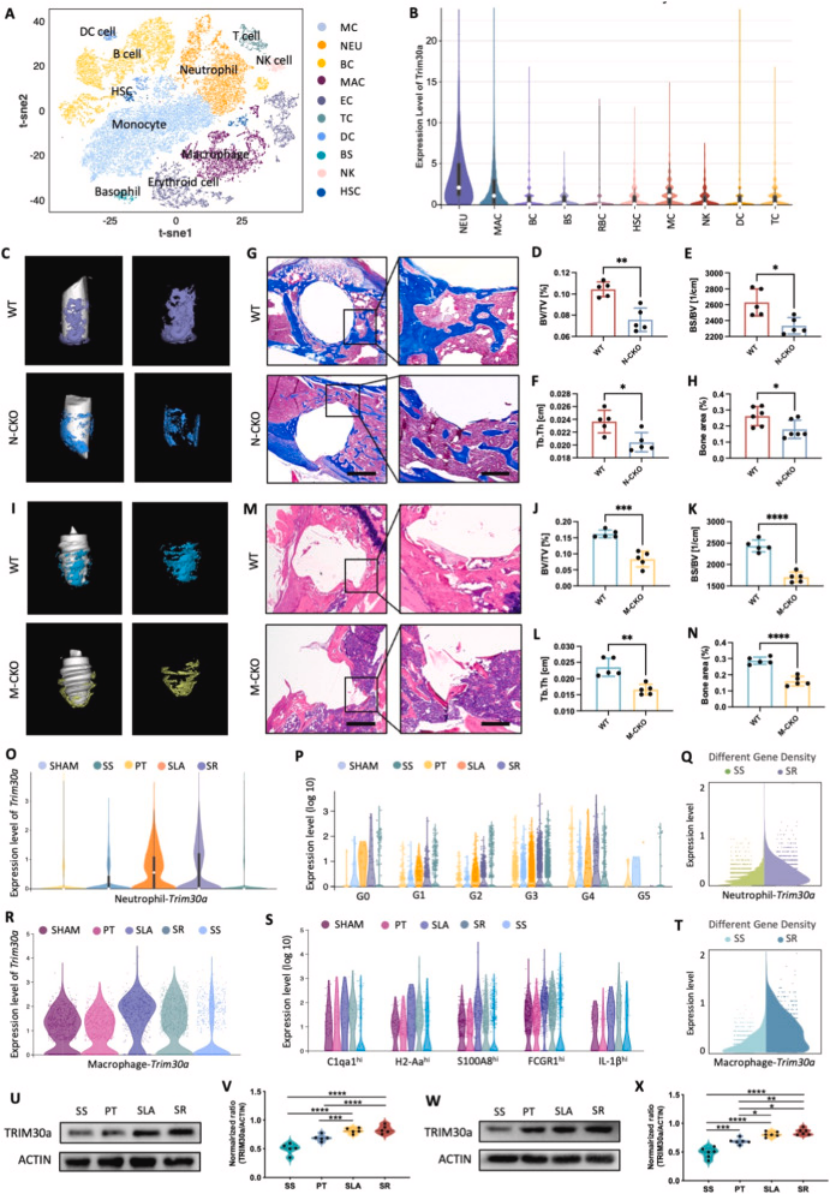
图2
第三步:体内外机制验证,解析 TRIM30a 抑制中性粒细胞 NETosis 的分子通路(图 3、图 4)
植入体调控 NETosis 表型:成骨型植入体(SR/SLA)可显著抑制中性粒细胞 NETosis 相关基因 / 蛋白(Mpo、Elane、NE、MPO)表达,减少 ROS 产生和 dsDNA 释放,而非成骨型植入体(SS)则显著促进 NETosis(图 3A-K);
通路富集分析:KEGG 分析显示,成骨型植入体可显著抑制中性粒细胞中 NF-κB 和 NLRP3 炎症小体通路,降低通路关键蛋白的磷酸化和表达水平(图 3L-S);
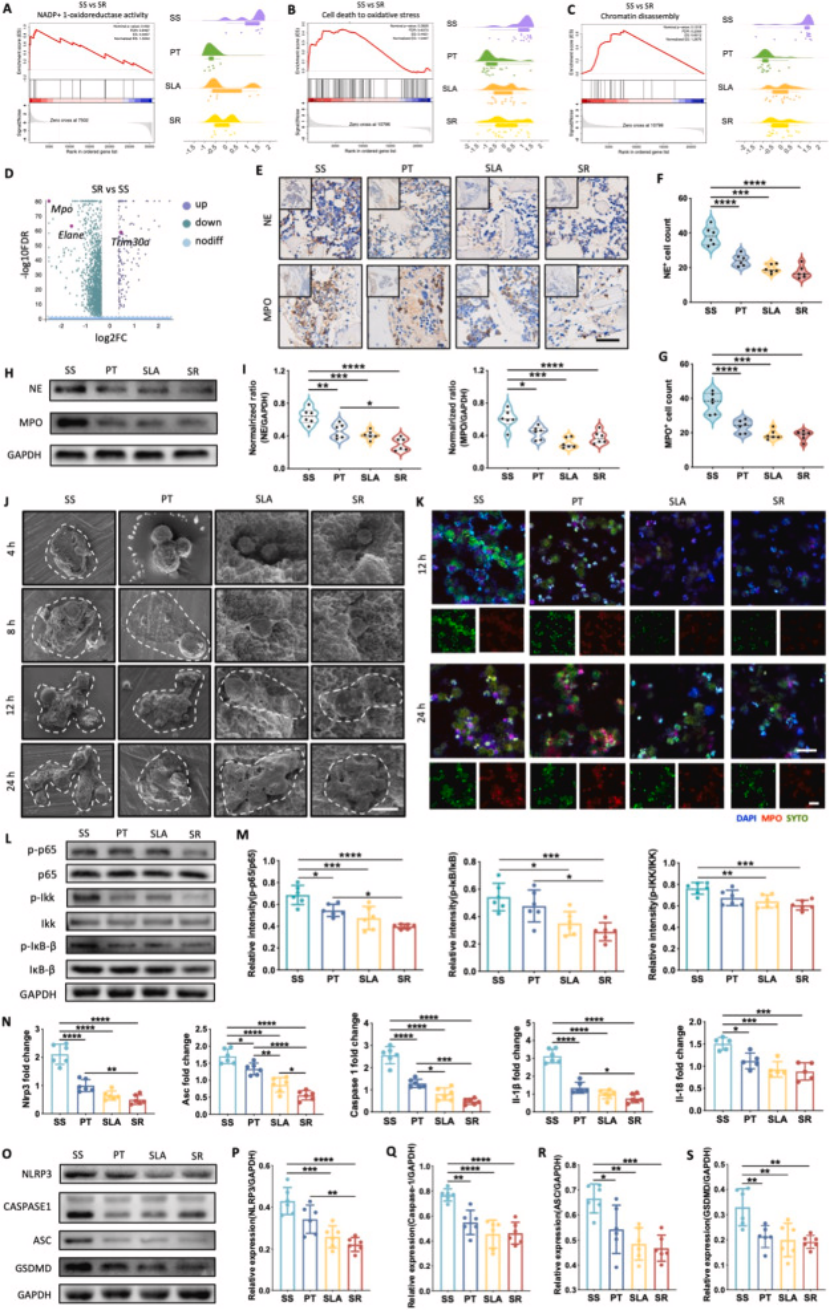
图3
TRIM30a 调控 NETosis 验证:通过 E3 泛素连接酶激动剂(PAR)/ 拮抗剂(K17)及 TRIM30a KO 细胞验证,TRIM30a 可显著抑制中性粒细胞 NETosis,KO 细胞则 NETosis 显著增强(图 4A-S);
核心机制解析:TRIM30a 通过抑制 NF-κB/NLRP3 通路的基因和蛋白表达,减少中性粒细胞 ROS、NE、MPO 释放及 dsDNA 分泌,从而抑制过度 NETosis(图 4T-AA),明确 TRIM30a 调控中性粒细胞的分子靶点。
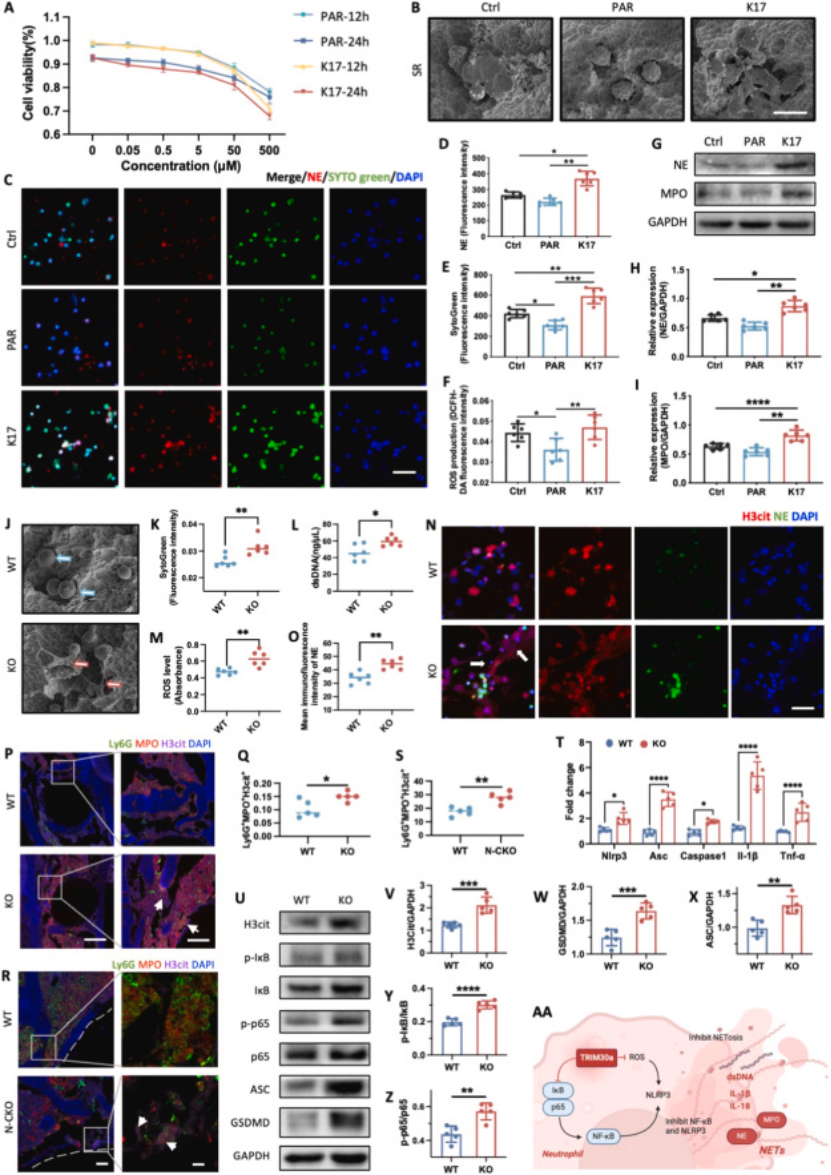
图4
第四步:细胞互作机制深挖,阐明 TRIM30a 校准巨噬细胞 cGAS-STING 信号的作用(图 5、图 6)
dsDNA 激活巨噬细胞信号:中性粒细胞 NETosis 释放的 dsDNA 可显著激活巨噬细胞 cGAS-STING 信号,DNase I 降解 dsDNA 则可抑制该通路(图 5A),明确 dsDNA 是中性粒细胞 - 巨噬细胞互作的分子桥梁;
TRIM30a 调控巨噬细胞感知 dsDNA:敲低巨噬细胞中 TRIM30a 可显著增强 cGAS-STING 通路及下游 NF-κB 通路的激活,促进 IFN-β、IL-6、TNF-α 等炎症因子分泌(图 5B-L),证实 TRIM30a 是巨噬细胞 cGAS-STING 信号的负调控因子;
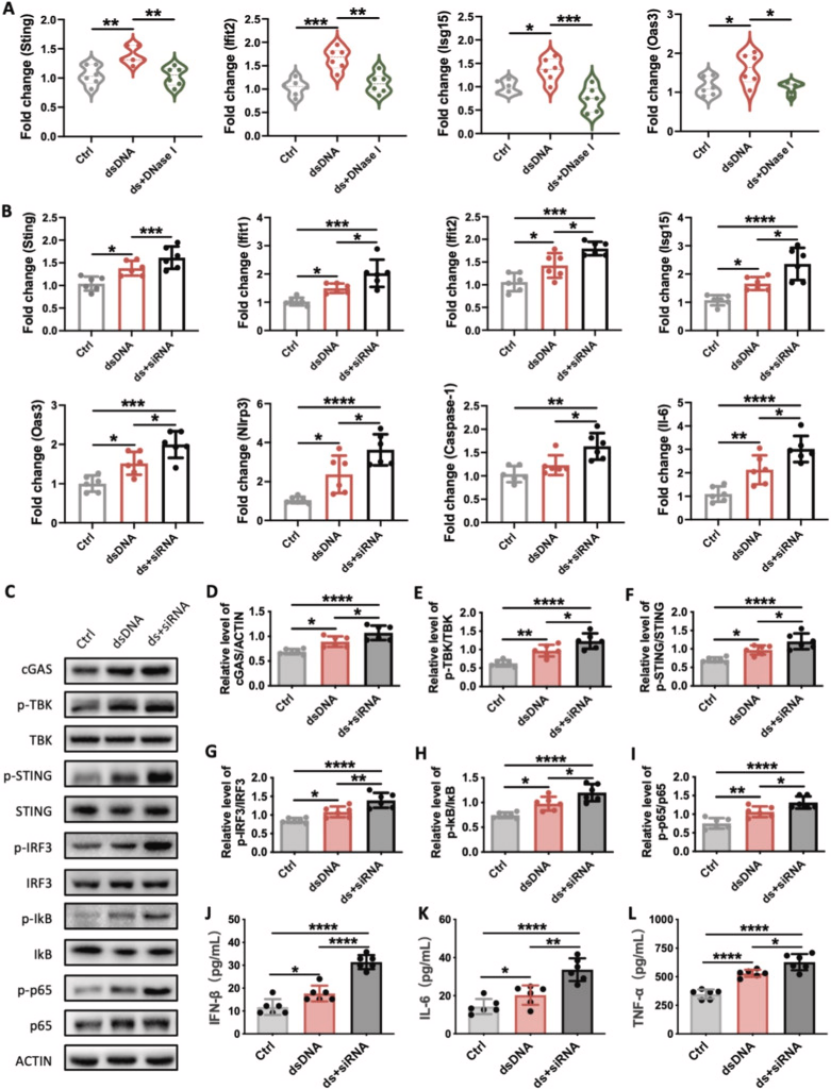
图5
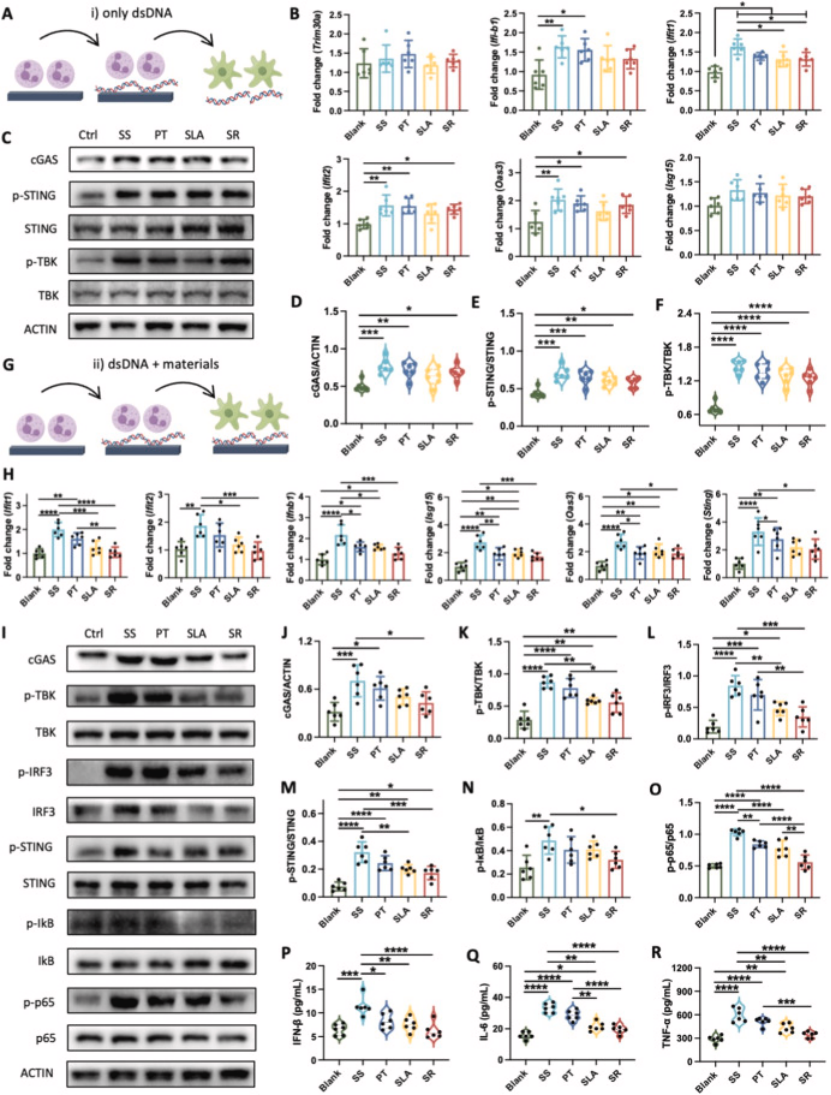
图6
植入材料协同调控机制:植入材料可通过双重途径调控巨噬细胞 cGAS-STING 信号:一是通过 TRIM30a 调控中性粒细胞 dsDNA 释放,二是直接调控巨噬细胞 TRIM30a 表达,其中成骨型植入体(SR)可显著抑制该通路激活,减少炎症因子分泌,非成骨型植入体(SS)则相反(图 6A-R),阐明植入体 - TRIM30a - 免疫细胞互作的完整调控网络。
第五步:药理学干预验证,证实 DNase I 靶向 dsDNA 可挽救骨整合缺陷(图 7)
药理学干预设计:对 TRIM30a KO 小鼠进行 DNase I 局部 + 全身注射,靶向降解 NETosis 释放的 dsDNA;
表型验证:免疫荧光证实 DNase I 可显著减少 KO 小鼠植入体周围 NETs 形成(图 7A-B);
成骨挽救验证:微 - CT 证实 DNase I 处理可显著恢复 KO 小鼠植入体周围骨体积、骨小梁厚度等成骨指标(图 7C-E),明确靶向 TRIM30a-NETosis/cGAS-STING 轴可有效提升骨整合效果,为临床干预提供可行方案;
机制总结:构建 TRIM30a 协调中性粒细胞 - 巨噬细胞互作调控骨整合的机制模型,明确成骨型植入体通过上调 TRIM30a,抑制中性粒细胞 NF-κB/NLRP3-NETosis 通路,同时校准巨噬细胞 cGAS-STING 信号,优化成骨免疫微环境,最终促进骨整合(图 7F)。
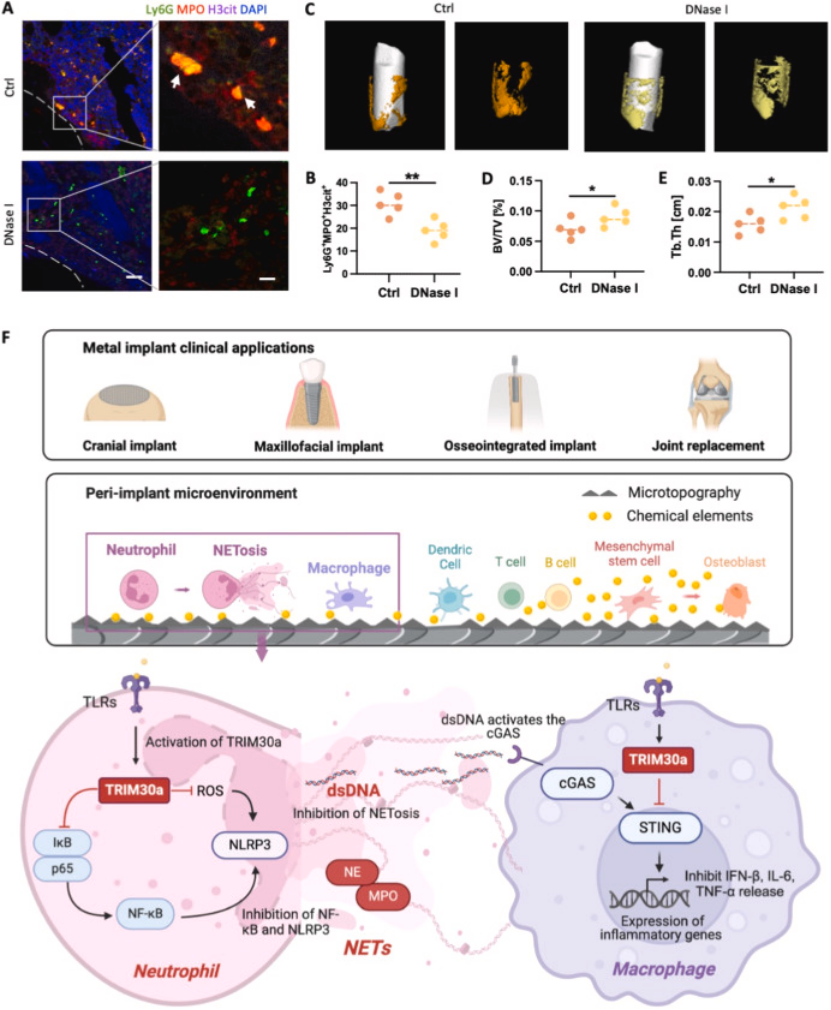
图7
医生发多组学顶刊论文的核心逻辑总结
浙江大学团队的这篇 IF=10.2 论文,为临床医生开展多组学研究并发表论文提供了可直接复刻的研究思路和行文架构,核心要点可归纳为 4 点:
选点精准:紧扣临床痛点(植入体骨整合失败),聚焦学科前沿(免疫细胞互作、NETosis/cGAS-STING 轴),将材料优化与免疫调控结合,提升研究的临床转化价值;
技术组合:采用“多组学筛分子 + 单细胞定细胞 + 体内外验机制 + 药理学证临床” 的经典技术路线,多组学(转录组 + 蛋白质组)挖掘核心调控因子,单细胞测序精准定位功能细胞,体内外实验层层解析分子机制,药理学干预验证临床应用潜力,技术体系完整且符合顶刊要求;
逻辑递进:研究结论由表型到分子、由单细到互作、由机制到干预,每一步均有对应的实验和图表支撑,关键图表(图 1-7)层层递进,从筛选因子到定位细胞,再到解析通路、验证干预,形成完整的证据链;
靶点明确:最终锁定 TRIM30a 及下游 NETosis/cGAS-STING 轴为骨整合的关键调控靶点,提出 DNase I 靶向干预方案,研究成果兼具基础理论价值和临床转化意义,契合顶刊对研究创新性和实用性的双重要求。
DOI: 10.1016/j.mtbio.2025.102652
专注期刊投稿、发表十年,任何投稿、写作难题欢迎咨询!

PAPER INFORMATION

快速预审、投刊前指导、专业学术评审,对文章进行评价

校对编辑、深度润色,让稿 件符合学术规范,格式体例等标准
.png)
适用于语句和结构尚需完善和调整的中文文章,确保稿件达到要求
.png)
数据库包括: 期刊、文书籍、会议、预印章、书、百科全书和摘要等

让作者在期刊选择时避免走弯路,缩短稿件被接收的周期

根据目标期刊格式要求对作者文章进行全面的格式修改和调整
.png)
帮助作者将稿件提交至目标期刊投稿系统,降低退稿或拒稿率
.png)
按照您提供的稿件内容,指导完成投稿附信(cover letter)

北京总部:北京市海淀区碧桐园 3 号楼 2 层 211 广州办事处:广州市黄埔区科学城国际企业孵化器 E栋306 联系人:客服 / 18163670350
Copyright © 2022-2024 北京特诺科技有限公司 版权所有 备案/许可证编号为: 京 ICP 备 2023007944 号