
来源:特诺科研

文章信息速览
原标题:Spatial multi-omics guides ASCT2-targeted delivery of glycolysis inhibitor for cervical cancer suppression and chemoresistance reversal
期刊:Journal of Advanced Research(IF=13.0)
关键词:宫颈癌、空间多组学、ASCT2 靶向、糖酵解抑制、顺铂耐药逆转、纳米脂质体、lonidamine(LND)
核心创新:① 空间多组学首次在临床组织层面验证宫颈癌肿瘤区域特异性糖酵解依赖,筛选出 ASCT2 为优选靶点(特异性优于 CD44);② 构建谷氨酰胺修饰脂质体(GL),实现 ASCT2 介导的肿瘤选择性 LND 递送,解决药物生物利用度低、肝毒性强的痛点;③ 双效机制:切断 ATP 供应 + 诱导 ROS 损伤抑瘤,抑制 MRP2 介导的顺铂外排 + 阻断 R5P 依赖的 DNA 修复逆转耐药;④ 体内外多模型(细胞、3D 肿瘤球、荷瘤小鼠)验证,抑瘤率最高达 85.21%,无明显肝肾损伤。
研究背景与临床痛点
宫颈癌治疗的三大核心困境亟待突破:
耐药率居高不下:顺铂是宫颈癌一线化疗药物,但临床耐药率高,耐药后患者预后极差,缺乏有效替代疗法;
糖酵解靶向瓶颈:肿瘤细胞依赖增强的糖酵解供能、维持耐药,但此前缺乏空间 resolved 验证(无法确认肿瘤区域是否特异性依赖),且糖酵解抑制剂(如 LND)生物利用度低、肝毒性显著,缺乏肿瘤特异性递送系统;
靶点选择局限:现有纳米载体多靶向 CD44 等泛癌靶点,肿瘤选择性不足,易脱靶导致副作用,治疗效果打折扣。
研究核心目标:① 用空间多组学精准定位宫颈癌的糖酵解依赖区域和特异性靶点;② 设计肿瘤靶向纳米载体,高效递送 LND,同时降低毒性;③ 验证其抑瘤活性及逆转顺铂耐药的双重功效。
研究核心亮点
这篇 IF=13.0 的研究以 “空间多组学指导精准治疗” 为核心,4 大亮点直击临床痛点:
1. 空间多组学 “精准导航”:锁定 ASCT2 为宫颈癌特异性靶点
首次通过空间代谢组(AFADESI-MSI)与空间转录组(10x Visium)联合分析,在临床宫颈癌组织中完成 “代谢 - 转录” 空间匹配:
糖酵解依赖验证:肿瘤区域葡萄糖代谢产物(m/z 215.0317)显著富集,糖酵解通路关键酶(HKⅡ、PFKP、PKM)转录水平上调,明确宫颈癌肿瘤区域存在特异性糖酵解依赖(图2c-d-e);
靶点筛选:从空间转录组数据中锁定谷氨酰胺转运体 ASCT2(SLC1A5),其在肿瘤区域特异性高表达,且在免疫细胞中不表达 —— 对比泛癌靶点 CD44,ASCT2 的肿瘤 / 正常组织表达差异更显著,是更优的特异性靶点(图1g-h);
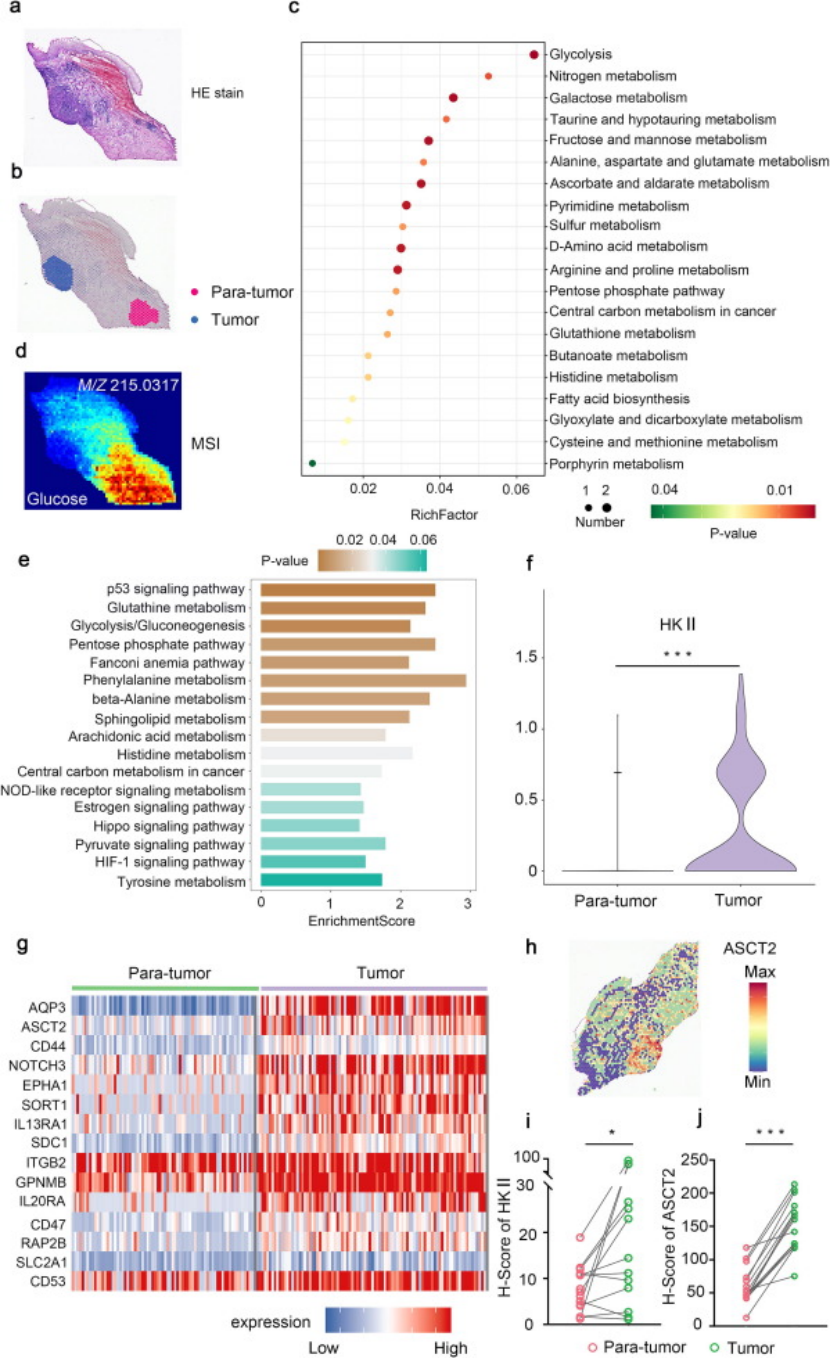
图1
多平台验证:单细胞 RNA-seq、TCGA 队列、15 对临床癌旁组织、小鼠模型及 5 种宫颈癌细胞系均证实:ASCT2 和 HKⅡ 在肿瘤组织中普遍高表达,验证靶点可靠性(图1i-j、S7-S16)。
2. 纳米载体 “精准投递”:谷氨酰胺修饰脂质体(GL),肿瘤靶向性拉满
基于 ASCT2 靶点设计谷氨酰胺(Gln)修饰脂质体(GL),解决 LND 递送难题:
载体表征:球形结构,粒径~108 nm,zeta 电位 - 44.18 mV,LND 包封率达 94%,载药率 7.5%,具备缓释特性,能持续释放药物(图2a-c-d);
靶向机制:GL 通过谷氨酰胺与肿瘤细胞表面 ASCT2 特异性结合,介导内吞 —— 预处理游离谷氨酰胺、ASCT2 抑制剂(GPNA)或 ASCT2 抗体后,细胞摄取量显著下降,证实靶向特异性(图2g-h);
体内靶向:SiHa 荷瘤小鼠静脉注射后,GL@Cy7 在肿瘤区域富集度显著高于未修饰脂质体,12 小时肿瘤荧光强度达峰值,且主要脏器分布少(图3i-j);
安全性:GL 载体本身无细胞毒性(500 μg/mL 浓度下细胞存活率>90%),无溶血活性,为后续给药安全性奠定基础(图2e-f)。
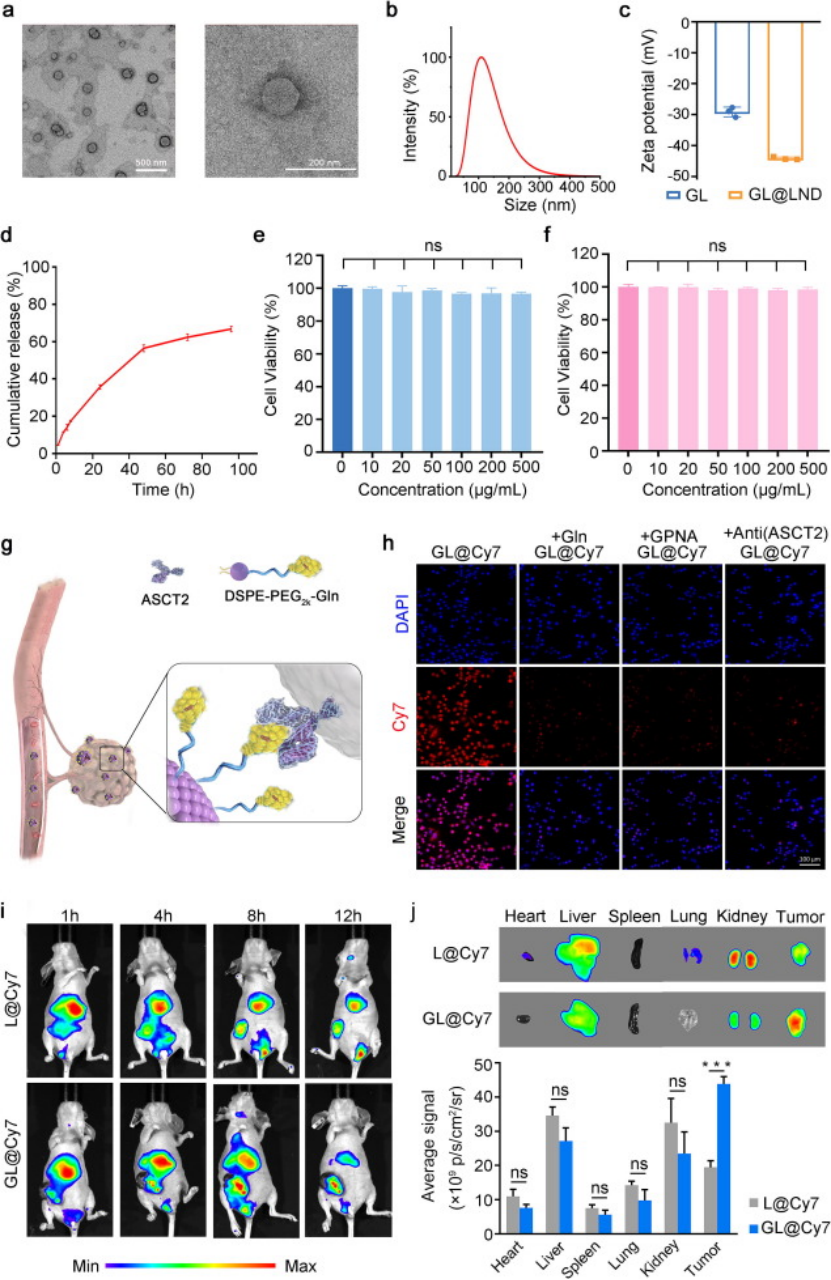
图2
3. 双效机制 “精准打击”:抑瘤 + 耐药逆转,一步到位
GL@LND 通过双重机制发挥作用,既解决 “肿瘤生长” 问题,又破解 “耐药” 困局:
抑瘤机制:LND 特异性抑制糖酵解关键酶 HKⅡ,切断肿瘤 ATP 供应(GL@LND 组 ATP 降低幅度是游离 LND 的 2 倍以上);同时诱导线粒体膜电位 depolarization,促进 ROS 生成,激活 Cyto-C/Bax/Bcl-2 凋亡通路 ——SiHa 细胞凋亡率达 25.58%,是游离 LND 组(6.51%)的 4 倍(图3a-g);
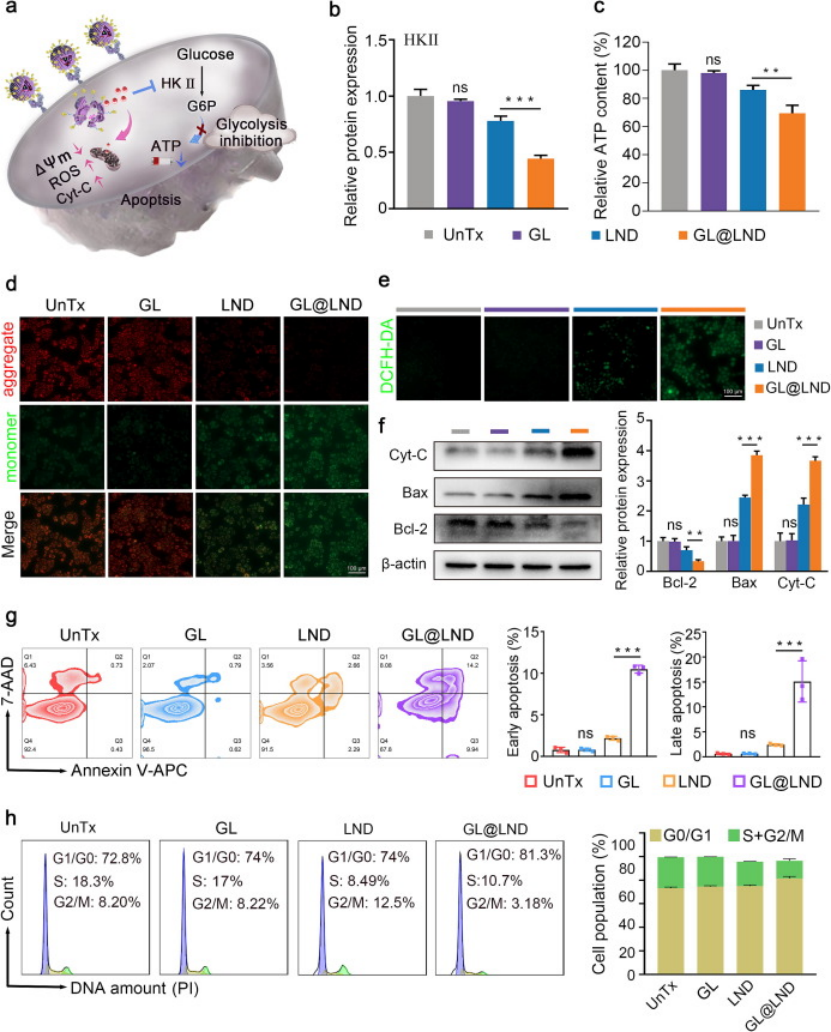
图3
耐药逆转机制:① 抑制 MRP2 介导的顺铂外排:LND 减少 ATP 生成,下调 ATP 依赖的多药耐药蛋白 MRP2,增加顺铂在耐药细胞(SiHa-DR)内积累;② 阻断 R5P 依赖的 DNA 修复:抑制糖酵解分支戊糖磷酸途径(PPP)关键酶 G6PD,减少 R5P 生成,阻碍顺铂诱导的 DNA 损伤修复 ——γ-H2AX 表达提升 2.67 倍,耐药细胞对顺铂重新敏感(图4a-j)。
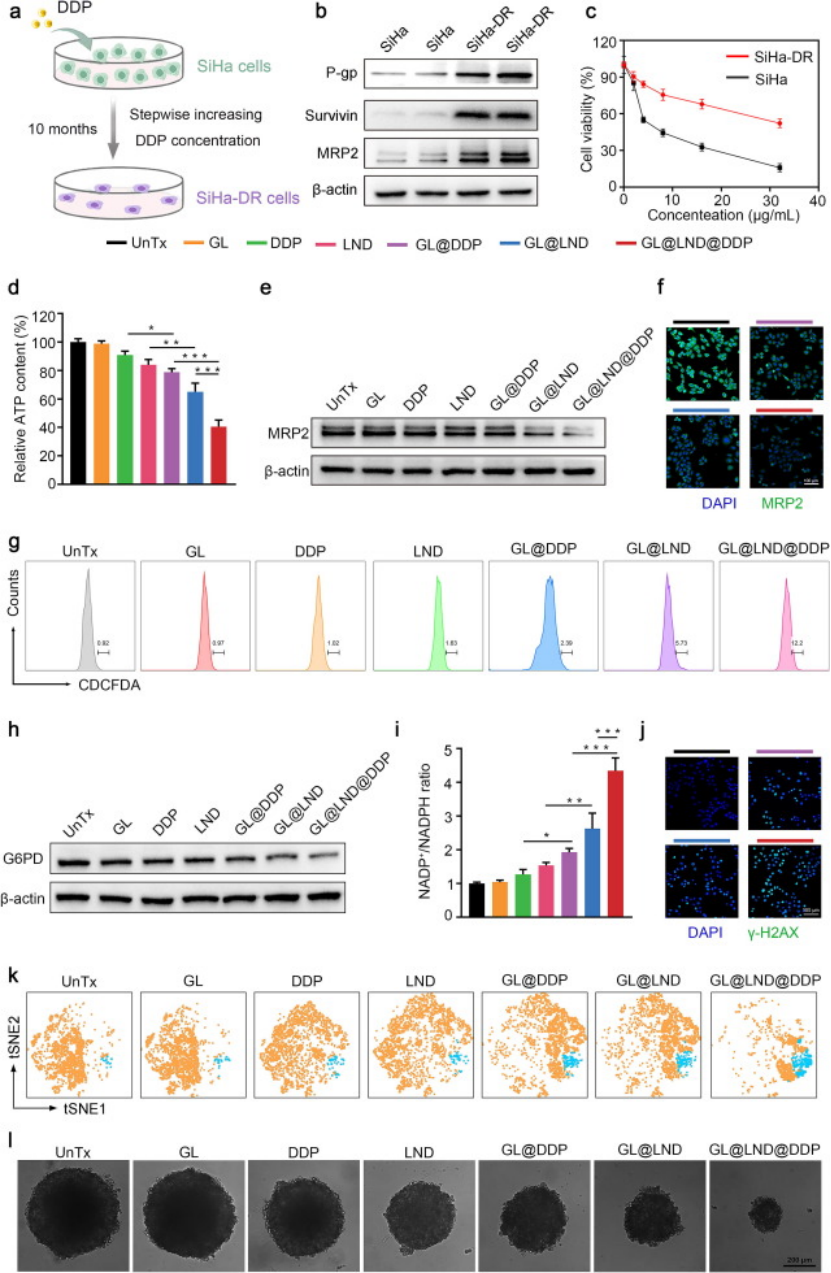
图4
4. 体内外验证 “精准落地”:抑瘤率 85.21%,安全性优异
多模型验证疗效,无明显毒副作用,临床转化潜力大:
敏感型宫颈癌:SiHa 细胞体外活力下降 60.72%(游离 LND 组仅 31.50%),3D 肿瘤球直径显著缩小;小鼠体内肿瘤抑瘤率达 68.77%,Ki-67 增殖 marker 降低,TUNEL 凋亡信号增强(图5a-g);
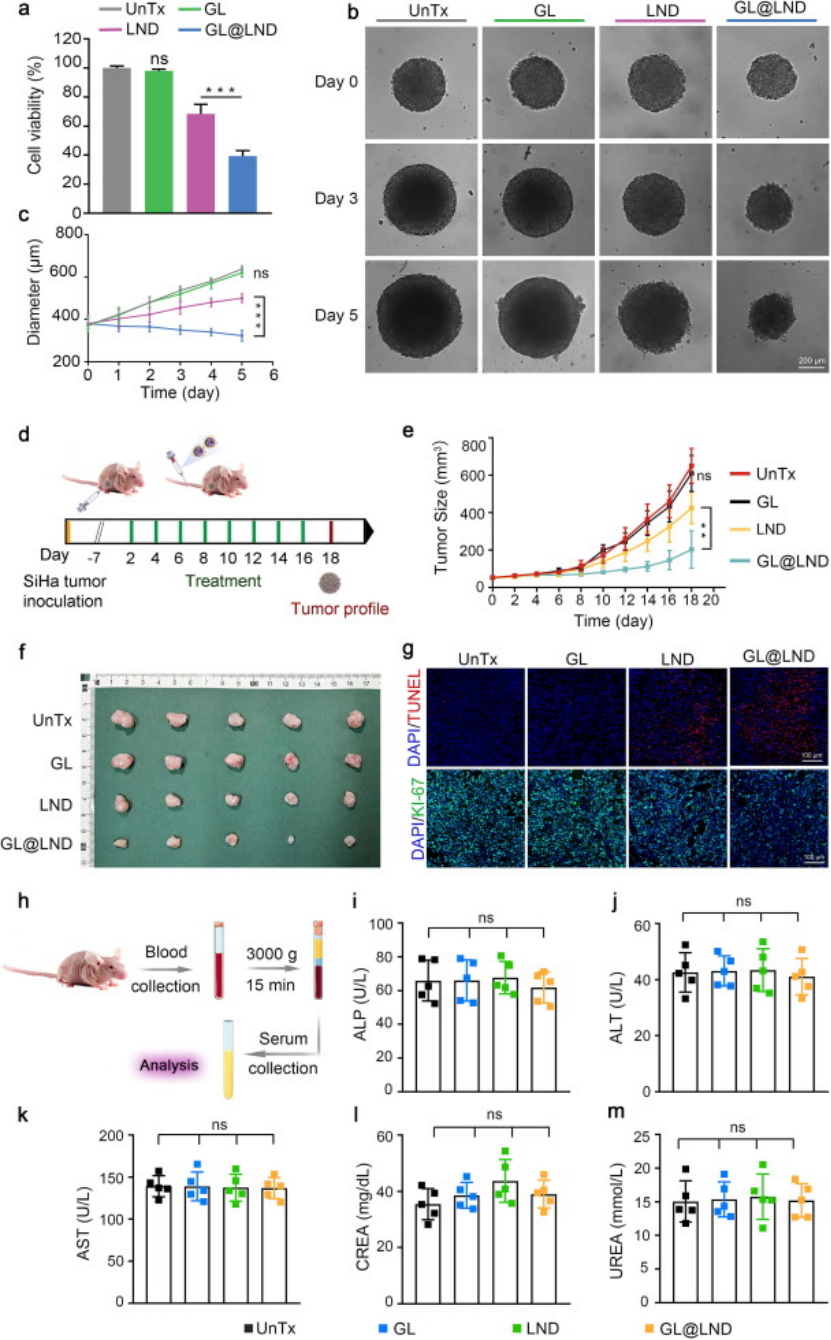
图5
顺铂耐药宫颈癌:SiHa-DR 细胞体外活力下降 86.70%(GL@DDP 组仅 38.70%),3D 肿瘤球几乎瓦解;小鼠体内肿瘤抑瘤率达 85.21%,而顺铂单药组肿瘤持续增长(图6a-e);
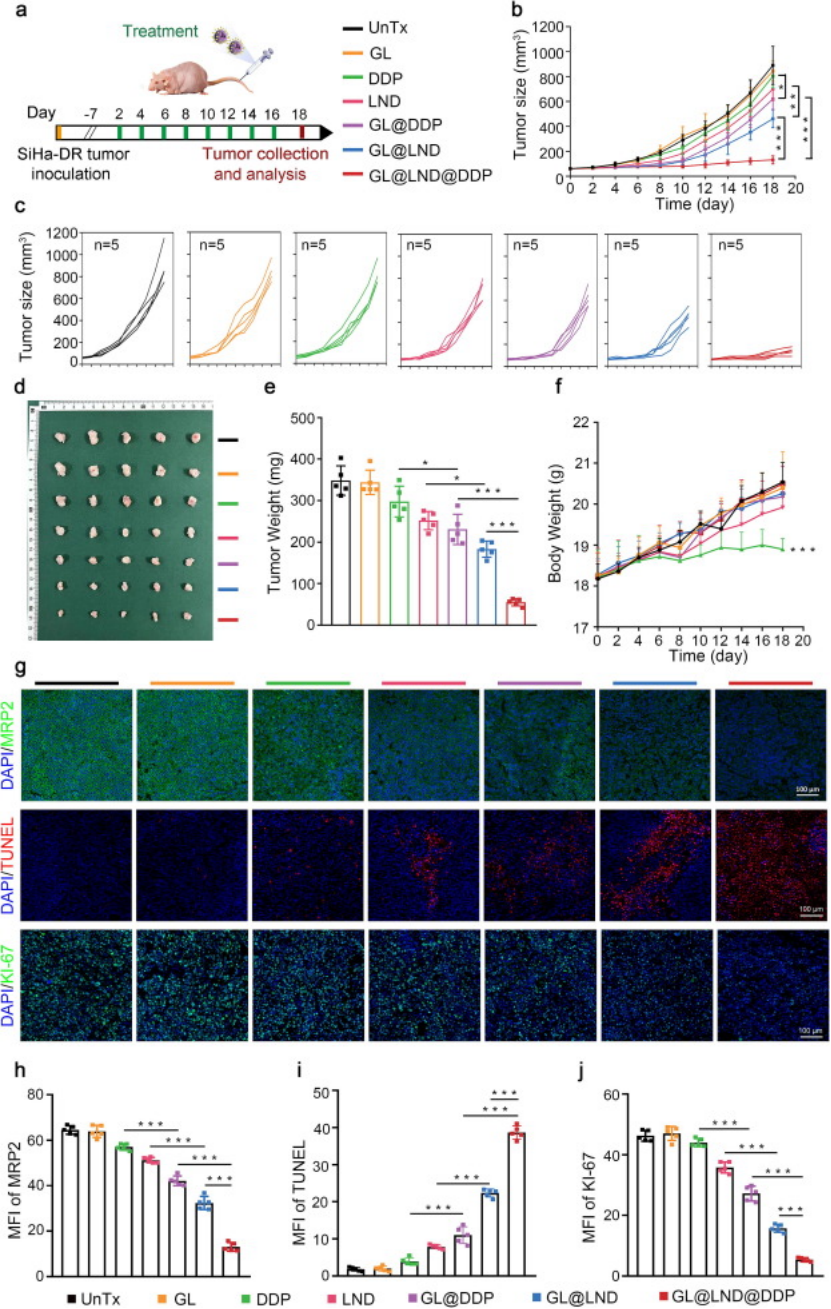
图6
安全性:给药期间小鼠体重稳定,肝肾功能指标(ALT、AST、CREA 等)无异常,主要脏器(心、肝、脾、肺、肾)组织形态正常,无明显毒副作用。
临床价值
对患者:破解顺铂耐药困境,提供全新治疗选择,同时降低药物肝毒性,提升治疗耐受性,改善预后;
对临床:提供“空间多组学靶点筛选→肿瘤特异性纳米递送→双效机制治疗” 的临床转化范式,可快速推进至临床前研究,填补耐药宫颈癌治疗空白;
对科研:验证 ASCT2 作为宫颈癌特异性靶点的潜力,为乳腺癌、卵巢癌等其他糖酵解依赖型肿瘤提供 “靶点筛选 - 药物递送” 参考,拓宽应用场景。
总体来说,这篇研究的核心突破在于构建了“空间多组学精准定位靶点→肿瘤特异性纳米递送→双效机制破解临床困境” 的完整闭环。空间多组学首次在临床组织层面证实宫颈癌的糖酵解依赖,锁定 ASCT2 这一 “比 CD44 更优” 的特异性靶点;谷氨酰胺修饰脂质体(GL)解决了 LND 的递送难题,实现 “精准给药、降低毒性”;而 “抑瘤 + 耐药逆转” 的双重机制,直击宫颈癌治疗的核心痛点。
随着后续前瞻性临床研究的推进,这款 ASCT2 靶向纳米药有望成为顺铂耐药宫颈癌患者的 “救命药”,同时为其他实体瘤的精准治疗提供可复制的研究范式,推动肿瘤治疗进入 “空间多组学指导下的靶点特异性治疗” 新时代。
原文DOI; 10.1016/j.jare.2025.11.035
专注期刊投稿、发表十年,任何投稿、写作难题欢迎咨询!

PAPER INFORMATION

快速预审、投刊前指导、专业学术评审,对文章进行评价

校对编辑、深度润色,让稿 件符合学术规范,格式体例等标准
.png)
适用于语句和结构尚需完善和调整的中文文章,确保稿件达到要求
.png)
数据库包括: 期刊、文书籍、会议、预印章、书、百科全书和摘要等

让作者在期刊选择时避免走弯路,缩短稿件被接收的周期

根据目标期刊格式要求对作者文章进行全面的格式修改和调整
.png)
帮助作者将稿件提交至目标期刊投稿系统,降低退稿或拒稿率
.png)
按照您提供的稿件内容,指导完成投稿附信(cover letter)

北京总部:北京市海淀区碧桐园 3 号楼 2 层 211 广州办事处:广州市黄埔区科学城国际企业孵化器 E栋306 联系人:客服 / 18163670350
Copyright © 2022-2024 北京特诺科技有限公司 版权所有 备案/许可证编号为: 京 ICP 备 2023007944 号