
来源:特诺科研
食管鳞状细胞癌(ESCC)是亚洲高发恶性肿瘤,5 年生存率仅 10%-30%,肿瘤内 / 间异质性显著导致早诊难、治疗手段有限,精准诊疗靶点匮乏成为临床核心痛点。近日,郑州大学团队在《Protein & Cell》(IF=12.8,生物领域顶刊,0 版面费开源获取)发表重磅综述研究,整合基因组、表观基因组、转录组、蛋白质组、代谢组等多组学技术,结合单细胞测序与实验验证,全面解析 ESCC 分子特征、肿瘤异质性及核心调控通路,还明确了多组学在 ESCC 诊断、预后、治疗中的临床转化价值,为食管鳞癌精准诊疗提供全新思路!医生朋友想发高分区多组学顶刊论文,专业论文服务就找我们,全程助力从实验设计、数据整合到发文落地,轻松攻克多组学发文难题。

文章信息速览
原标题:Advances in multi-omics for esophageal squamous cell carcinoma: Diagnostic, prognostic, and therapeutic perspectives
期刊:Protein & Cell(IF=12.8,生物领域顶刊,0 版面费开源获取,遵循 CC BY 4.0 协议)
关键词:食管鳞状细胞癌、高通量组学、基因组、转录组、代谢组、蛋白质组、诊断标志物、预后标志物、治疗靶点、肿瘤微环境
研究背景与临床痛点
患病现状严峻:ESCC 占全球食管癌发病的 90%,亚洲为高发区域,5 年生存率仅 10%-30%,手术切除为主要根治手段,但局部晚期患者术后易复发、远处转移,预后极差。
精准诊疗困境:ESCC 肿瘤内 / 间异质性突出,缺乏特异性早诊标志物,传统放化疗、免疫治疗未结合患者分子特征制定个性化方案,治疗响应率低。
技术应用短板:单一组学技术仅能揭示肿瘤某一层面的分子变化,无法系统解析 ESCC 发生发展的完整机制,而多组学整合分析的标准化流程尚未建立。
临床转化障碍:多组学在 ESCC 中的研究虽有进展,但因样本质量参差不齐、多中心验证不足、数据整合难度大,难以落地常规临床诊疗工作。
研究核心亮点
这篇 IF=12.8 顶刊综述,完美契合生物领域顶刊对多组学研究的审稿偏好,从临床痛点切入→单组学分层解析→多组学整合创新→临床转化落地→展望领域未来的五步逻辑,成为医生发表多组学顶刊论文的绝佳范本,关键结果均以可视化图表支撑(图 1-6),让研究核心一目了然:
第一步:锚定临床痛点,单组学分层解析分子特征,夯实研究基础(图 1、2)
发文技巧:从临床高发肿瘤的诊疗痛点切入,先通过单组学技术解析核心分子特征,结合公共数据库交叉验证,为多组学整合奠定坚实基础,同时用示意图清晰展示分子调控通路和公共数据集分布,让审稿人快速抓住研究核心。关键结果:
基因组层面:通过全基因组 / 外显子测序,明确 TP53、NOTCH1、FAT1 等为 ESCC 高频突变基因,RTK/RAS、PI3K/AKT、Wnt 等为核心致癌通路,绘制出 ESCC 基因组全景图谱(图 1)。
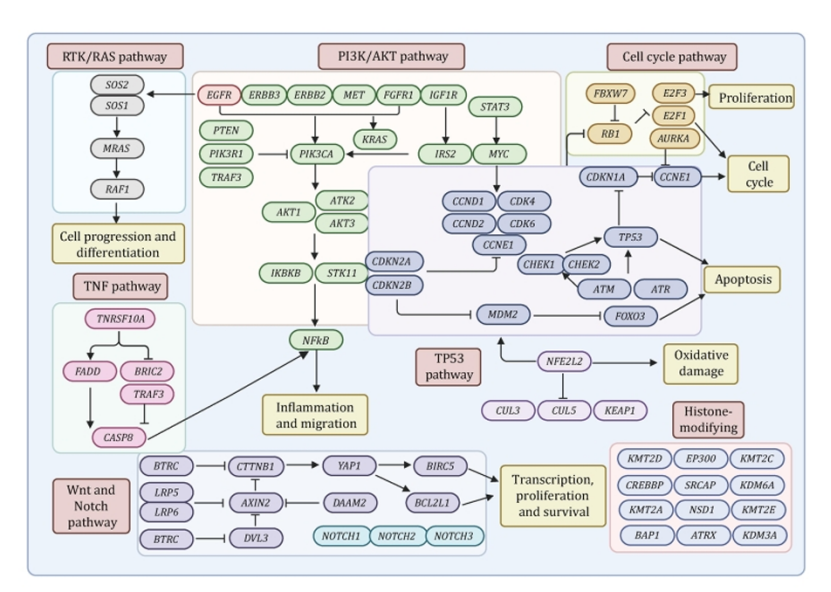
图1
转录组层面:整合 GEO 公共数据集,系统解析 mRNA、lncRNA、miRNA、circRNA 等多 RNA 层表达特征,筛选出 ANO1、MMP3、PLEK2 等与 ESCC 预后密切相关的基因(图 2)。
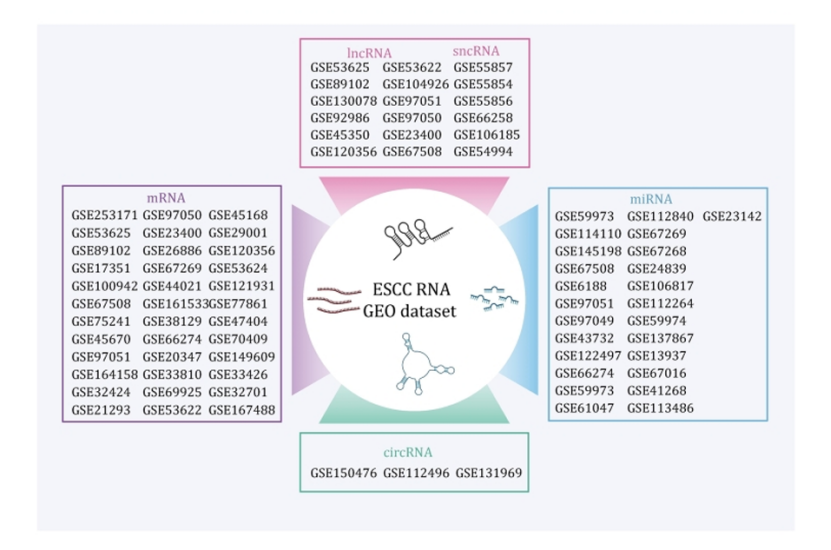
图2
第二步:多组学横向整合,跨维度挖掘分子关联,打造研究核心创新点(图 3、4)
发文技巧:单一组学研究难以登上顶刊,需通过单细胞测序(scRNA-seq)整合多组学数据,同时结合蛋白翻译后修饰(PTMs)分析,跨维度挖掘分子间调控关系,突出研究的系统性和创新性,用流程示意图展示技术路线和核心发现。关键结果:
单细胞测序整合多组学:解析出 ESCC 肿瘤微环境的免疫抑制特征,发现 CST1⁺肌成纤维细胞与患者不良预后相关,还明确了肿瘤细胞与微环境的复杂通讯网络(图 3)。
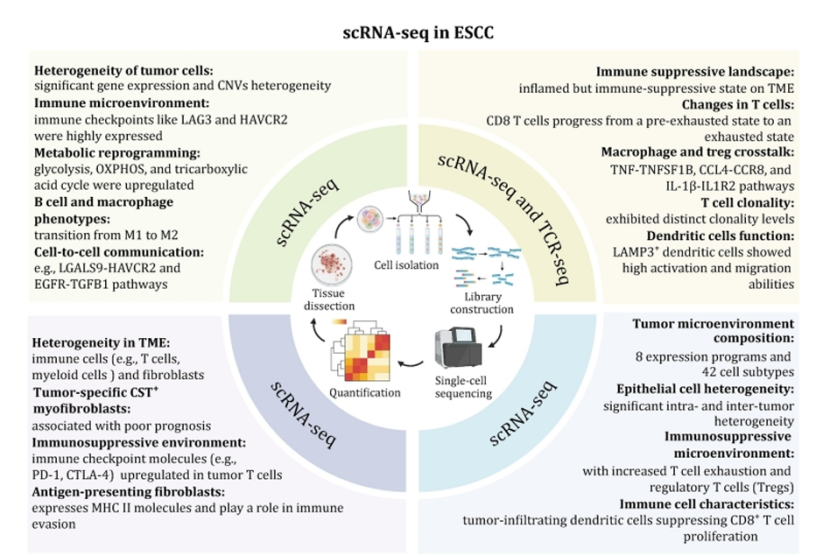
图3
蛋白翻译后修饰分析:总结出磷酸化、糖基化、乙酰化是 ESCC 的关键蛋白调控方式,为后续靶点挖掘提供了全新方向(图 4)。
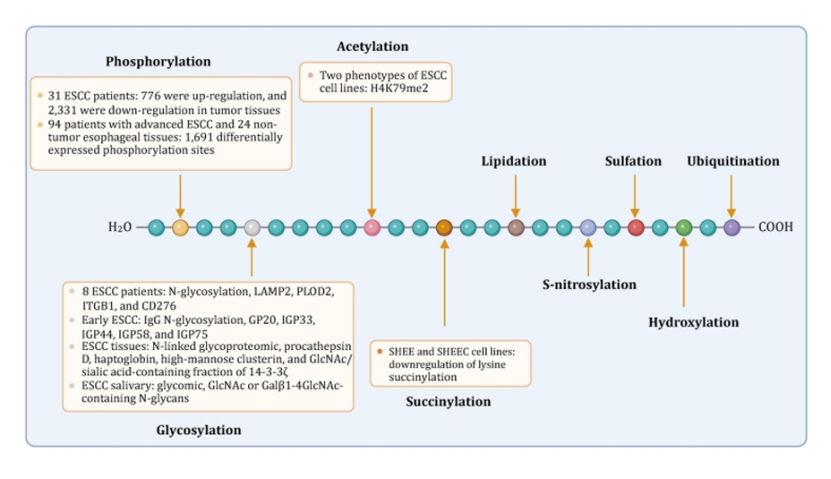
图4
第三步:聚焦临床转化,多组学锚定诊疗标志物与治疗靶点,实现研究价值落地(图 5)
发文技巧:顶刊高度重视研究的临床意义,多组学分析后需进一步锚定可转化的诊断 / 预后标志物和可用药治疗靶点,搭建多组学分析 - 分子特征 - 临床应用的完整逻辑链,用示意图清晰展示转化路径。关键结果:
诊断 / 预后标志物:筛选出 PAX9、SIM2 等甲基化早诊标志物,以及 CCND1、SOX2 等预后相关基因,为 ESCC 早筛和预后评估提供了特异性指标。
潜在治疗靶点:明确 PIK3CA、EGFR、HER2 等为 ESCC 可用药靶点,还通过多组学分析实现 ESCC 分子亚型分类,为患者分层治疗提供依据(图 5)。
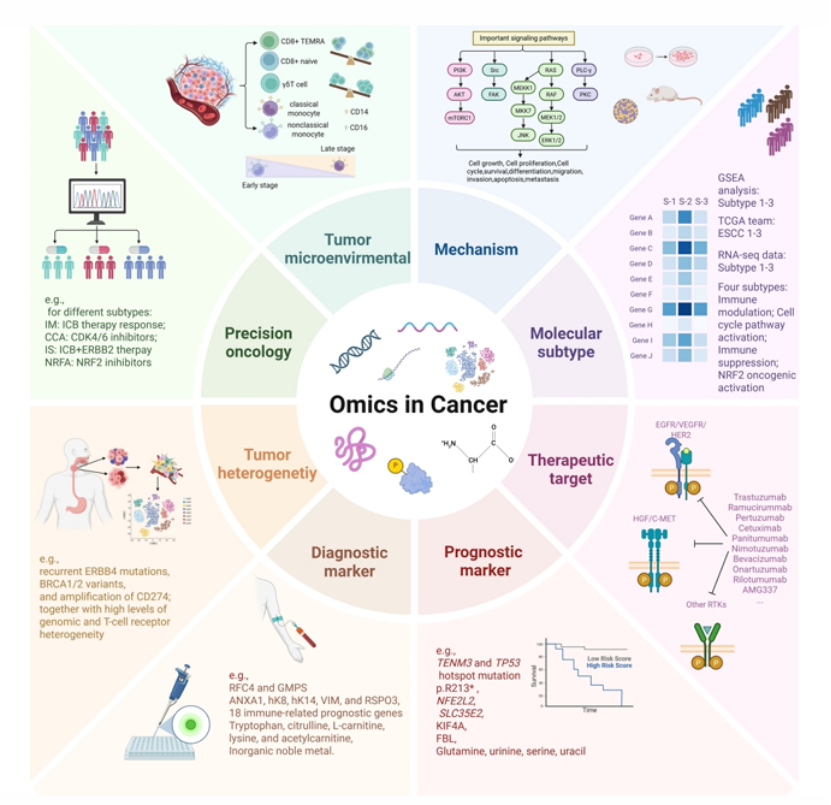
图5
第四步:直面研究挑战,提出解决方案与未来方向,提升研究深度与前瞻性(图 6)
发文技巧:高质量多组学文章不仅要解析领域现状,还需客观分析研究中存在的挑战,并提出针对性解决方案和未来研究方向,体现研究的前瞻性和深度,契合顶刊的审稿要求。关键结果:
指出领域挑战:ESCC 多组学研究存在样本匮乏、肿瘤异质性大、分析流程不标准、多中心验证不足等问题。
提出未来方向:建议将人工智能与多组学数据结合,提升数据整合效率;开展大样本多中心研究,推动多组学成果向临床常规诊疗落地(图 6)。
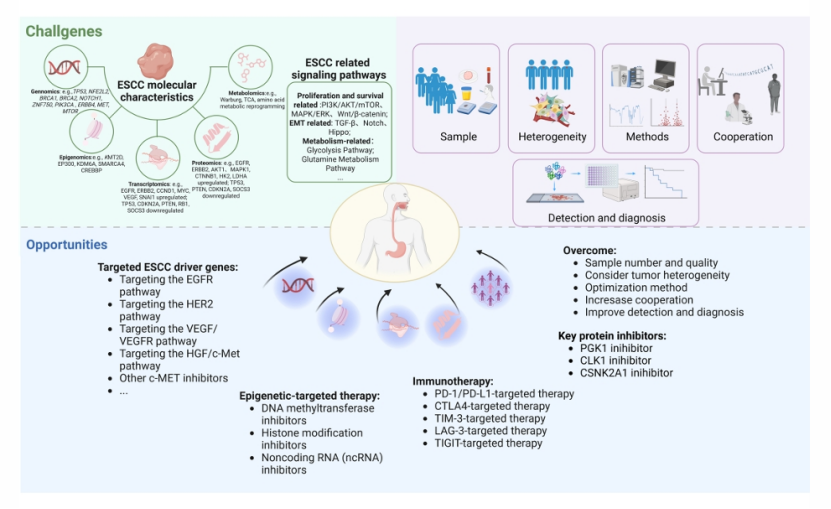
图6
从顶刊力作看:医生如何发表高质量多组学文章?
结合郑州大学团队这篇 IF=12.8 顶刊研究,从选题、技术、数据、图表、临床转化5 个核心维度,为临床医生梳理多组学文章的发文思路,避开发文误区,精准契合顶刊偏好:
1. 选题:紧扣临床痛点,拒绝 “纯数据堆砌”
多组学研究选题需围绕临床未解决的核心问题展开,如 ESCC 的早诊难、靶点匮乏、异质性大等,让研究始终服务于临床,避免脱离临床的纯基础组学数据解析,这样的研究更易获得顶刊认可。
2. 技术:单组学为基,多组学为核,结合实验验证
单一组学技术难以支撑高分区论文,建议采用单组学分层解析 + 多组学整合分析 + 实验验证的技术搭配,比如基因组 + 转录组 + 代谢组联合,再用单细胞测序解析肿瘤微环境,通过细胞 / 动物实验验证靶点功能,让研究证据链更完整。
3. 数据:善用公共数据库,做好交叉验证
临床医生开展多组学研究时,可充分利用 GEO、TCGA 等公共数据库,补充自身样本量的不足;同时对组学数据进行多平台、多队列交叉验证,提升研究结果的可靠性。
4. 图表:可视化呈现,让复杂数据 “一目了然”
顶刊对图表要求极高,多组学研究涉及大量数据,需将复杂的分子通路、技术流程、临床转化路径转化为清晰的示意图(如图 1-6 的设计逻辑),让审稿人快速理解研究核心,提升文章可读性。
5. 临床转化:锚定 “诊疗价值”,让研究有落地可能
多组学研究的最终落脚点是临床转化,需从海量组学数据中筛选出可检测、可应用、可验证的标志物和靶点,或提出个性化治疗、患者分层的策略,让研究不只是“纸上谈兵”,而是有实际的临床应用价值。
总结
郑州大学团队在《Protein & Cell》发表的这篇多组学综述,不仅全面解析了食管鳞癌的高通量组学分子特征,为ESCC 的精准诊断、预后评估和靶向治疗提供了重要依据,更以0 版面费开源发表的模式,让更多研究者能免费获取研究成果,助力食管鳞癌领域的发展。同时,这篇研究的行文和研究逻辑,也为临床医生发表多组学顶刊论文提供了可复制、可借鉴的范本 —— 多组学研究的核心从来不是 “技术的堆砌”,而是以技术为工具,解决临床问题,实现临床转化。
原文DOI:10.1093/procel/pwag005
专注期刊投稿、发表十年,任何投稿、写作难题欢迎咨询!

PAPER INFORMATION

快速预审、投刊前指导、专业学术评审,对文章进行评价

校对编辑、深度润色,让稿 件符合学术规范,格式体例等标准
.png)
适用于语句和结构尚需完善和调整的中文文章,确保稿件达到要求
.png)
数据库包括: 期刊、文书籍、会议、预印章、书、百科全书和摘要等

让作者在期刊选择时避免走弯路,缩短稿件被接收的周期

根据目标期刊格式要求对作者文章进行全面的格式修改和调整
.png)
帮助作者将稿件提交至目标期刊投稿系统,降低退稿或拒稿率
.png)
按照您提供的稿件内容,指导完成投稿附信(cover letter)

北京总部:北京市海淀区碧桐园 3 号楼 2 层 211 广州办事处:广州市黄埔区科学城国际企业孵化器 E栋306 联系人:客服 / 18163670350
Copyright © 2022-2024 北京特诺科技有限公司 版权所有 备案/许可证编号为: 京 ICP 备 2023007944 号