
来源:特诺科研
青蒿素类药物是全球抗疟的“主力军”,但恶性疟原虫的 “环期存活(RS)” 表型 —— 部分环状体可耐受药物短半衰期潜伏存活,最终导致感染复发 —— 一直是耐药防控的棘手难题。此前仅明确 PfK13 基因突变与耐药相关,却无法解释大量无 PfK13 突变的耐药现象。近日,由中、美、法等国研究者组成的联合团队在《Nature Communications》(2024 IF=15.7)发表突破性研究:组蛋白乙酰转移酶 PfMYST 通过表观遗传调控,独立且协同 PfK13 通路驱动恶性疟原虫环期存活,同时影响多种抗疟药敏感性,填补了青蒿素耐药的表观遗传机制空白!
文章信息速览
原标题:Epigenetically conferred ring-stage survival in Plasmodium falciparum against artemisinin treatment
期刊:Nature Communications(综合顶刊,2024 IF=15.7)
关键词:恶性疟原虫、青蒿素耐药、环期存活(RS)、PfMYST、表观遗传、PfK13、多组学、单细胞 RNA 测序
研究背景与目的
青蒿素耐药的临床痛点亟待破解:
恶性疟原虫环状体存活(RS≥1% 为 “部分耐药”)依赖联合用药清除,一旦联合药物失效,复发率显著升高;
PfK13 基因突变仅能解释部分耐药案例,大量耐药菌株无该突变,提示存在未知调控途径;
表观遗传调控被推测参与耐药,但具体分子靶点、调控网络及与已知通路的关系不明。
团队核心目标:① 筛选调控RS 表型的表观遗传关键因子;② 解析其分子机制及与 PfK13 通路的关联;③ 验证其对多种抗疟药的影响,为联合用药优化和新药研发提供依据。
核心创新:
① 首次证实 PfMYST 是调控恶性疟原虫 RS 表型的核心表观遗传因子,与耐药完全关联;
② 揭示 PfMYST 通过 H4K5ac/H4K8ac 修饰调控靶基因,诱导环期发育延迟和代谢静止;
③ 发现 PfMYST 与 PfK13 通路存在 46% 靶基因重叠,形成 “遗传 + 表观遗传” 双驱动耐药;
④ 证实 PfMYST 调控氯喹、阿莫地喹等多种抗疟药的敏感性。
研究核心亮点
这篇研究的核心突破的是“首次打通表观遗传与遗传耐药通路”,5 大关键发现直击核心:
1. 关键因子:PfMYST 与 RS 表型强关联,独立于 PfK13 突变
团队对 30 株临床分离株和 43 株亚克隆菌株进行系统分析,在 10 种组蛋白乙酰转移酶(HATs)中,仅 PfMYST 的表达量与 RS 表型呈显著负相关(图 1d):
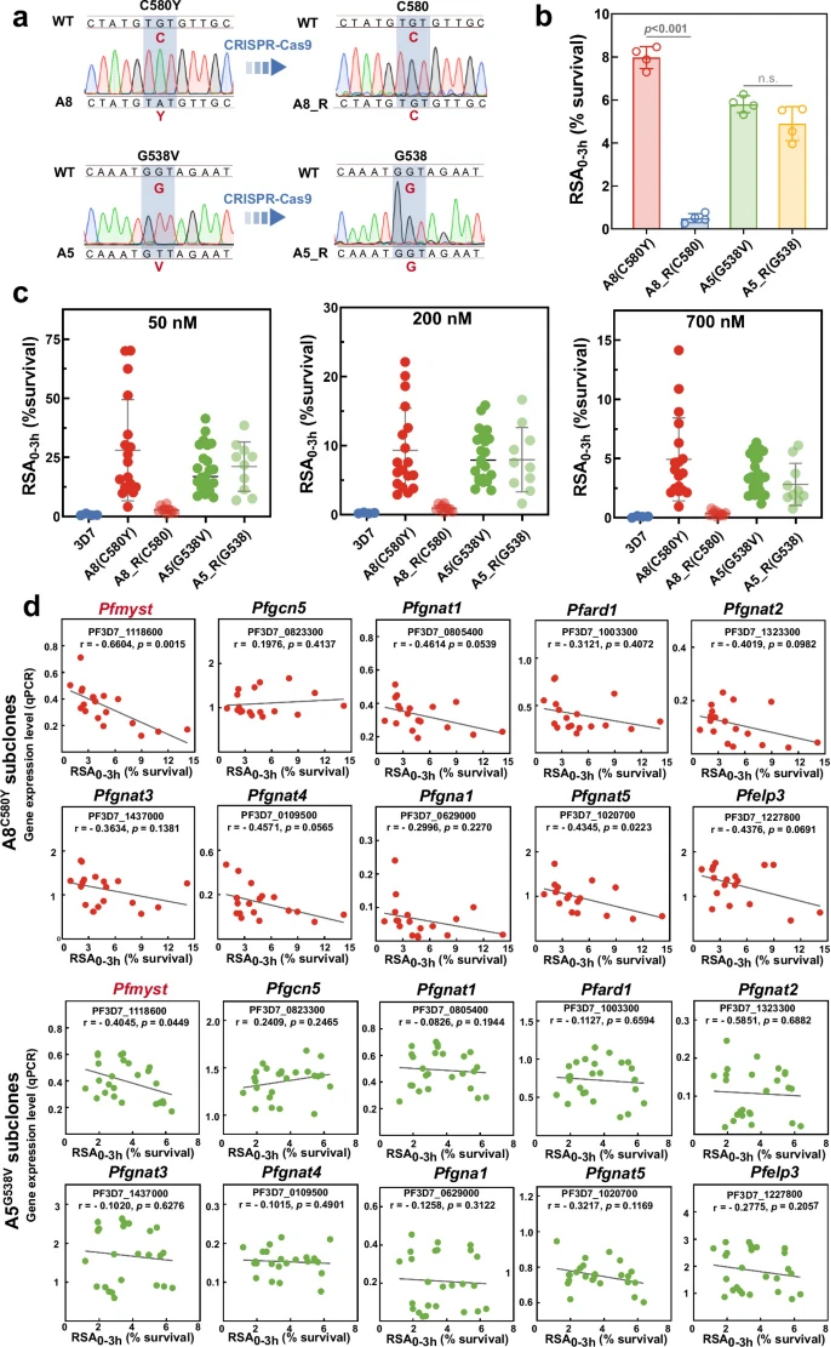
图1
PfMYST 表达越低,RS 率越高(50nM DHA 处理下,相关系数 r=0.53,P=0.0008);
该关联在 PfK13 野生型、C580Y 突变株、G538V 突变株中均成立,证实其独立于 PfK13 的调控作用(图 2a)。
2. 表型与代谢:PfMYST 敲低诱导环期延迟 + 代谢静止
通过 CRISPR/Cas9 构建 PfMYST 敲低(PfM-KD)菌株,验证其功能(图 2b-e):
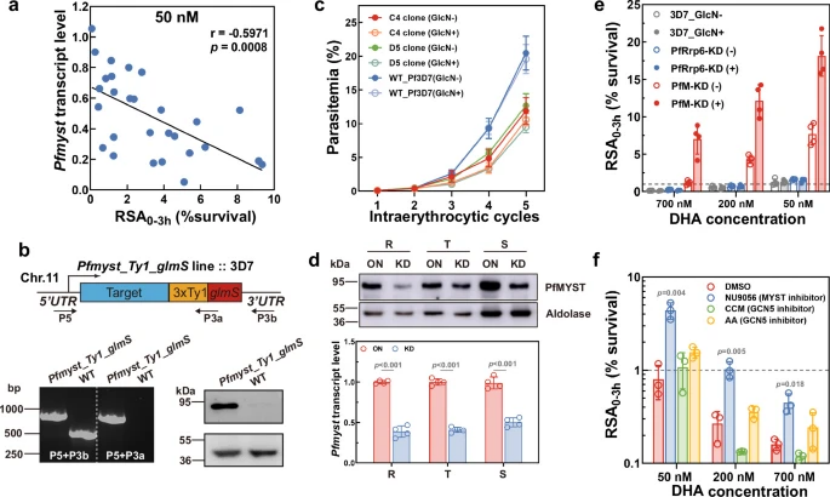
图2
耐药表型:PfMYST 敲低后,RS 率显著升高(700nM DHA 处理下从 1.1% 升至 7.9%),且环状体发育延迟约 6 小时,与 PfK13 突变株表型一致(图 3a-c);
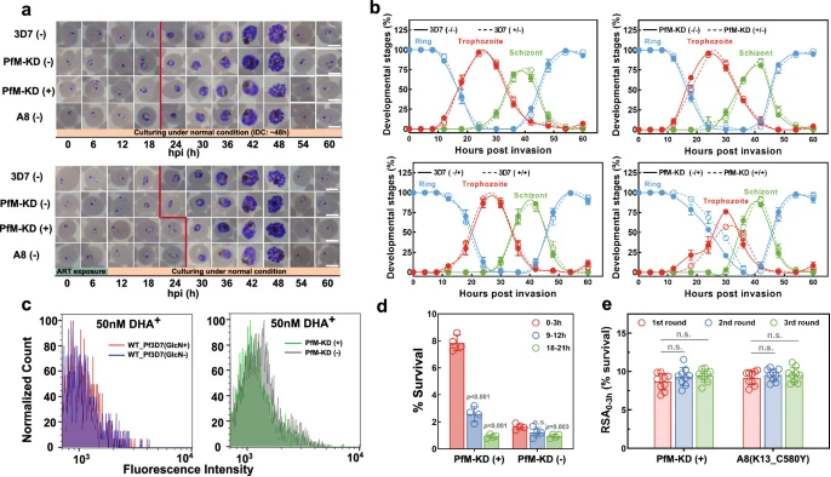
图3
代谢特征:靶向代谢组学显示,PfM-KD 菌株呈现 “代谢静止” 状态 —— 糖酵解和戊糖磷酸途径中间产物升高,与 PfK13 突变株的三羧酸循环(TCA)异常形成互补,共同支撑环期存活(图 4c);
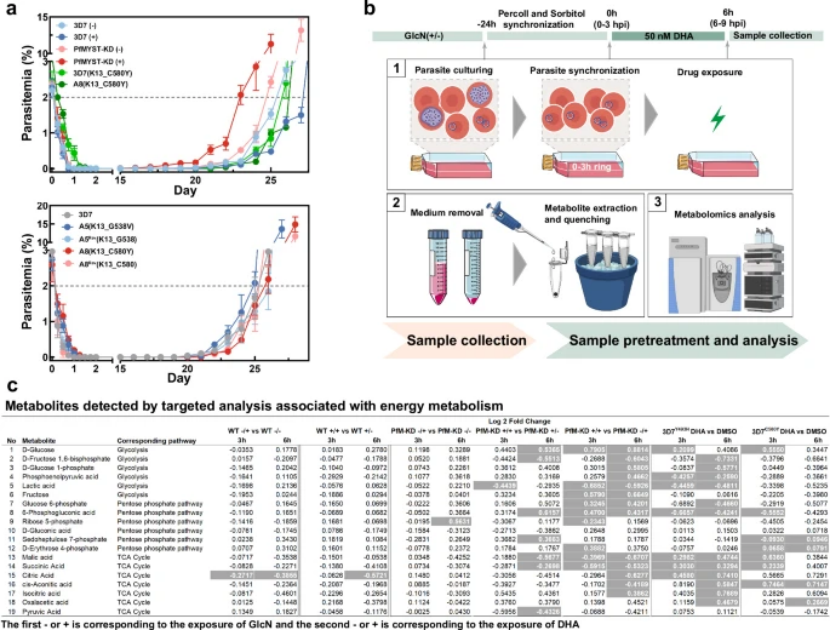
图4
化学验证:PfMYST 特异性抑制剂 NU9056 处理后,RS 率显著升高,而 PfGCN5 抑制剂无此效果,证实 PfMYST 的特异性调控作用(图 2f)。
3. 调控网络:多组学鉴定 46 个靶基因,与 PfK13 通路交叉
结合单细胞 RNA-seq、ChIP-seq 和 CRISPR 功能验证,解析 PfMYST 的调控网络(图 5a-h):
ChIP-seq 证实:PfMYST 通过调控 H4K5ac、H4K8ac 组蛋白修饰,靶向结合环期关键基因的启动子区域;
单细胞 RNA-seq:筛选出 46 个 “PfMYST 靶基因”,其中 21 个与 PfK13 靶基因重叠(占比 46%),涉及细胞周期、内吞作用、应激响应等核心通路(图 5g);
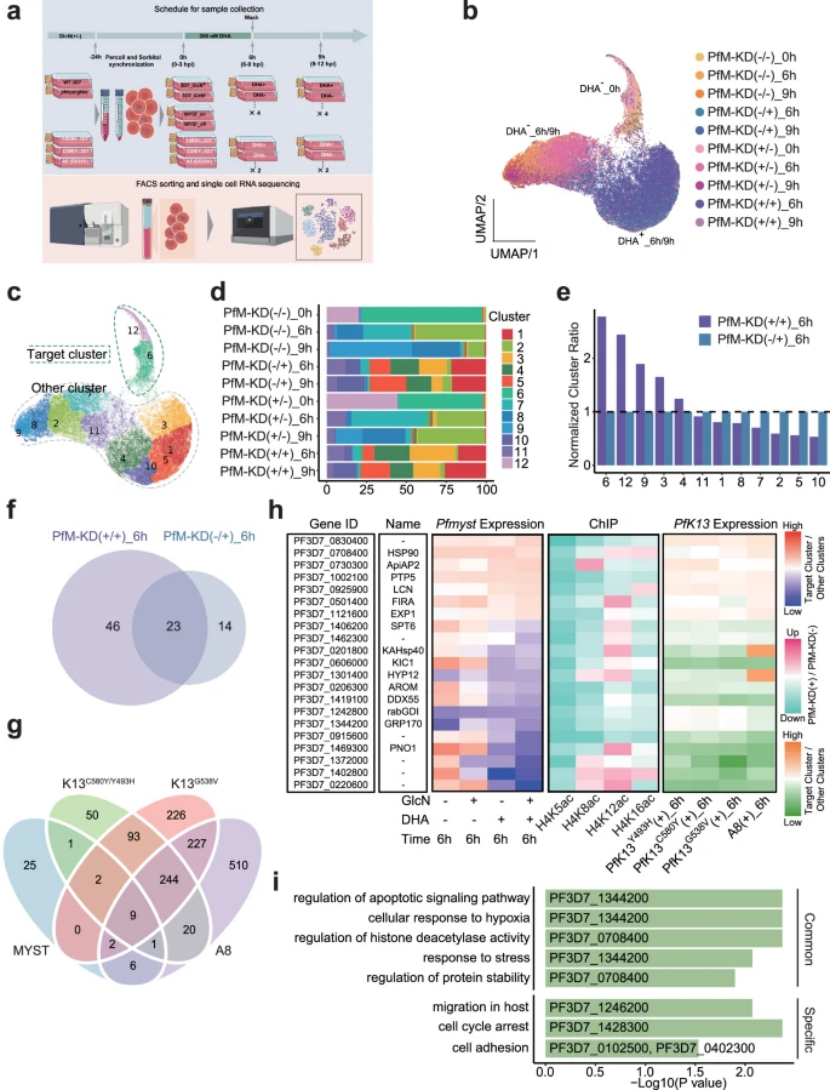
图5
通路差异:PfMYST 侧重表观遗传调控,PfK13 侧重血红蛋白内吞,最终通过不同途径共同导致环期存活和感染复发(图 7)。
4. 功能验证:6 个靶基因敲低增强耐药,2 个加速复发
对 27 个候选靶基因进行遗传操作(过表达、敲除、敲低),发现(图 6a-d):
敲低 KAHRP、2G4、DDX5、PHISTa/b、GTPase1 等 6 个基因,RS 率显著升高;
敲低 PHISTb 和 2G4 后,体外复发时间缩短 2-4 天,直接证实其在耐药复发中的关键作用。
5. 跨界影响:调控多种抗疟药的敏感性
PfMYST 的调控作用并非局限于青蒿素,还影响其他常用抗疟药的 RS 率(图 6e-f):
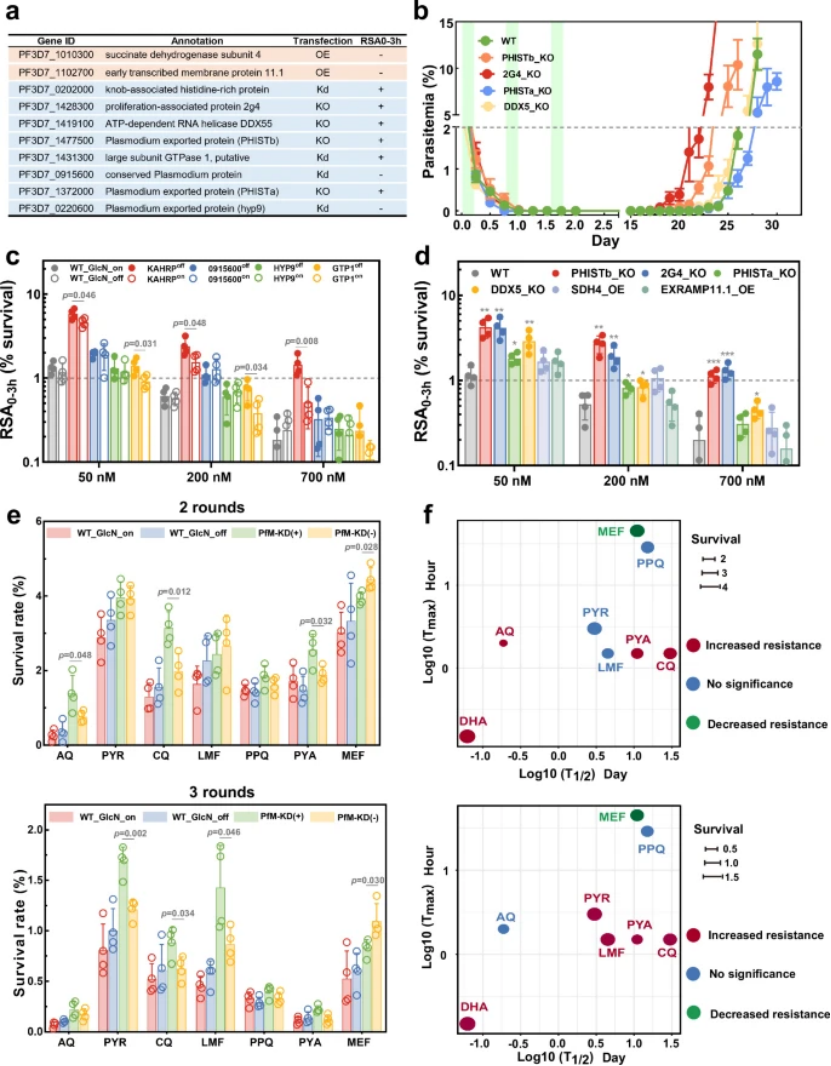
图6
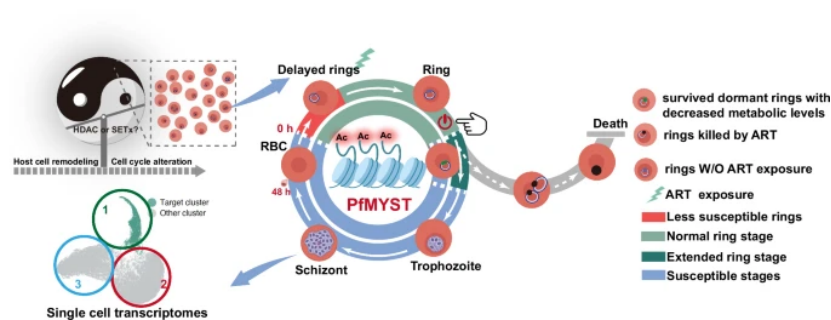
图7
敏感性增强(RS 率升高):氯喹(CQ)、阿莫地喹(AQ)、乙胺嘧啶(PYR)、咯萘啶(PYA);
无显著影响:lumefantrine(LMF)、甲氟喹(MEF)、哌喹(PPQ);
防控提示:PfMYST 介导的表观遗传耐药可能引发 “交叉耐药”,为联合用药组合选择提供重要预警。
临床 / 防控价值:
新药靶点:PfMYST 可作为抗疟新药开发的核心靶点,通过开发其激活剂或抑制下游通路,逆转表观遗传耐药;
联合用药优化:避免将 PfMYST 调控敏感的药物(如氯喹)与青蒿素联用,降低交叉耐药风险;
耐药监测升级:将 PfMYST 表达量纳入耐药监测指标,补充 PfK13 突变检测,提升耐药菌株筛查的准确性;
机制拓展:为弓形虫、利什曼原虫等其他寄生虫的表观遗传耐药研究提供可复制的范式。
中、美、法多国联合团队的这项研究,首次阐明了 PfMYST 介导的表观遗传调控在青蒿素耐药中的核心作用,构建了 “PfMYST 下调→H4 乙酰化异常→靶基因表达改变→环期发育延迟 + 代谢静止→RS 表型 + 复发” 的完整机制链(图 7),且与 PfK13 遗传通路形成关键交叉。
这一发现不仅填补了青蒿素耐药的机制空白,更为抗疟防控提供了“靶向干预 + 精准监测 + 用药优化” 的三维解决方案,有望延缓耐药扩散,巩固青蒿素类药物的临床价值。
原文DOI:10.1038/s41467-025-62479-2
专注期刊投稿、发表十年,任何投稿、写作难题欢迎咨询!

PAPER INFORMATION

快速预审、投刊前指导、专业学术评审,对文章进行评价

校对编辑、深度润色,让稿 件符合学术规范,格式体例等标准
.png)
适用于语句和结构尚需完善和调整的中文文章,确保稿件达到要求
.png)
数据库包括: 期刊、文书籍、会议、预印章、书、百科全书和摘要等

让作者在期刊选择时避免走弯路,缩短稿件被接收的周期

根据目标期刊格式要求对作者文章进行全面的格式修改和调整
.png)
帮助作者将稿件提交至目标期刊投稿系统,降低退稿或拒稿率
.png)
按照您提供的稿件内容,指导完成投稿附信(cover letter)

北京总部:北京市海淀区碧桐园 3 号楼 2 层 211 广州办事处:广州市黄埔区科学城国际企业孵化器 E栋306 联系人:客服 / 18163670350
Copyright © 2022-2024 北京特诺科技有限公司 版权所有 备案/许可证编号为: 京 ICP 备 2023007944 号