
来源:特诺科研
脓毒症作为全球重症医学领域的“致命难题”,死亡率居高不下(约20-30%),其中肝损伤是其最突出的器官并发症之一,严重加剧病情进展,但目前尚无针对性靶向治疗药物。近日,重庆医科大学附属第二医院团队(通讯作者Zuojin Liu等)在《International Journal of Surgery》(IF=10.3,外科领域顶刊,开源可免费获取)发表重磅研究,通过多组学整合、孟德尔随机化(MR)、体内外实验及分子模拟等多种技术,首次锁定TBCB为脓毒症诱导肝损伤的关键治疗靶点,阐明其通过调控代谢重编程和炎症反应驱动疾病进展的核心机制,并筛选出潜在小分子治疗药物,为脓毒症的精准治疗提供了全新策略。

文章信息速览
原标题:Multi-omics analysis identifies TBCB as a therapeutic target in sepsis-induced liver injury
期刊:International Journal of Surgery(IF=10.3,外科领域顶刊,开源获取,无版面费)
关键词:脓毒症、脓毒症诱导肝损伤、TBCB、孟德尔随机化、代谢重编程、治疗靶点、多组学、分子对接、MD模拟
研究背景与临床痛点
1. 治疗困境:脓毒症是感染引发的全身性炎症反应综合征,可导致多器官功能障碍,其中肝脏作为核心免疫代谢器官,极易受损;临床现有治疗仅依赖抗生素、液体复苏等支持性护理,缺乏针对疾病核心机制的靶向药物,患者预后不佳。
2. 机制盲区:脓毒症诱导肝损伤的分子机制复杂,炎症反应过度激活、氧化应激加剧是关键特征,但调控这一过程的核心靶点及上下游通路尚未明确,制约了靶向治疗的发展。
3. 技术机遇:多组学技术与孟德尔随机化(MR)的结合,为精准筛选疾病因果靶点、阐明分子机制提供了强有力的工具,可有效规避传统研究的混杂偏倚,提升研究的可靠性和 translational potential(转化潜力)。
研究核心亮点
这篇IF=10.3顶刊研究的成功关键的在于“多组学整合→MR因果推断→体内外实验验证→机制深挖→小分子筛选”的完整研究闭环,完全贴合高分多组学论文的发文逻辑,每一步均有明确图表支撑,关键结果如下:
1. 第一步:多队列蛋白质组MR,筛选脓毒症候选靶蛋白(图1)
整合5个大型队列(deCODE、UK Biobank、ARIC等,总样本量超10万)的血浆蛋白数量性状位点(cis-pQTL)数据,结合FinnGen R12 sepsis GWAS数据(17133例病例、439048例对照),开展蛋白质组全基因组MR分析。
关键结果:筛选出CRP、APLP2、ERLEC1、TBCB 4个与脓毒症风险呈提示性关联的蛋白( nominal P < 0.05);其中TBCB因与微管动力学密切相关(微管重塑是脓毒症器官损伤的关键机制),且colocalization分析显示其与脓毒症易感位点共享遗传信号(PPH4=0.70,中等程度共定位),被纳入后续验证;PPI网络分析显示,TBCB与APLP2处于脓毒症相关分子网络的关键节点(图1A-C)。
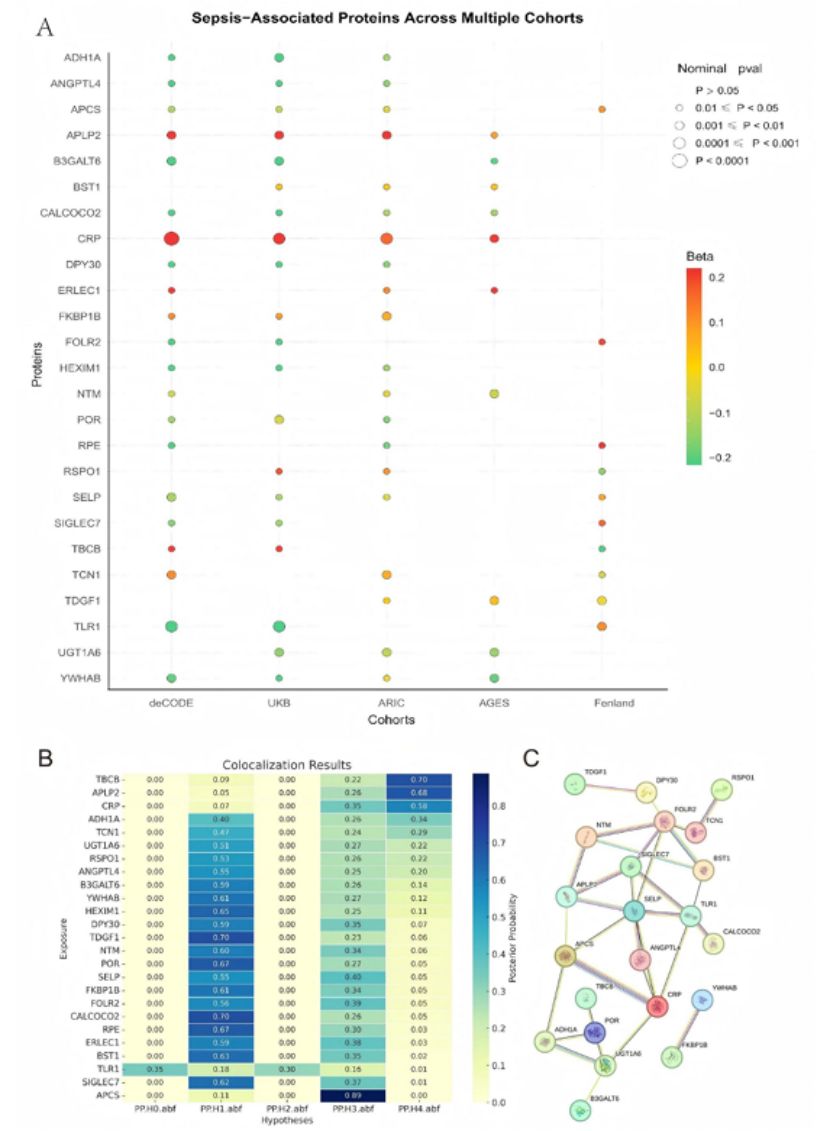
图1
2. 第二步:eQTL-SMR分析,锁定TBCB为核心靶点(图2)
整合eQTLGen(31684例)、GTEx v8(838例供体)的表达数量性状位点(eQTL)数据,与FinnGen、UK Biobank的sepsis GWAS数据进行SMR和HEIDI分析,验证基因水平的关联。
关键结果:仅TBCB显示提示性关联(nominal SMR_P < 0.05,HEIDI_P ≥ 0.05,排除异质性);通路富集分析显示,SMR筛选出的提示性基因显著富集于Toll样受体信号通路、PI3K-Akt信号通路等脓毒症核心病理通路,进一步证实TBCB的生物学相关性(图2A-E)。
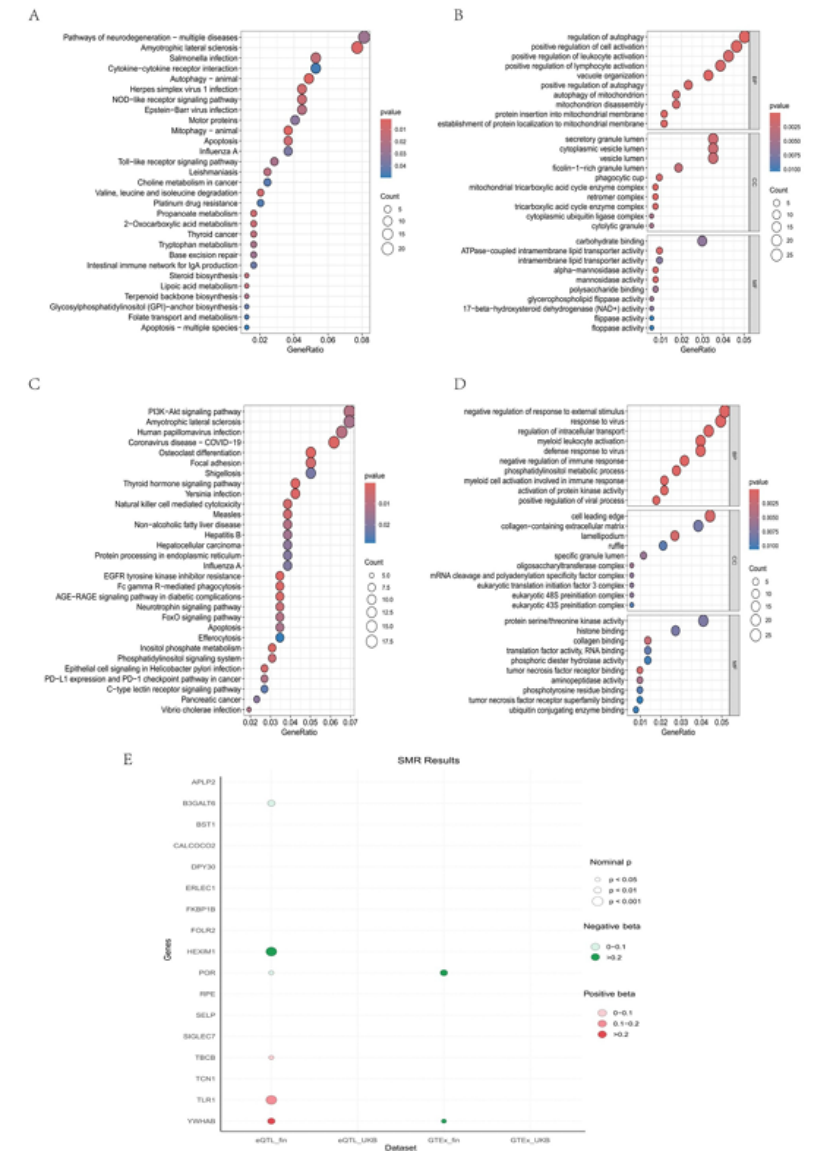
图2
3. 第三步:体内实验验证,TBCB在脓毒症肝损伤中显著上调(图3)
构建两种脓毒症小鼠模型(盲肠结扎穿孔术CLP模型、脂多糖LPS注射模型),设置假手术组、模型组对照,评估肝损伤及TBCB表达水平(图3A)。
关键结果:① 病理层面:H&E染色显示,CLP和LPS模型组小鼠肝组织出现明显肝细胞气球样变、胞质空泡化及坏死,且24h损伤程度较6h更严重(图3B);② 生化层面:模型组小鼠血清ALT、AST水平显著升高,证实肝损伤发生(图3C-D);③ 蛋白层面:Western blot显示,模型组肝组织中TBCB显著上调,而APLP2、ERLEC1无明显变化(图3E-H);④ 定位层面:免疫荧光染色证实,TBCB主要在肝组织巨噬细胞中高表达(图3I-J)。
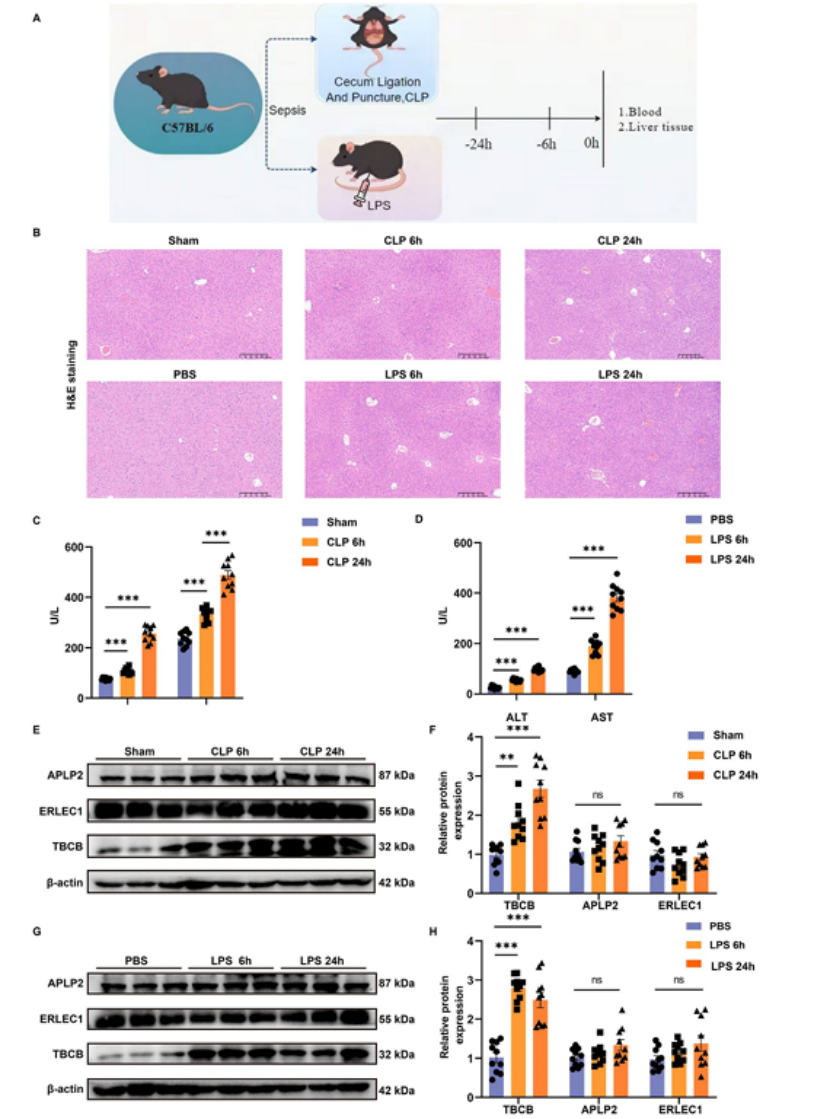
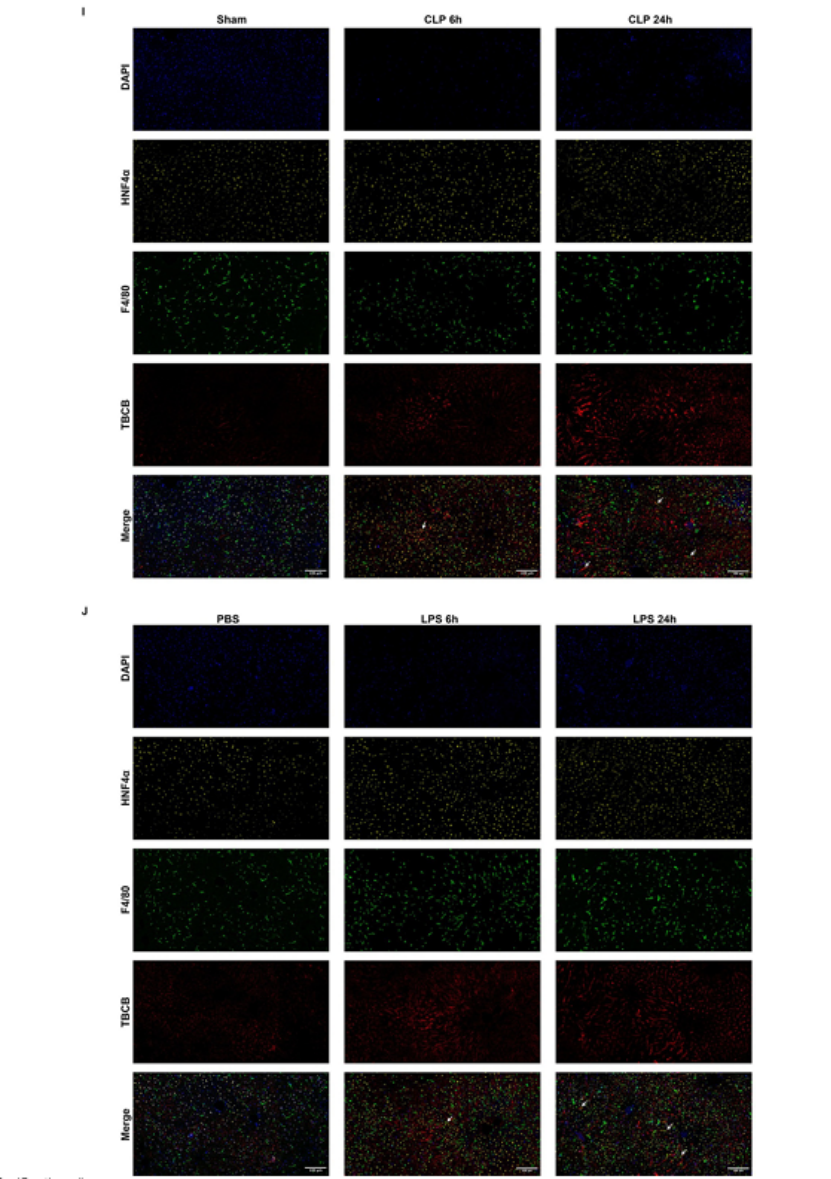
图3
4. 第四步:体外细胞验证,TBCB在炎症环境中特异性上调(图4)
构建体外脓毒症模型:分别用LPS刺激骨髓来源巨噬细胞(BMDMs)、LPS刺激Alpha小鼠肝细胞(AML12),模拟脓毒症炎症环境(图4A)。
关键结果:① BMDMs中:LPS刺激后,TBCB蛋白表达显著上调,12h达到峰值,同时炎症标志物iNOS、TNF-α显著升高(图4B-D);② AML12细胞中:LPS刺激后,TBCB表达无明显变化,提示TBCB的上调主要发生在巨噬细胞中,而非肝细胞(图4E-F)。
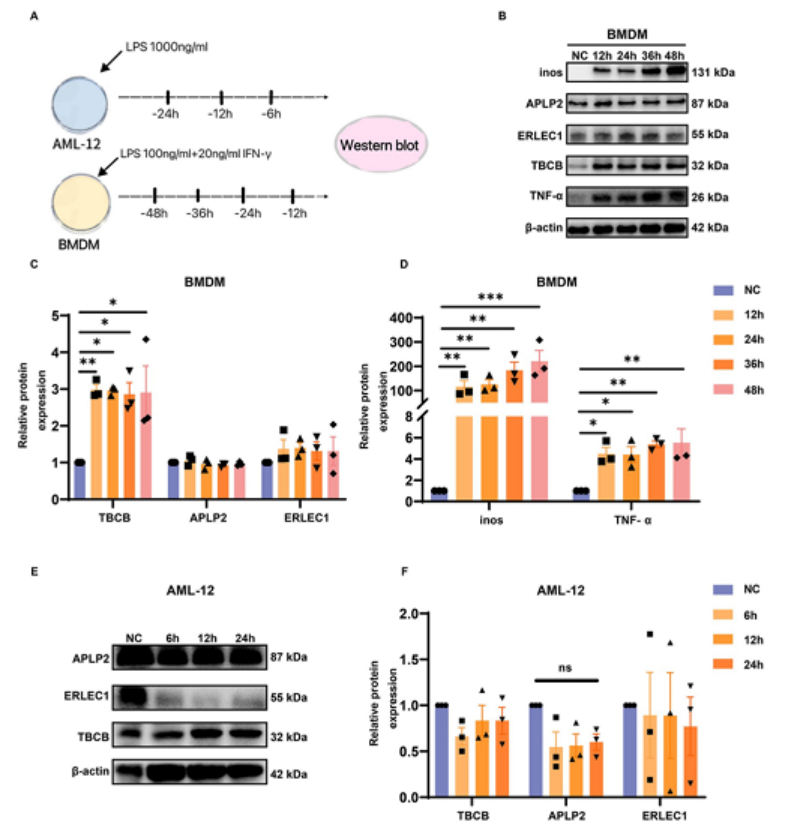
图4
5. 第五步:功能验证,TBCB敲低可显著减轻巨噬细胞炎症(图5)
用siRNA转染BMDMs,敲低TBCB表达(筛选出siTBCB#3敲低效率最高),再用LPS+IFN-γ刺激,检测炎症标志物表达。
关键结果:TBCB敲低后,BMDMs中炎症标志物iNOS、caspase-1、剪切型caspase-1、IL-1β的蛋白水平均显著降低,证实TBCB可促进巨噬细胞炎症反应,敲低TBCB能有效减轻脓毒症相关炎症(图5A-D)。
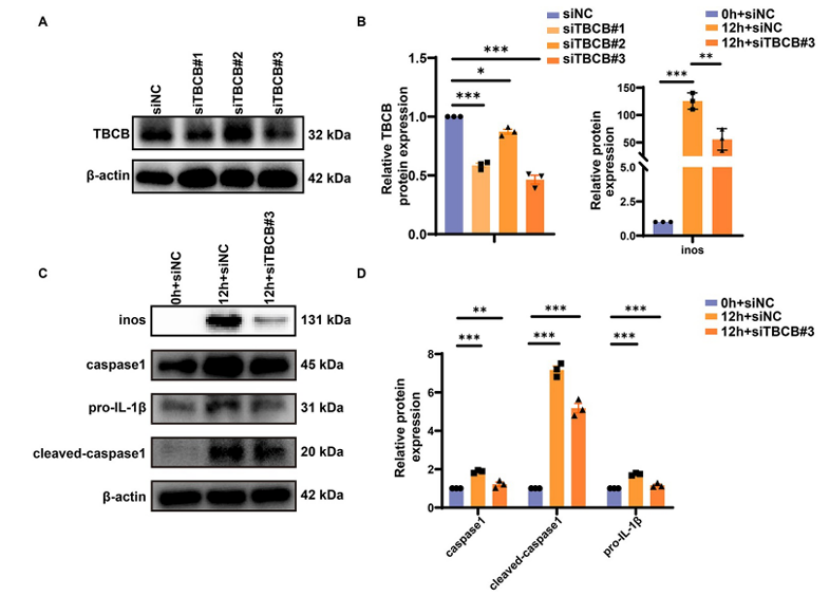
图5
6. 第六步:代谢组MR,揭示TBCB通过代谢重编程介导脓毒症进展(图6)
整合加拿大纵向衰老研究(n=8299)的代谢组GWAS数据,开展代谢组全基因组MR分析,并进行介导MR分析,探索TBCB→代谢物→脓毒症的调控轴。
关键结果:① 筛选出多个与脓毒症风险呈提示性关联的代谢物(图6A);② 通路富集显示,这些代谢物主要富集于精氨酸和尿素循环、谷胱甘肽代谢、胆汁酸/肠道脂质吸收等免疫代谢通路(图6B-D);③ 介导分析显示,TBCB可通过调控下游代谢物影响脓毒症风险,其中stearidonate(18:4n3)的介导比例最高(62.77%),证实代谢重编程是TBCB调控脓毒症进展的核心机制之一。
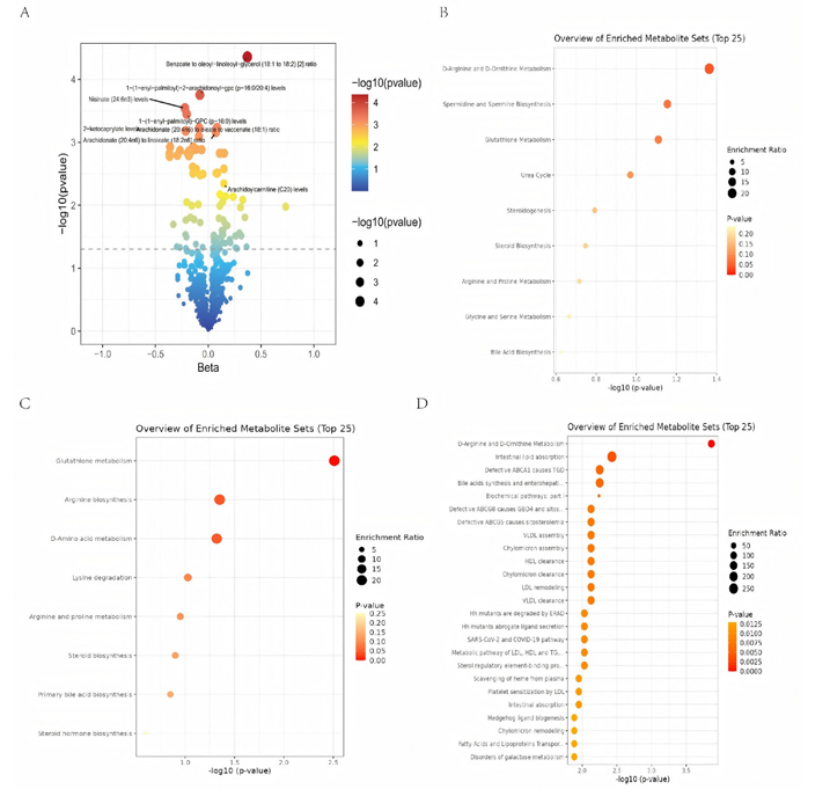
图6
7. 第七步:分子对接+MD模拟,筛选TBCB潜在小分子药物(图7)
以TBCB蛋白(AlphaFold结构)为靶点,筛选PubChem数据库中的小分子化合物,通过AutoDock Vina进行分子对接,再用GROMACS开展100 ns MD模拟,评估蛋白-配体复合物的稳定性。
关键结果:筛选出3种tocopherol类小分子(A-tocopherol、tocophero、tocopherol),MD模拟显示,这3种小分子与TBCB形成的复合物均具有良好稳定性(RMSD在60-70 ns后趋于平稳,Rg、SASA降低并 plateau,氢键稳定,RMSF值低),提示其可能成为TBCB靶向治疗的潜在药物(图7A-E)。
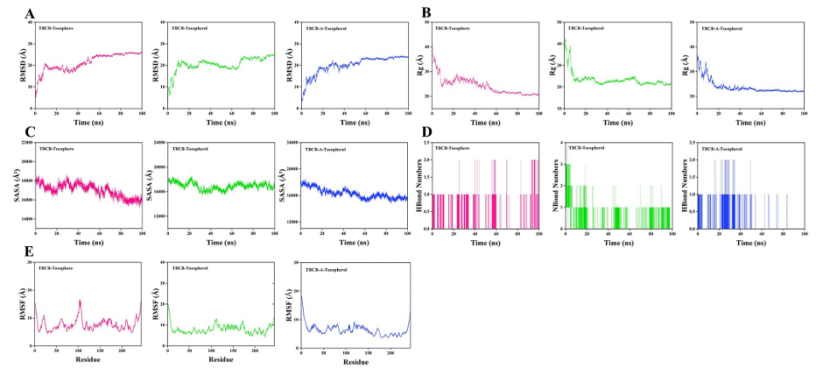
图7
总结:完整研究闭环,为脓毒症治疗+高分发文提供双重参考
重庆医科大学附属第二医院团队的这项研究,完美复刻了高分多组学论文的“筛选-验证-机制-转化”发文逻辑,通过“多队列蛋白质组MR→eQTL-SMR→体内模型→体外细胞→功能验证→代谢组机制→小分子筛选”的7步流程,明确了TBCB是脓毒症诱导肝损伤的因果性治疗靶点,阐明了其“调控巨噬细胞炎症+代谢重编程”的双重机制,并筛选出潜在小分子药物,研究可靠性强、转化价值高,最终成功发表于IF=10.3的顶刊,且开源可获取,无版面费负担。
对于临床医生而言,这不仅为脓毒症的靶向治疗提供了新的突破口,更提供了一套可直接借鉴的高分多组学论文发文模板——无需复杂的临床样本收集,依托公共数据库(GWAS、pQTL、eQTL等),结合简单的体内外验证和生物信息学分析,即可快速产出高质量成果。
原文DOI: 10.1097/JS9.0000000000004770
专注期刊投稿、发表十年,任何投稿、写作难题欢迎咨询!

PAPER INFORMATION

快速预审、投刊前指导、专业学术评审,对文章进行评价

校对编辑、深度润色,让稿 件符合学术规范,格式体例等标准
.png)
适用于语句和结构尚需完善和调整的中文文章,确保稿件达到要求
.png)
数据库包括: 期刊、文书籍、会议、预印章、书、百科全书和摘要等

让作者在期刊选择时避免走弯路,缩短稿件被接收的周期

根据目标期刊格式要求对作者文章进行全面的格式修改和调整
.png)
帮助作者将稿件提交至目标期刊投稿系统,降低退稿或拒稿率
.png)
按照您提供的稿件内容,指导完成投稿附信(cover letter)

北京总部:北京市海淀区碧桐园 3 号楼 2 层 211 广州办事处:广州市黄埔区科学城国际企业孵化器 E栋306 联系人:客服 / 18163670350
Copyright © 2022-2024 北京特诺科技有限公司 版权所有 备案/许可证编号为: 京 ICP 备 2023007944 号