
来源:特诺科研
帕金森病(PD)是全球第二大神经退行性疾病,GBA1 杂合致病性变异是其最显著的遗传风险因素,而 GBA1 相关帕金森病(GBA1-PD)发病机制尚未完全阐明,且缺乏临床验证的早期诊断标志物,临床诊疗面临巨大挑战。
近日,大连医科大学附属第一医院联合美国 NIH、上海健康医学院团队在神经退行性疾病领域顶刊《Molecular Neurodegeneration》(IF=17.5,开源获取 0 版面费)发表重磅综述:通过整合基因组、转录组、蛋白质组、脂质组 多组学技术,结合单细胞测序、神经影像特征及体内外实验验证,系统解析 GBA1-PD 的临床表型、分子发病机制,筛选出多组学来源的分型生物标志物,同时搭建了针对性的精准诊断和靶向治疗框架,为破解帕金森病异质性难题提供了全新的研究思路和实践方向。

文章信息速览
原标题:Multi-omics insights into GBA1-associated Parkinson’s disease: interplay of genomics, transcriptomics, proteomics, and lipidomics
期刊:Molecular Neurodegeneration(IF=17.5)
关键词:GBA1 相关帕金森病、临床表型、多组学、代谢紊乱、生物标志物、基因组、转录组、蛋白质组、脂质组、神经影像、GCase、α- 突触核蛋白
研究背景与临床痛点
疾病负担重,遗传机制待深挖:PD 呈年龄依赖性高发,65 岁以上人群年发病率达 108-212/10 万,GBA1 杂合突变是其最主要遗传风险因素,但 GBA1 功能异常介导 PD 发生的精准分子机制尚未阐明;
临床鉴别难,表型特征不明确:GBA1-PD 与特发性 PD(iPD)存在大量临床重叠,且不同 GBA1 突变亚型的临床表型差异显著,缺乏明确的分型依据,导致鉴别诊断困难;
标志物缺失,早期诊断无依据:目前 GBA1-PD 的识别仅依赖基因筛查,缺乏临床验证的、微创的早期诊断生物标志物,无法实现前驱期检测和风险分层;
治疗获益有限,精准方案待开发:GBA1-PD 患者发病更早、进展更快,对深部脑刺激等传统治疗获益有限,且无针对 GBA1-PD 病理特征的靶向治疗策略;
多组学应用散,整合分析不足:多组学技术为解析 PD 异质性提供了工具,但针对 GBA1-PD 的多组学研究多为单一维度,缺乏基因组、转录组、蛋白组、脂质组的系统整合,且未与临床表型、神经影像有效结合。
研究核心亮点
这篇 IF=17.5 顶刊综述的成功,为临床医生和科研人员发表多组学相关论文提供了可直接复制的经典行文与研究设计范式:从“基因分型 - 临床表型” 精准关联切入,以核心分子功能异常 为机制主线,整合多维度组学技术筛选分子标志物,结合影像学实现多维度验证,最终落地精准诊断 + 靶向治疗 临床框架,全程以 图1-图4 核心图表直观支撑结论,让多组学数据不再是单纯堆砌,而是紧密服务于临床和机制研究。以下结合研究内容和图表,拆解多组学论文的发文关键步骤:
第一步:锚定核心遗传靶点,建立基因分型与临床表型的量化关联(图1)—— 多组学研究的临床基础
多组学研究需先明确研究的核心遗传靶点,梳理其基因结构和变异特征,再建立基因型 - 临床表型 的精准、量化关联,用可视化图表直观展示,为后续组学分析奠定临床锚点。
核心遗传靶点解析:明确 GBA1 基因定位于 1q21,含 11 个外显子,编码溶酶体水解酶 GCase,其假基因 GBA1P 因高同源性易导致测序误差,同时梳理出全球已发现的 400 余种 GBA1 变异,其中错义变异最常见,且变异存在显著种族异质性(如亚裔以 L444P 为主,德系犹太人以 N370S 为主);
基因分型标准建立:根据对戈谢病(GD)的严重影响,将 GBA1 变异分为 5 类(严重 / 复杂 / 轻度 / 风险 / 未知),不同亚型的 PD 患病风险、外显率差异显著;
基因型 - 表型量化关联:图1 清晰展示 GBA1-PD 与 iPD 的临床表型差异,且突变严重程度与 PD 患病风险(OR 值)、发病年龄、症状进展速度直接相关:严重变异(L444P 等)OR 值达 6.4-30.4,发病年龄比轻度变异早 5 年,同时 GBA1-PD 存在性别差异(严重变异更多影响女性,轻度 / 风险变异更多见于男性);
临床表型特征明确:系统总结 GBA1-PD 的核心临床特征 —— 发病年龄平均早 5 年、运动 / 非运动症状进展更快、路易体痴呆风险更高、死亡率更高,且深部脑刺激治疗获益有限。
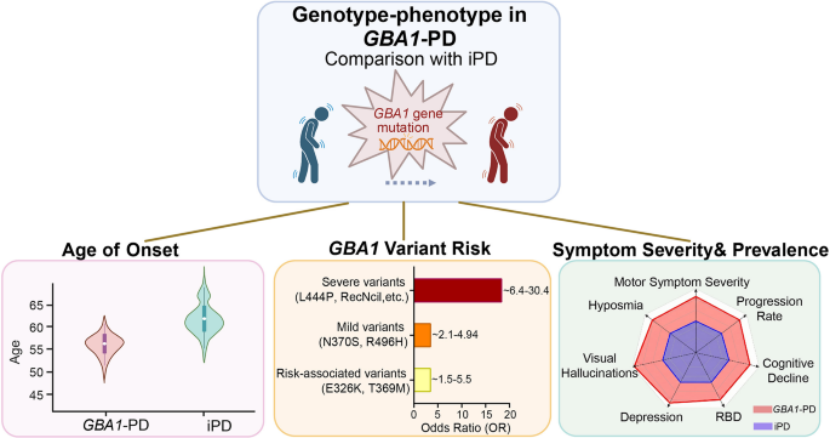
图1
第二步:深挖核心分子功能异常机制,构建病理级联反应通路(图2)—— 多组学研究的逻辑主线
多组学研究并非单纯的组学数据堆砌,需先明确核心分子的功能异常机制,构建 “功能异常 - 病理级联反应” 的完整通路框架,后续再用多组学数据验证、补充和完善该通路,让组学数据服务于机制解析。
核心分子功能定位:明确 GCase 不仅调控鞘脂代谢,还是自噬 - 溶酶体通路(ALP)的关键调控蛋白,为机制分析奠定基础;
双假说解析核心机制:提出 GBA1 突变介导疾病的两大核心假说 ——功能丧失假说(GCase 活性降低,底物 GlcCer/GlcSph 蓄积,稳定毒性 α- 突触核蛋白寡聚体促进其聚集)、毒性获得假说(错误折叠的 GCase 在内质网蓄积引发 ER 应激,抑制分子伴侣介导的自噬,进一步阻碍 α- 突触核蛋白降解);
构建双向正反馈环路:图2 清晰展示 GCase 功能异常与 α- 突触核蛋白聚集形成双向正反馈病理环路,这是 GBA1-PD 的核心发病机制;
拓展下游病理级联反应:核心环路进一步触发下游线粒体功能障碍(抑制线粒体自噬、破坏复合物 I 完整性)、神经炎症等病理事件,最终导致多巴胺能神经元变性死亡,形成完整的病理级联反应通路。
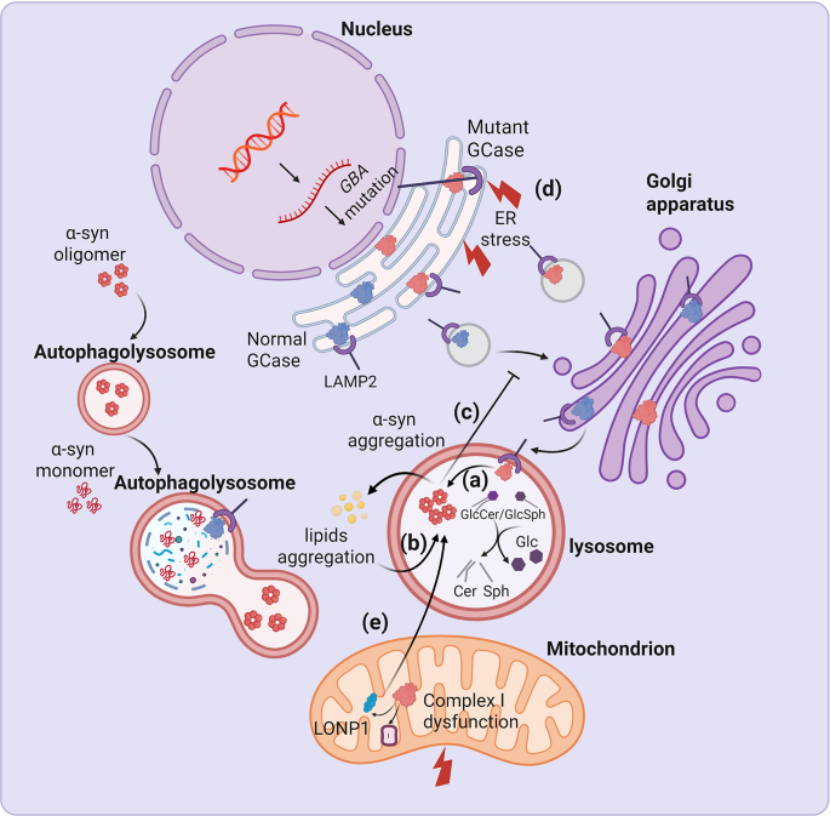
图2
第三步:整合多组学技术,筛选跨维度分子特征与候选标志物(图3)—— 多组学研究的核心技术环节
开展多组学研究时,需根据疾病机制选择匹配的组学技术,采用外周样本(血、CSF)+ 中枢样本(脑组织、特异性神经元) 结合的策略,筛选出跨组学的核心分子特征和候选标志物,并通过图表整合多组学结果,让数据更清晰、更有说服力。
基因组:明确 PD 相关 GBA1 变异主要集中在 8-10 号外显子,筛选出 L444P、N370S、E326K 等核心风险变异,建立变异分型标准和在线数据库,为基因筛查提供依据;
转录组:通过外周血单核细胞、巨噬细胞及 iPSC 来源多巴胺能神经元的转录组分析,发现 SNCA(α- 突触核蛋白编码基因)上调、多巴胺能神经元身份基因(JUNB/EGR1/NR4A2)下调、锌代谢 / 衰老相关通路紊乱等核心特征,且 DUSP1/COLEC12 等基因可区分症状性 GBA1-PD 与无症状携带者;
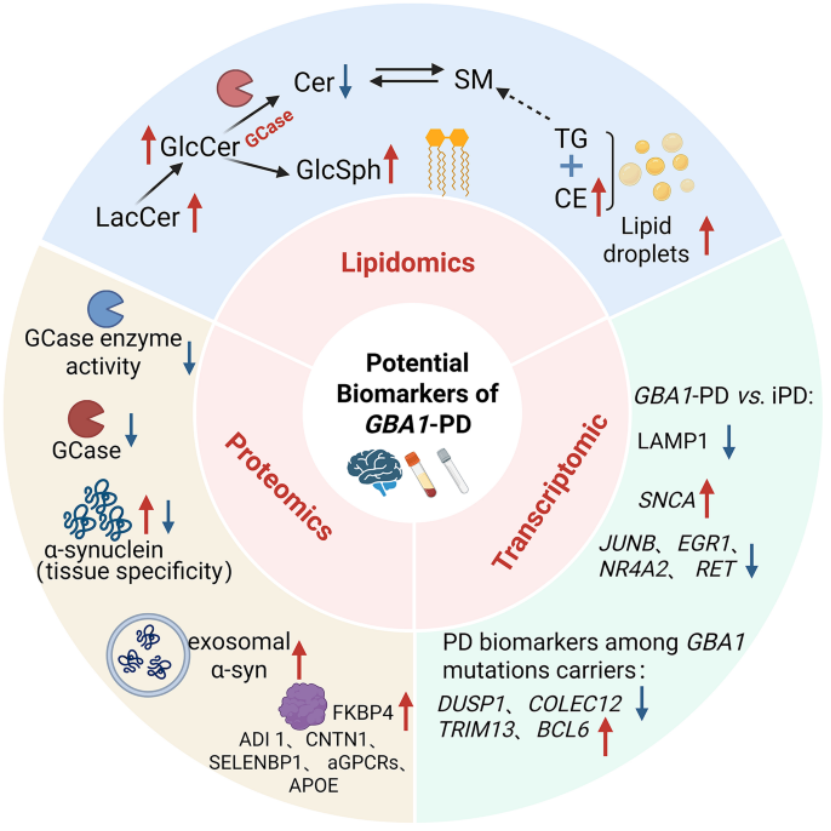
图3
蛋白质组:发现 GCase 活性在 GBA1-PD 患者血、CSF、脑组织中均显著降低,且与突变严重程度相关;CSF 中 CNTN1、SELENBP1、aGPCRs、APOE 下调、FKBP4 上调为潜在蛋白标志物;同时明确外泌体相关 α- 突触核蛋白寡聚体参与病理传播;
脂质组:发现 GCase 功能异常导致鞘脂代谢紊乱(GlcCer/GlcSph 蓄积、神经酰胺亚型失衡)、脂滴蓄积、溶酶体胆固醇异常,且 CSF 中 GlcCer/GalCer 比值、GlcCer/SM 比值为潜在脂质标志物;
多组学整合:图3 将基因组、转录组、蛋白质组、脂质组的核心发现进行整合,明确了 GBA1-PD 的多组学分子特征和候选生物标志物,为疾病分型和早期诊断提供了多维度依据。
第四步:结合神经影像技术,实现“组学 - 影像 - 临床” 三重验证 —— 多组学研究的临床价值提升
对于神经疾病的多组学研究,结合结构 / 功能 / 分子神经影像技术 是提升研究临床转化价值的关键,可实现分子水平(组学)与组织 / 器官水平(影像)、临床表型的三重验证,让研究结果更贴近临床应用。
结构影像:结构 MRI 发现 GBA1-PD 患者颞顶枕叶皮质变薄速度更快,扩散张量成像(DTI)显示皮质脊髓束等白质微结构异常,且白质纤维密度与 GCase 活性、临床症状严重程度相关;
功能影像:GBA1-PD 患者默认模式网络节点中心性升高、纹状体与顶枕叶皮质功能连接降低,且功能网络异常与疲劳、认知下降相关;
分子影像:PET/SPECT 显示 GBA1-PD 患者黑质 - 纹状体多巴胺能神经末梢丢失更显著,且存在顶枕叶低灌注,与路易体痴呆的影像特征一致;
全身影像:心脏核素显像证实 GBA1-PD 患者存在心脏交感神经去神经化,PET 显示胆碱能神经变性更广泛,补充了全身系统的病理证据。
第五步:基于多组学与机制发现,搭建精准诊疗框架(图4)—— 多组学研究的最终落脚点
顶刊对多组学研究的核心要求是有临床应用价值,因此研究需基于组学发现的分子特征和病理机制,挖掘潜在治疗靶点,提出针对性的诊断和治疗策略,让多组学研究落地临床,这也是医生发多组学论文的关键。
精准诊断框架:提出结合GBA1 基因分型 + 多组学生物标志物(GCase 活性、脂质比值、蛋白标志物)+ 神经影像特征 的 GBA1-PD 精准诊断和风险分层策略,实现前驱期检测和亚型鉴别;
靶向治疗策略:图4 系统梳理了基于 GBA1-PD 病理机制的治疗策略,分为两大类:①GCase 中心策略(基因治疗恢复 GBA1 功能、小分子伴侣改善 GCase 折叠、酶替代治疗补充 GCase、底物减少治疗降低 GlcCer 蓄积);②下游病理通路靶向策略(如抑制硬脂酰辅酶 A 去饱和酶 SCD 改善脂质代谢和 α- 突触核蛋白聚集);
临床转化方向:提出需建立标准化的组学检测流程,结合患者 GBA1 突变类型和严重程度进行精准分层,为后续临床研究和药物开发提供框架。
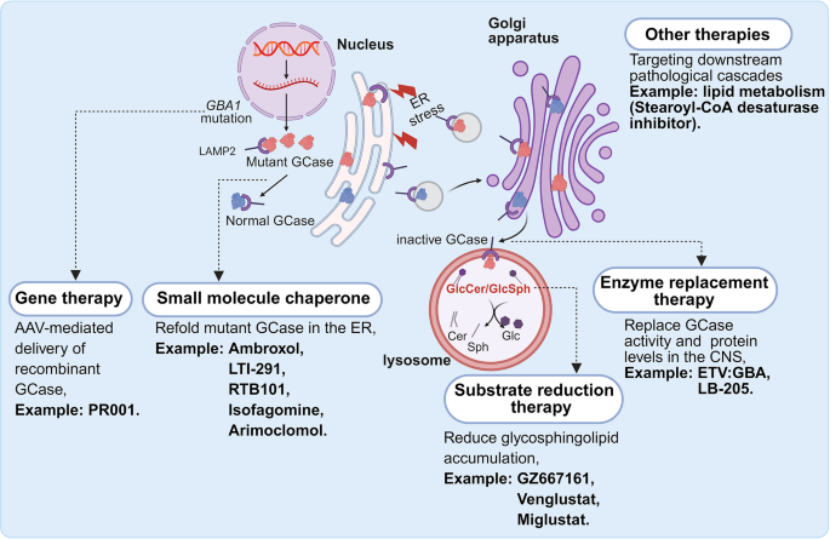
图4
总结:多组学论文发文的核心逻辑—— 从临床痛点出发,落地临床应用
大连医科大学附属第一医院 / 乐卫东团队的这篇 IF=17.5 顶刊综述,为临床医生和科研人员发表多组学相关论文提供了可复制的核心逻辑:从临床实际痛点出发,以核心分子功能异常为机制主线,整合多维度组学技术筛选分子标志物,结合影像学实现多维度验证,最终落地精准诊断和靶向治疗的临床框架。
整个研究过程中,核心图表(图1-图4)分别承担了基因型 - 表型关联、病理机制展示、治疗策略梳理、多组学结果整合 的功能,让研究逻辑层层递进,多组学数据与临床、机制紧密结合,而非单纯的数据分析和堆砌。这也是该研究能在神经退行性疾病顶刊发表的关键,为后续多组学研究的设计和论文撰写提供了经典范例。
原文DOI: 10.1186/s13024-026-00931-7
专注期刊投稿、发表十年,任何投稿、写作难题欢迎咨询!

PAPER INFORMATION

快速预审、投刊前指导、专业学术评审,对文章进行评价

校对编辑、深度润色,让稿 件符合学术规范,格式体例等标准
.png)
适用于语句和结构尚需完善和调整的中文文章,确保稿件达到要求
.png)
数据库包括: 期刊、文书籍、会议、预印章、书、百科全书和摘要等

让作者在期刊选择时避免走弯路,缩短稿件被接收的周期

根据目标期刊格式要求对作者文章进行全面的格式修改和调整
.png)
帮助作者将稿件提交至目标期刊投稿系统,降低退稿或拒稿率
.png)
按照您提供的稿件内容,指导完成投稿附信(cover letter)

北京总部:北京市海淀区碧桐园 3 号楼 2 层 211 广州办事处:广州市黄埔区科学城国际企业孵化器 E栋306 联系人:客服 / 18163670350
Copyright © 2022-2024 北京特诺科技有限公司 版权所有 备案/许可证编号为: 京 ICP 备 2023007944 号