
来源:特诺科研
肿瘤相关巨噬细胞(TAMs)是肿瘤微环境中功能异质的核心群体,分为促瘤和抑瘤亚型,可由外周单核细胞或组织驻留巨噬细胞(TRMs)分化而来,但其分化背后的表观遗传调控机制长期未被阐明,成为肿瘤免疫治疗的研究难点。
近日,天津医科大学 团队在Journal of Advanced Research(IF=13.0)发表重磅泛癌研究:通过整合单细胞 ATAC-seq、scRNA-seq 等多组学技术,结合小鼠骨髓源巨噬细胞多组学分析、人源细胞体外 CRISPR 功能验证,首次绘制了人类 TAMs 的泛癌表观遗传图谱,揭示了外周单核细胞、TRMs 分别分化为 SPP1+、C1QC + 促瘤 TAM 的独特表观轨迹,证实增强子驱动的 Pol II 暂停调控而非启动子可及性,是促瘤 TAM 重编程的核心机制,且促瘤 TAM 超级增强子特征可作为泛癌预后生物标志物,为靶向 TAMs 的肿瘤免疫治疗提供全新表观遗传靶点!

文章信息速览
原标题:Pan-cancer epigenetic landscape of human tumor-associated macrophages reveals crucial enhancers governing their heterogenous formation by Pol II pausing modulation
期刊:Journal of Advanced Research(IF=13.0)
关键词:肿瘤相关巨噬细胞、增强子、RNA 聚合酶 II 暂停、泛癌、表观遗传、单细胞测序、超级增强子、预后标志物
研究背景与临床痛点
分型困境:TAMs 存在显著功能异质性,促瘤亚型可来源于外周单核细胞或 TRMs,但两种来源的细胞分化为特定 TAM 亚型的表观调控通路尚未明确;
机制盲区:增强子是调控细胞特异性基因表达的关键,但促瘤 TAM 特异性增强子、转录因子如何驱动不同来源巨噬细胞的异质分化,其调控方式(启动子可及性 / Pol II 暂停)仍属未知;
临床短板:靶向 TAMs 是肿瘤免疫治疗的重要方向,但缺乏基于表观遗传机制的特异性靶点,且尚无可靠的 TAMs 相关泛癌预后标志物;
技术缺口:缺乏对人类 TAMs 的泛癌水平单细胞表观遗传分析,难以揭示不同癌种中 TAMs 调控的共性与特异性规律。
研究核心亮点
这篇 IF=13.0 顶刊研究的成功,核心在于以泛癌为视角、单细胞多组学为核心、实验验证为支撑,从表观轨迹→关键调控因子→核心机制→临床标志物 层层递进解析 TAMs 异质形成,6 大核心研究步骤贴合顶刊发文逻辑,关键图表直观支撑核心结论,为临床医生开展多组学研究提供了可复制的经典范式:
第一步:泛癌单细胞表观测序,绘制健康 / 肿瘤髓系细胞表观图谱,锁定核心促瘤 TAM 亚型(图 1)
数据基础:收集 208 个单细胞 ATAC-seq 样本,涵盖健康成人 / 胎儿组织、癌前病变、结直肠癌 / 肾透明细胞癌 / 卵巢癌 / 子宫内膜癌等泛癌组织髓系细胞,整合分析后聚类得到 14 个髓系细胞亚群,含 5 种巨噬细胞亚型(图 1A-C);
核心分型:发现 Macro-SPP1 主要富集于癌组织、Macro-C1QC 富集于癌前病变,Macro-LYVE1/MSR1 为健康组织 TRMs,且 Macro-SPP1 高表达 IL10、SPP1 等抑炎促瘤基因,富集伤口愈合、缺氧、血管生成通路(图 1D-G);
调控初筛:通过基序富集分析,发现 Macro-SPP1 激活的顺式调控元件富集 NF-κB、bZIP 家族转录因子基序,Macro-C1QC 富集 bHLH、C2H2 锌指因子基序(图 1H),为后续筛选关键转录因子奠定基础。
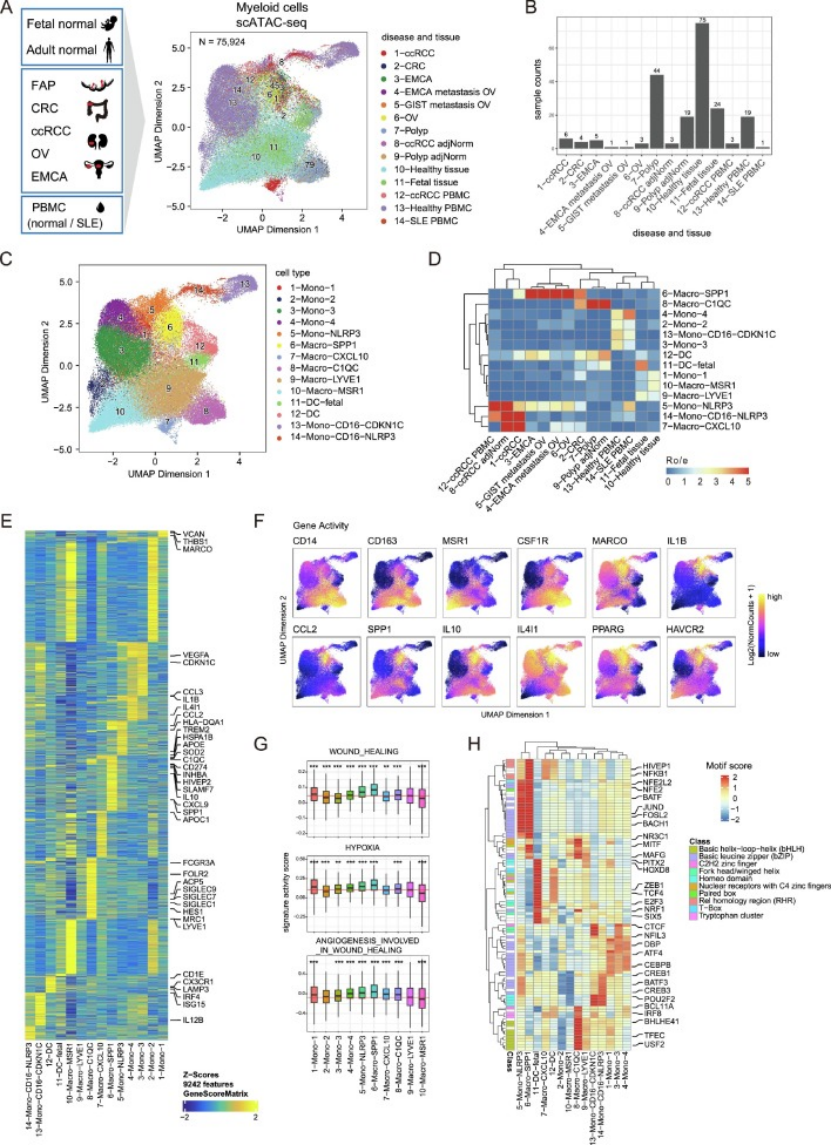
图1
第二步:多组学整合 + 超级增强子分析,证实 TAM 超级增强子特征为泛癌独立预后标志物(图 2)
多组学整合:将 scATAC-seq 与泛癌髓系细胞 scRNA-seq 数据整合,验证基因表达与染色质可及性高度匹配,构建峰 - 基因链接,发现 SPP1、PPARG 等促瘤基因的表达与增强子可及性显著相关(图 2A-C);
关键转录因子筛选:通过转录因子表达与基序可及性的相关性分析,筛选出 KLF2、CEBPB、MAF 等髓系细胞正调控转录因子(图 2D);
超级增强子分析:鉴定出 Macro-SPP1、Macro-C1QC 的超级增强子调控基因,其中 Macro-SPP1 超级增强子靶基因富集炎症反应、IL10 信号、血管生成等促瘤通路(图 2E-F);
临床预后验证:基于 TCGA 泛癌数据的生存分析显示,Macro-SPP1 超级增强子调控基因特征评分高的患者,在 18 种癌种中均表现出较差的总生存期,且该特征的预后价值独立于 M2 巨噬细胞浸润比例(图 2G-H),证实其为泛癌预后生物标志物。
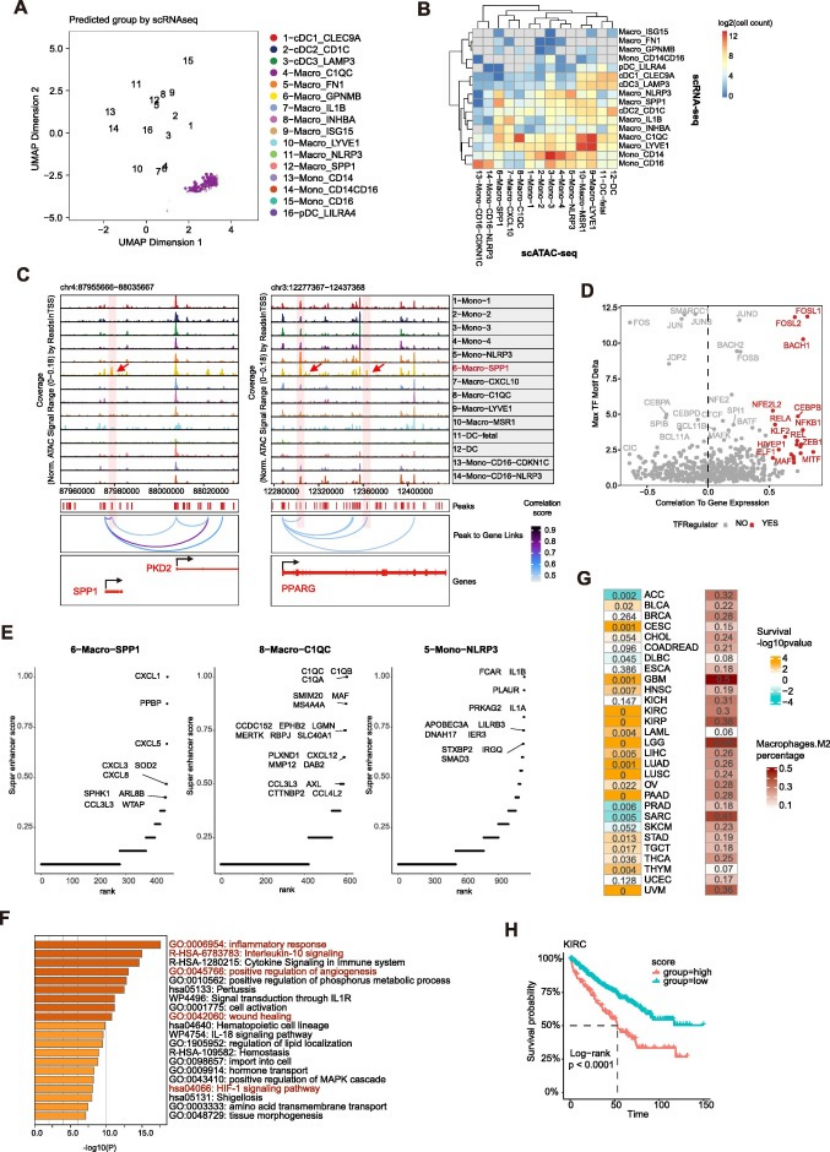
图2
第三步:表观轨迹分析,揭示两种促瘤 TAM 亚型的独特分化来源与调控级联(图 3)
轨迹构建:通过 Monocle3 和 PAGA 无监督轨迹分析,首次明确外周单核细胞经 Mono-NLRP3 中间阶段分化为 Macro-SPP1,TRMs(Macro-LYVE1)直接分化为 Macro-C1QC 的表观轨迹(图 3A-C);
阶段特异性调控:单核细胞向 Macro-SPP1 分化中,先激活 NF-κB、AP-1 家族因子引发炎症反应,后期 PPARG、NFAT5 等驱动终末促瘤表型;TRMs 向 Macro-C1QC 分化则依赖 MAF、PRDM1、HES1 等转录因子(图 3D-E);
核心调控因子鉴定:通过基序评分、基因表达、染色质可及性三重筛选,确定PPARG、NFAT5、MECP2 为 Macro-SPP1 核心调控因子,MAF、HES1、PRDM1 为 Macro-C1QC 核心调控因子(图 3F-H),为后续功能验证锁定关键靶点。
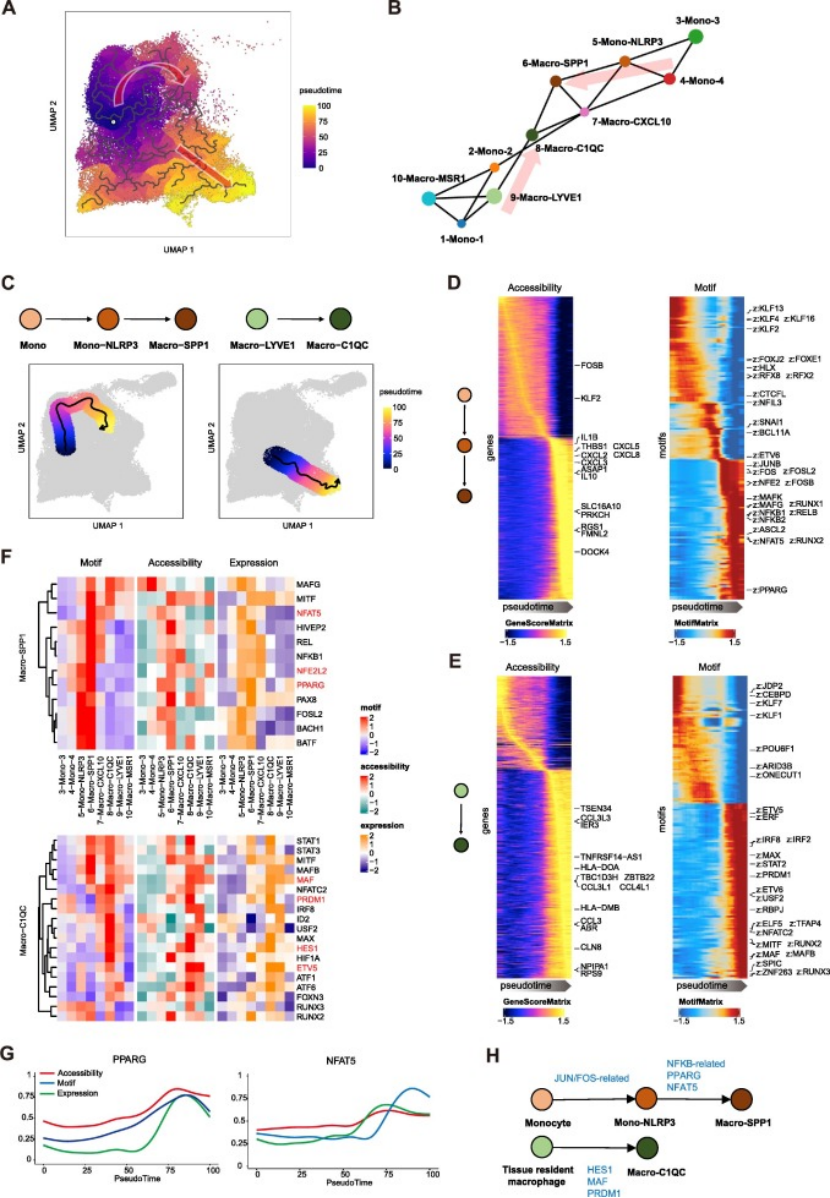
图3
第四步:体外细胞模型功能验证,证实核心转录因子调控促瘤 TAM 极化的关键作用(图 4)
巨噬细胞极化模型构建:将人 THP-1 单核细胞诱导为 M0 巨噬细胞,再分别极化为 M1(IFN-γ+LPS)和 M2(IL-4)巨噬细胞,通过流式和 qPCR 验证极化表型(图 4A-C);
因子表达验证:发现 PPARG、NFAT5、MECP2 在 M2 促瘤表型巨噬细胞中显著高表达,与 Macro-SPP1 中的表达特征一致(图 4D);
CRISPR 敲低验证:敲低 PPARG、NFAT5、MECP2 后,M2 巨噬细胞的 CD206、CD163 等促瘤标志物的 mRNA 和蛋白水平均显著降低(图 4E-G);
肿瘤条件培养基验证:在肿瘤细胞条件培养基诱导的 TAM 样 M2 巨噬细胞中,敲低上述因子同样显著抑制促瘤表型,且 NFAT5 靶基因富集 IL-10、HIF-1 等促瘤通路(图 4H-J),证实其为促瘤 TAM 极化的核心调控因子。
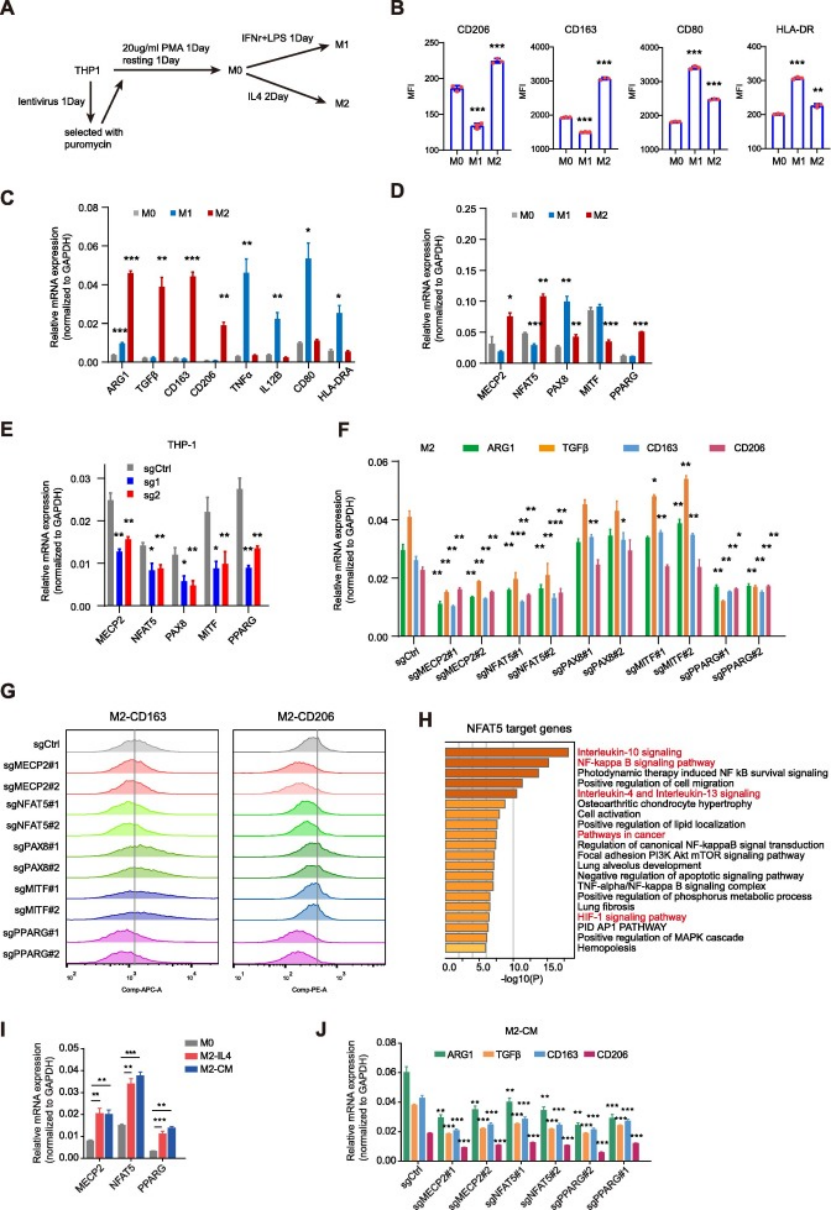
图4
第五步:顺式调控元件分类分析,证实促瘤 TAM 基因以 “启动子组成型可及 + 增强子动态调控” 为特征(图 5)
基因分类标准:根据基因表达与启动子 / 增强子可及性的关联,将促瘤 TAM 相关基因分为 5 类,其中E 型基因(表达仅与增强子可及性相关,启动子组成型可及)为核心类型(图 5A);
泛癌特征:Macro-SPP1 相关基因中 71.2% 为 E 型基因(含 NFAT5、CCL2),19.6% 为 PE’型基因(含 SPP1、PPARG),且 E/PE’型基因表达与顺式调控元件可及性相关性更高(图 5B-C);
临床相关性:E 型基因相关增强子显著富集癌症风险 GWAS 精细定位 SNP,且其靶基因富集伤口愈合、血管生成等促瘤通路(图 5D-E),证实其临床相关性;
增强子功能验证:CRISPR 敲除 NFAT5 的 Macro-SPP1 特异性增强子后,NFAT5 表达及 M2 巨噬细胞促瘤标志物均显著降低(图 5F-I),证实增强子对促瘤 TAM 极化的关键调控作用。
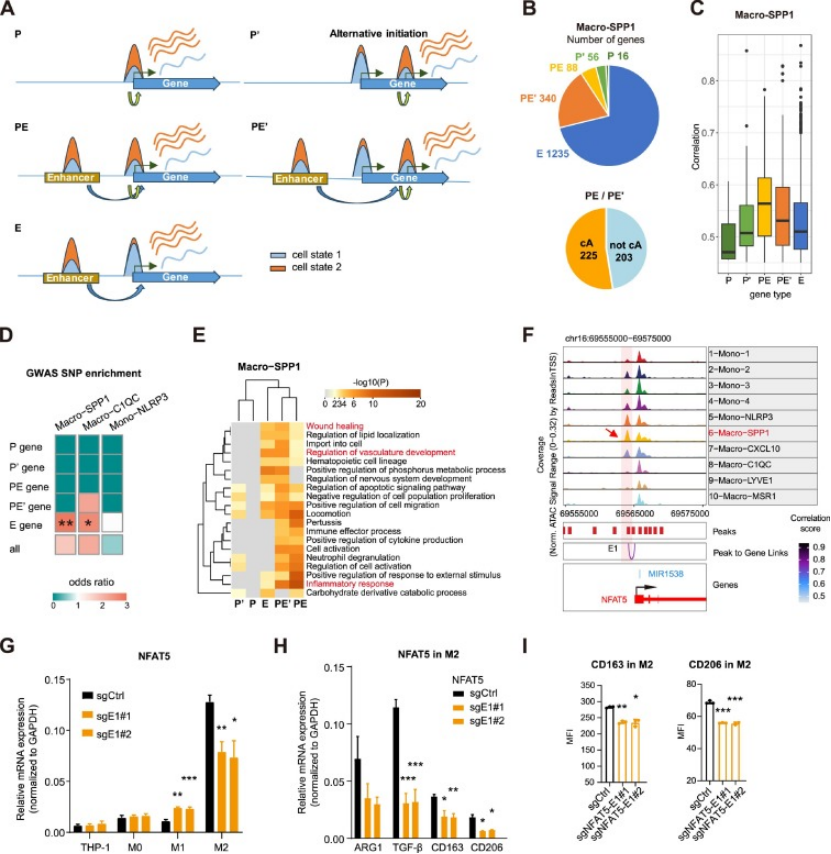
图5
第六步:Pol II 暂停机制解析 + 功能验证,证实增强子通过调控 Pol II 暂停释放驱动促瘤 TAM 形成(图 6)
Pol II 暂停特征分析:利用小鼠骨髓源巨噬细胞 Pol II ChIP-seq 数据,发现 Macro-SPP1 相关 E 型 / PE’型基因在静息巨噬细胞中 Pol II 暂停指数高,IL-4 诱导的 M2 极化后暂停指数显著降低,提示 Pol II 暂停释放为基因激活关键(图 6A);
关键靶基因验证:选择 HIPK2(E 型促瘤基因)为研究对象,证实其在 M2 巨噬细胞中高表达,敲低 HIPK2 可显著抑制 M2 促瘤表型(图 6B-G);
增强子调控 Pol II 暂停验证:敲除 HIPK2 的 Macro-SPP1 特异性增强子 E1/E4 后,HIPK2 表达显著降低,且其启动子区 Pol II 富集增加、基因体区 Pol II 富集减少,表明 Pol II 暂停释放受阻(图 6H-K);
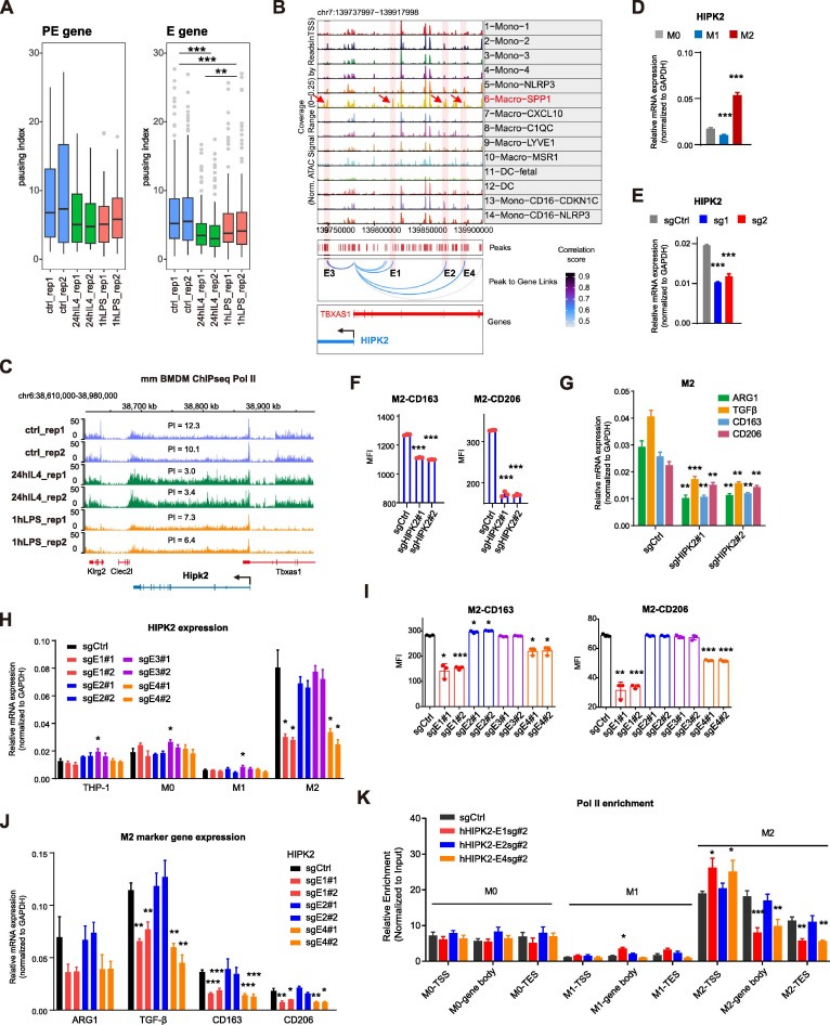
图6
核心机制结论:促瘤 TAM 特异性增强子通过调控靶基因的 Pol II 暂停释放,驱动巨噬细胞向促瘤表型极化,而非通过改变启动子可及性。
延伸研究:解析 TAMs 调控的癌种特异性与发育阶段特异性(图 7、S7)
癌种特异性:不同癌种 TAMs 在共有促瘤特征外,存在独特的激活基因和调控基序,如卵巢癌 TAMs 富集伤口愈合通路、肾透明细胞癌 TAMs 富集 MAPK 信号(图 S7);
发育阶段特异性:对比健康胎儿 / 成人组织巨噬细胞,发现胎儿巨噬细胞由 HOXD8 等因子调控,成人巨噬细胞则富集与促瘤 TAMs 一致的 Jun 家族因子,且巨噬细胞表观遗传异质性具有组织特异性(图 7)。
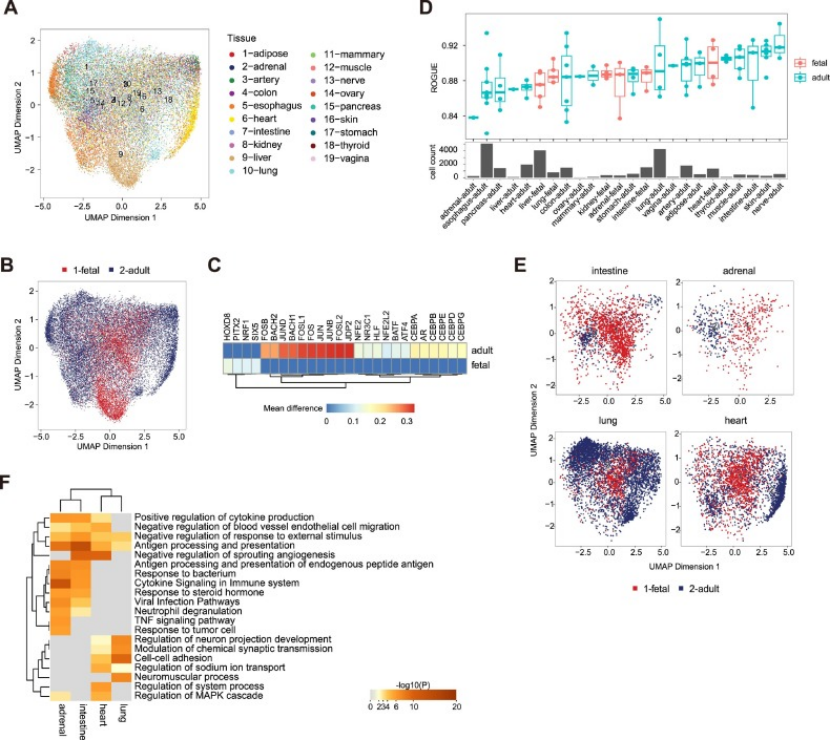
图7
多组学发文经典范式总结
天津医科大学团队的这篇泛癌研究,为临床医生开展多组学研究提供了从研究设计→技术选择→结果验证→临床转化 的完整顶刊发文范式,核心要点可总结为 3 点:
1. 选题:从临床痛点出发,锚定 “泛癌共性 / 癌种特异性” 科学问题
以 TAMs 异质分化的表观调控盲区这一免疫治疗核心痛点为切入点,突破单一癌种研究局限,以泛癌视角分析 TAMs 调控的共性规律,同时延伸解析癌种 / 发育阶段特异性,既保证了研究的广度,又体现了深度,契合顶刊对研究创新性和系统性的要求。
2. 技术:以 “单细胞多组学” 为核心,实现 “表观 + 转录” 多维度整合
核心采用单细胞 ATAC-seq(表观)+scRNA-seq(转录)多组学技术,结合公共数据库挖掘,先通过表观组绘制细胞分型和轨迹,再通过转录组验证基因表达特征,构建 “峰 - 基因链接” 实现多组学数据的深度整合,同时结合 GWAS、TCGA 数据库完成临床相关性分析,让多组学数据不仅有机制意义,更有临床价值。
3. 验证:遵循 “生信挖掘→体外模型→功能实验” 的层层验证逻辑
生信挖掘筛选出的核心亚型、转录因子、增强子,均通过体外细胞模型(THP-1 巨噬细胞极化、肿瘤条件培养基诱导 TAM)和功能实验(CRISPR 敲低 / 敲除、ChIP-seq、流式、qPCR)进行验证,同时结合小鼠骨髓源巨噬细胞数据进行跨物种机制验证,让生信结论有坚实的实验支撑,符合顶刊对研究可靠性的要求。
4. 转化:从机制到临床,挖掘 “预后标志物 + 治疗靶点” 双重临床价值
研究不仅解析了促瘤 TAM 形成的核心表观机制,还鉴定出促瘤 TAM 超级增强子特征 这一泛癌预后标志物,同时发现促瘤 TAM 特异性增强子、Pol II 暂停调控通路 为潜在免疫治疗靶点,实现了 “机制研究→临床标志物→治疗靶点” 的临床转化,让研究具备明确的临床应用前景,提升了文章的临床价值。
研究结论与临床意义
天津医科大学团队通过单细胞多组学整合 + 泛癌分析 + 体外功能验证,首次绘制了人类 TAMs 的泛癌表观遗传图谱,明确了外周单核细胞 / TRMs 分化为 SPP1+/C1QC + 促瘤 TAM 的独特表观轨迹及核心调控因子,揭示了增强子驱动的 Pol II 暂停调控 是促瘤 TAM 异质形成的核心机制,且促瘤 TAM 超级增强子特征可作为泛癌独立预后标志物。
该研究的最大突破在于,打破了传统对 TAMs 调控的转录因子层面研究,从表观遗传 - 转录延伸层面阐明了促瘤 TAM 形成的全新机制,为靶向 TAMs 的肿瘤免疫治疗提供了增强子、Pol II 暂停通路 等全新表观遗传靶点,同时为临床医生开展多组学研究提供了可复制的顶刊发文范式,兼具科学价值与临床转化意义。
DOI: 10.1016/j.jare.2026.01.048
专注期刊投稿、发表十年,任何投稿、写作难题欢迎咨询!

PAPER INFORMATION

快速预审、投刊前指导、专业学术评审,对文章进行评价

校对编辑、深度润色,让稿 件符合学术规范,格式体例等标准
.png)
适用于语句和结构尚需完善和调整的中文文章,确保稿件达到要求
.png)
数据库包括: 期刊、文书籍、会议、预印章、书、百科全书和摘要等

让作者在期刊选择时避免走弯路,缩短稿件被接收的周期

根据目标期刊格式要求对作者文章进行全面的格式修改和调整
.png)
帮助作者将稿件提交至目标期刊投稿系统,降低退稿或拒稿率
.png)
按照您提供的稿件内容,指导完成投稿附信(cover letter)

北京总部:北京市海淀区碧桐园 3 号楼 2 层 211 广州办事处:广州市黄埔区科学城国际企业孵化器 E栋306 联系人:客服 / 18163670350
Copyright © 2022-2024 北京特诺科技有限公司 版权所有 备案/许可证编号为: 京 ICP 备 2023007944 号