
来源:科诺科研
在生物医学工程领域,水凝胶作为一种极具潜力的组织修复与密封材料,长期以来受困于一个根本性矛盾:要想承受体内复杂的力学环境,水凝胶需要高度交联的致密网络来提供结构强度;而要想在湿润、动态的组织表面实现牢固粘附,又需要界面高分子链具备足够的运动能力来重新排列并与组织形成键合。这种源于氢键竞争性分布的“强度-粘附权衡”困境,严重限制了高性能组织密封材料的临床转化。无论是传统的聚乙二醇二丙烯酸酯单网络体系,还是明胶甲基丙烯酰水凝胶,都难以在同一材料体系中同时实现优异的力学性能和可靠的湿态粘附。如何从分子层面破解这一矛盾,成为该领域亟待突破的核心科学问题。
针对这一挑战,浙江大学吴梦婕教授、贺永教授和四川大学华西口腔医院朱舟副教授合作,提出了一种颠覆性的“熵驱动氢键重组”策略。研究团队通过巧妙设计,构建了一种层级熵介导的双相水凝胶。该材料在热活化下首先进入高熵混合状态,随后通过熵驱动的氢键重新分布,诱导发生局部相分离,在材料内部形成刚性的聚乙二醇二丙烯酸酯增强骨架与柔性的明胶富集界面域。这种独特的结构设计使得氢键得以在体相中集中形成致密网络以提供力学增强,同时在界面处形成氢键贫乏的纳米限域水层,为动态的聚合物-组织氢键结合创造了条件,从而一举打破了传统水凝胶中内聚强度与界面粘附之间的固有矛盾。实验数据显示,该水凝胶的模量高达约13兆帕,能够承受高达368毫米汞柱的静水压力——这一数值远超人体生理动脉压和心脏破裂阈值,甚至在动态搏动性出血模型中实现了即时、牢固的密封。相关论文以“Tough Hydrogels with Robust Wet Adhesion via Entropy-Driven Hydrogen Bond Reorganization”为题,发表在Advanced Materials上。

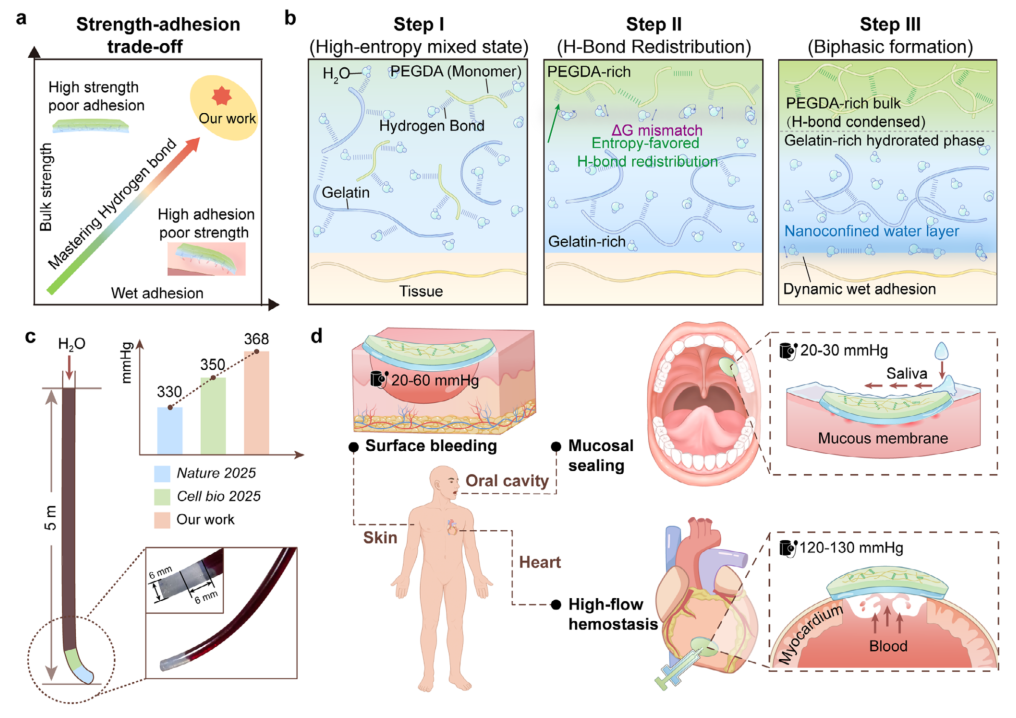
图1 | HEBH的设计概念、相分离架构及多组织适应性。(a) 本体材料强度与界面粘附之间固有矛盾的示意图。(b) 熵驱动氢键重组及相分离导致HEBH形成的示意图。(c) 用于模拟高达5米水头(368 mmHg)生理压力的静水密封实验装置(p = ρgh)。(d) 代表性生物场景,包括皮肤密封、黏膜粘附及高流量心脏止血,展示了HEBH广泛的功能适应性。
在结构表征层面,研究团队通过扫描电镜和能谱分析揭示了该材料的微观奥秘。纯聚乙二醇二丙烯酸酯水凝胶表面光滑致密,呈现单相合成网络的均质特征;而纯明胶水凝胶则表现出粗糙、片状且脆性的断裂表面。与之形成鲜明对比的是,层级熵介导的双相水凝胶展现出清晰的相分离形貌:柔顺的明胶微区与刚性的聚乙二醇二丙烯酸酯网络在微米尺度上相互穿插,形成了粗糙的区域和界面边界。能谱元素面分布图进一步证实了这种双相结构,碳、氧、氮元素在复合体系中呈现分散且互补的分布模式,确证了相分离的发生以及双相结构的形成。X射线光电子能谱分析则从分子层面揭示了交联前后表面化学状态的变化:交联后,碳-氧和碳=氧键的相对分数分别从18%和9%增至24%和12%,羟基/吸附氧组分从42%升至58%,而氮元素峰面积从6%显著增加至14%,表明交联过程不仅稳定了聚乙二醇二丙烯酸酯骨架,还有效调控了表面极性和氢键能力,为后续的结构重组提供了分子基础。
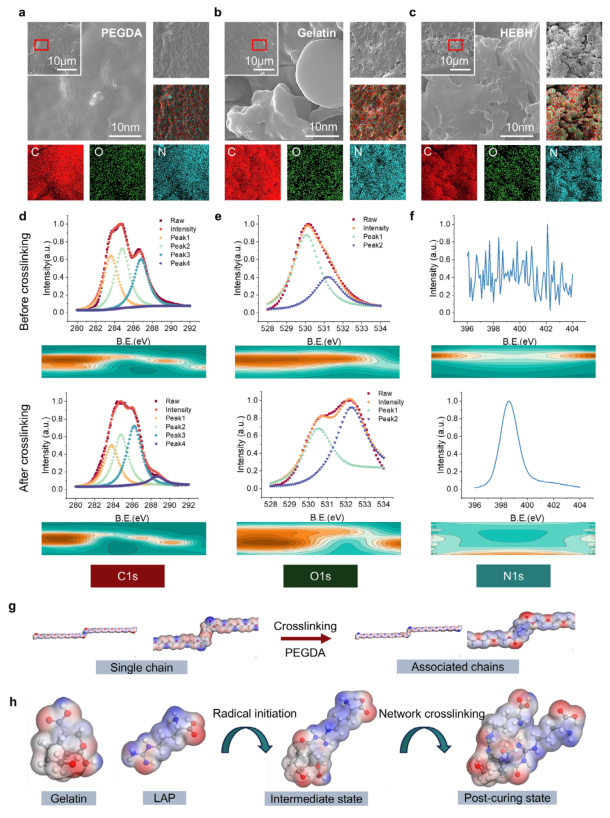
图2 | PEGDA、明胶和HEBH水凝胶的结构与化学表征。(a-c) (a) PEGDA、(b) 明胶和(c) HEBH的SEM图像及EDS元素分布图,展示表面形貌及C、O、N分布。(d-f) 交联前后(d) C1s、(e) O1s和(f) N1s的XPS分析,包括高分辨谱图及伪彩色强度图。(g) 交联前后PEGDA链的分子表示,展示从线型链到共价连接网络片段的转变。(h) 显示LAP激活、自由基生成及体系中后续交联过程的光化学途径示意图。
力学性能测试进一步验证了该材料的卓越表现。在单轴压缩试验中,层级熵介导的双相水凝胶表现出显著的应变硬化行为,应力-应变曲线较传统水凝胶明显更加陡峭,且能在承受大应变的同时不发生破裂。拉伸测试显示,该水凝胶同时实现了更高的拉伸应力和更大的断裂伸长率,标志着刚度和延展性的协同增强。仪器化压痕测试则证实了其优越的承载和回复能力,表现为更高的峰值载荷和更宽、更滞后的加载-卸载曲线,这与材料内部高效的能量耗散机制高度吻合。为从分子层面解释这些宏观力学特性,研究团队开展了相场和原子尺度模拟。结果显示,纯聚乙二醇二丙烯酸酯呈现均匀的层状网络,分子链伸展且缠结有限;明胶则呈现碎片化的马赛克状结构,分子链呈高度柔顺的线圈构象;而层级熵介导的双相水凝胶则整合了两者的结构优势,聚乙二醇二丙烯酸酯富集区与明胶富集区紧密交织,刚性与柔性域并存。局部自由能景观分析进一步揭示,该水凝胶形成了多个被有限能垒分隔的局部极小值,使其在受载时能够通过亚稳微区的渐进式重组来分配和耗散机械能,而非将能量集中于单一的破坏事件,从而实现了高强度、高韧性与可恢复性的统一。
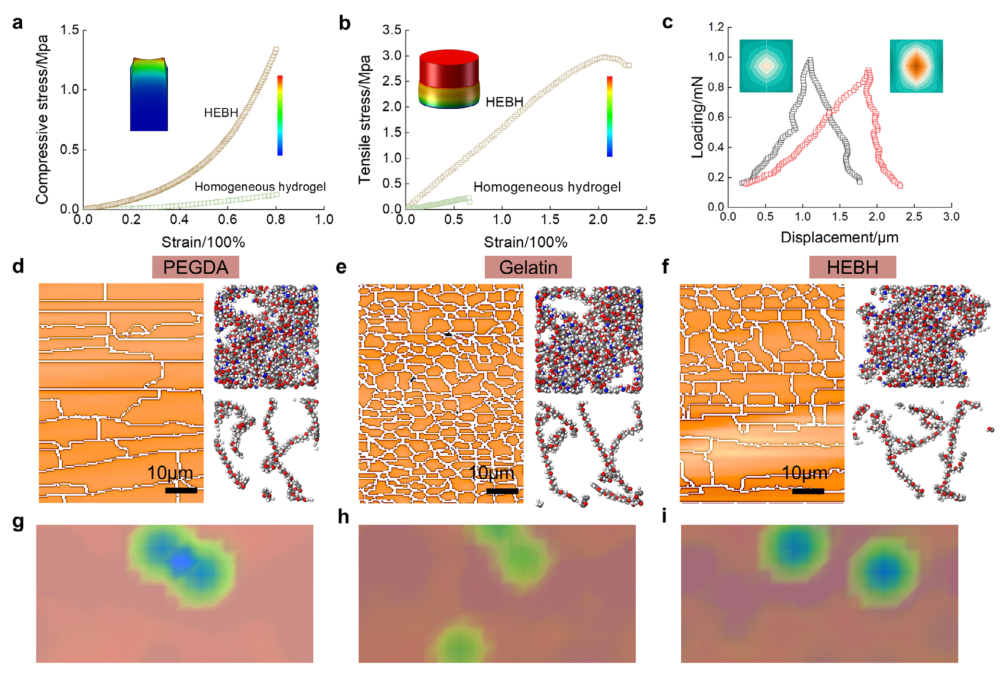
图3 | PEGDA、明胶和HEBH水凝胶的力学性能及多尺度模拟。(a-c) 宏观力学测试。(a) HEBH与传统水凝胶的压缩应力-应变曲线,插图为有限元应变分布图。(b) 拉伸应力-应变曲线及相应变形图。(c) 仪器化压痕加载-位移曲线,插图为代表性接触变形场。(d-f) 网络结构的相场模拟及原子模型。(d) PEGDA、(e) 明胶和(f) HEBH的相场图(左)及相应原子模型(右),展示域组织、链构象及网络均匀性的差异。(g-i) 局部自由能景观分析。(g) PEGDA、(h) 明胶和(i) HEBH的局部自由能极小值空间分布。
在动态高压生理环境中的应用验证中,该水凝胶展现了令人瞩目的止血密封能力。研究人员首先在大鼠跳动心脏上制造心室切口,在湿润的心肌表面滴加水凝胶前体溶液并光照激活后,仅需数秒便形成了紧密贴合的弹性薄膜,实现了即刻止血。该薄膜在整个心动周期中始终与动态收缩的心肌保持紧密接触,无一例再出血或脱落。随后,研究团队建立了更具挑战性的兔心室穿刺模型:用细针穿透心室壁造成节律性高压喷血。将层级熵介导的双相水凝胶喷涂于穿孔部位并原位交联后,材料迅速形成牢固锚定于缺损边缘的粘性插头,成功抵抗了心室内高压,无需缝合即可实现完全持久的止血。作为对照,纯聚乙二醇二丙烯酸酯水凝胶因湿态粘附差而脱落,纯明胶水凝胶则因内聚强度不足而移位,均无法维持密封。这一结果凸显了刚性-柔性耦合结构在心脏密封应用中的独特优势:聚乙二醇二丙烯酸酯富集相提供结构鲁棒性和能量耗散,明胶富集域贡献柔韧性和界面粘附,而快速交联则将两相整合为具有组织顺应性的一体化栓塞。
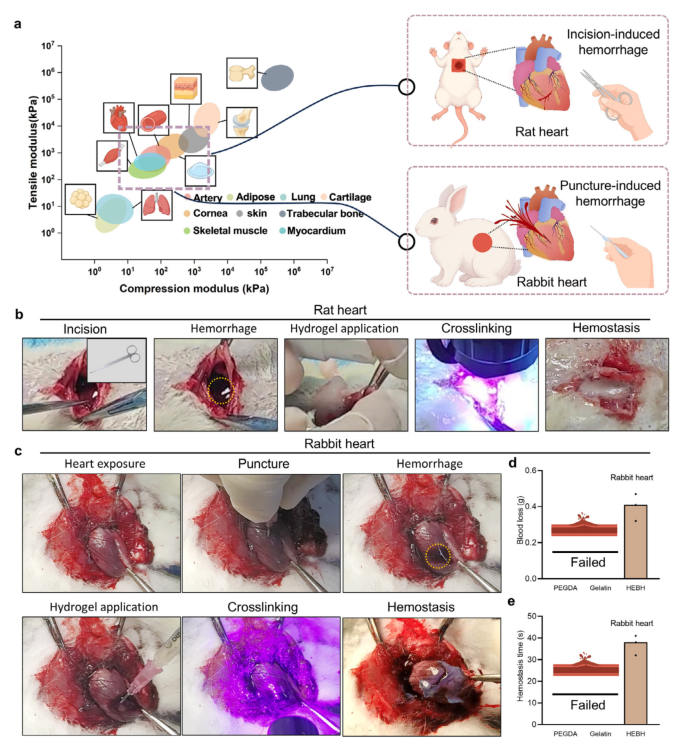
图4 | HEBH在高压动态条件下的即时止血密封。(a) HEBH及代表性生物组织基于报道的拉伸与压缩模量范围的力学图谱。虚线框表示机械测试获得的HEBH模量范围,组织区域表示文献报道范围。(b) 大鼠心脏切口模型:出血、水凝胶施加、交联及止血过程。(c) 兔心室穿刺模型:穿刺、搏动性出血、水凝胶注射、交联及密封过程。(d,e) PEGDA、明胶和HEBH组间密封成功率与止血时间的定量评估(n=3)。由于对照组一致失败,未进行统计学比较。
在更具挑战性的长期湿态环境修复中,该材料同样表现出色。研究人员采用大鼠口腔黏膜溃疡模型——这一组织环境持续湿润、存在酶活性和剪切流,是对材料界面粘附和降解抗性的严苛考验。在此条件下,纯聚乙二醇二丙烯酸酯水凝胶虽能形成初始物理膜,但无法维持粘附,常在唾液剪切和温度波动下脱落,导致上皮修复延迟;组织学评估显示其修复后上皮薄且不连续,黏膜下胶原稀疏。独特的是,纯聚乙二醇二丙烯酸酯处理组的愈合速度甚至慢于未经处理的对照组,这种“反常效应”源于其高度交联、低表面能的惰性网络缺乏极性或粘附官能团,不仅无法整合到组织修复过程中,反而作为非整合的物理屏障隔离了正常的再生信号。相比之下,层级熵介导的双相水凝胶表现出稳健的界面粘附、优异的抗流体冲刷能力和稳定的屏障完整性,有效加速了伤口闭合,并形成了结构良好的再生组织。
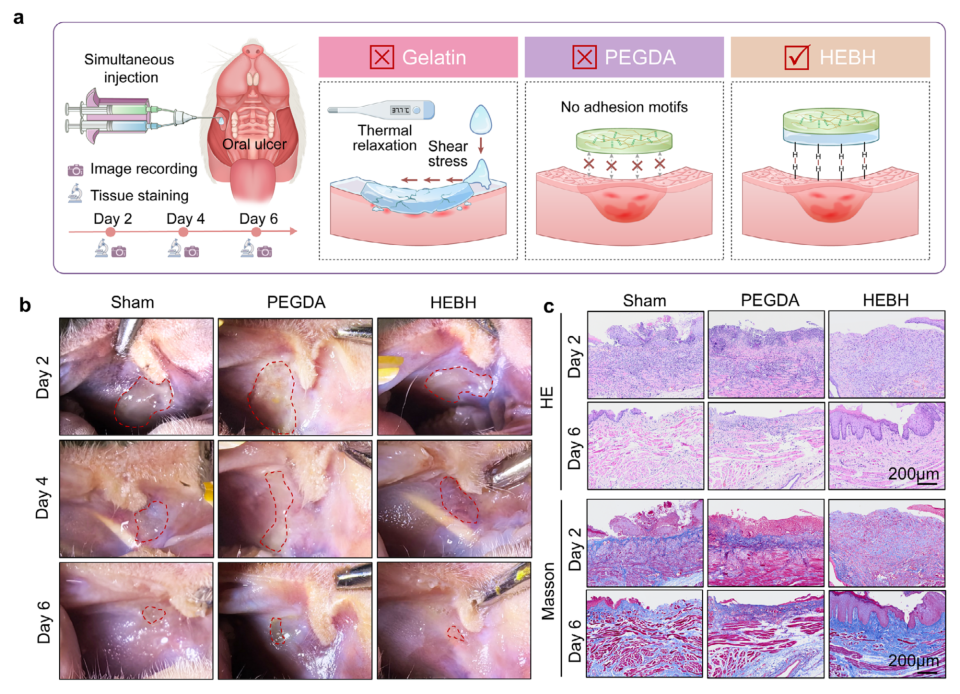
图5 | HEBH在口腔黏膜溃疡模型中实现持久的湿粘附与适应性愈合。(a) 用于动态潮湿环境测试的口腔黏膜溃疡模型示意图。因明胶快速溶胀与降解而被排除。(b) 治疗后第2、4、6天的口腔内连续照片,展示溃疡部位的愈合进程。(c) 相应时间点的H&E和Masson染色,评估上皮完整性与细胞外基质组织。
在全层皮肤缺损模型中,该材料进一步验证了其在力学负载和相对干燥环境下的修复效能。未经处理的对照组愈合缓慢,第14天时仍可见明显缺损;聚乙二醇二丙烯酸酯组虽因力学刚度诱导了部分收缩,但边缘不规则且上皮化不全;明胶组由于力学鲁棒性不足,长期密封效果受限。而层级熵介导的双相水凝胶处理的伤口在第14天时几乎完全闭合,边缘平整,表皮分层良好。组织学染色显示,该组形成了致密且排列有序的胶原束,伴有连续的表皮覆盖。定量分析进一步证实,其细胞核密度指数和胶原体积分数均显著优于其他各组,标志着增强的上皮再生和细胞外基质重塑能力。体外细胞相容性实验和体内主要脏器组织学评估也确认了该材料良好的生物安全性。
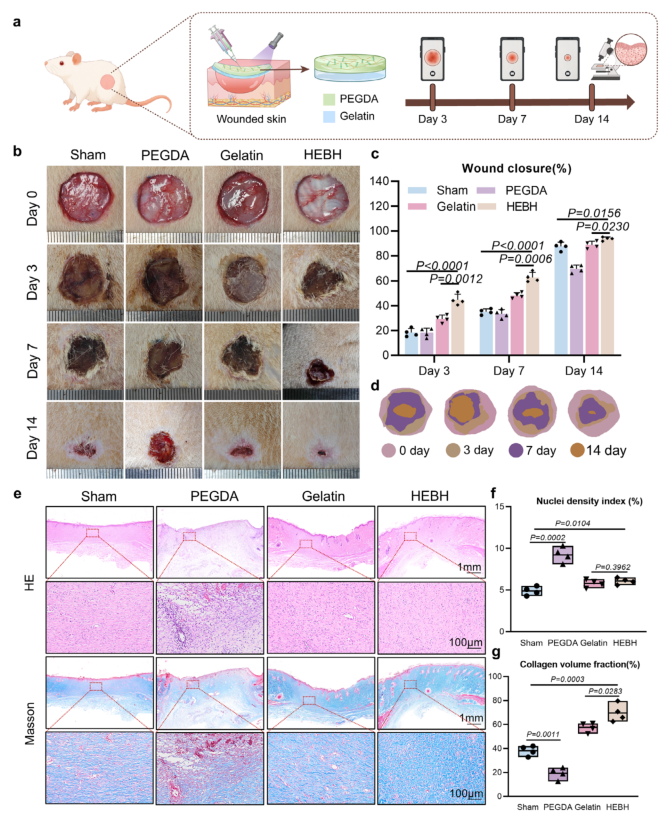
图6 | HEBH在皮肤伤口模型中的密封与再生性能。(a) 全层皮肤缺损模型及治疗组示意图。(b) 第0、3、7和14天伤口愈合进程的代表性照片记录。(c) 通过ImageJ面积法量化的伤口闭合率随时间变化曲线(n=4)。(d) 第0、3、7和14天伤口闭合示意图。(e) 用于表皮和胶原评估的代表性H&E和Masson三色染色。(f) 量化细胞增殖的细胞核密度指数(n=4)。(g) 根据组织学切片量化的胶原体积分数(n=4)。组间差异通过单因素方差分析进行评估,方差齐性经Levene检验验证;当假设违反时应用Welch方差分析。事后比较根据需要采用Tukey或Games-Howell检验。数据以均值±标准误表示。
总结而言,这项研究建立了一种全新的熵介导策略,从根本原理上破解了水凝胶材料中体相强度与湿态粘附之间的固有冲突。所提出的熵驱动氢键重组与相分离机制,使材料能够自发组装形成刚柔并济的双相结构,同时在体相和界面分别实现力学增强与动态粘附。该水凝胶在极端条件下的卓越表现——包括承受368毫米汞柱静水压力的密封能力以及在搏动性出血模型中的即时止血效果——为熵介导策略的有效性提供了极具说服力的证据。这一突破不仅为设计具有“兼不相容”特性的高性能水凝胶开辟了新路径,更为皮肤损伤、口腔黏膜溃疡及心脏出血等复杂临床场景下的组织修复提供了富有前景的解决方案,有望推动医用密封胶材料从“结构替代”向“功能整合”的范式转变。
专注期刊投稿、发表十年,任何投稿、写作难题欢迎咨询!

PAPER INFORMATION

快速预审、投刊前指导、专业学术评审,对文章进行评价

校对编辑、深度润色,让稿 件符合学术规范,格式体例等标准
.png)
适用于语句和结构尚需完善和调整的中文文章,确保稿件达到要求
.png)
数据库包括: 期刊、文书籍、会议、预印章、书、百科全书和摘要等

让作者在期刊选择时避免走弯路,缩短稿件被接收的周期

根据目标期刊格式要求对作者文章进行全面的格式修改和调整
.png)
帮助作者将稿件提交至目标期刊投稿系统,降低退稿或拒稿率
.png)
按照您提供的稿件内容,指导完成投稿附信(cover letter)

北京总部:北京市海淀区碧桐园 3 号楼 2 层 211 广州办事处:广州市黄埔区科学城国际企业孵化器 E栋306 联系人:客服 / 18163670350
Copyright © 2022-2024 北京特诺科技有限公司 版权所有 备案/许可证编号为: 京 ICP 备 2023007944 号